
�±���ʵ�顰�����������롰���ۡ���Ӧ��ϵ��ȷ��һ����
���������� | ���� | |
A | ���еμ�����Ũ���ᣬ������������ͨ�뱽������Һ����Һ����� | ���ԣ����̼����� |
B | ȡij��Һ���������������ữ���Ȼ�����Һ�����ְ�ɫ���� | ����Һ��һ�����д�����SO42�� |
C | ȡ����Fe(NO3)2������ˮ�ܽ⣬��ϡ�����ữ���μ�KSCN��Һ����Һ��ΪѪ��ɫ | ��Fe(NO3)2�����Ѿ����� |
D | �����Ƶ�������Һ�Թ��м���������������Һ����ˮԡ���ȣ��Թ��ڱڸ���һ������ɫ���� | �������ǻ�ԭ���� |
 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭ʡ����ʮУ������߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ������
�绯ѧԭ���ڻ�ѧ��ҵ���й㷺��Ӧ�ã��������ͼ�ش����⣺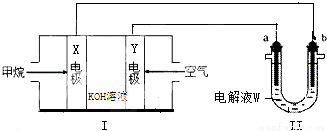
��1��װ�â��е�X�缫�������� ��Y�缫�ĵ缫��ӦʽΪ ������һ��ʱ����Һ��PH�� �����������С���������䡱����
��2����װ�â���a��b��ΪPt�缫��WΪ����ʳ��ˮ�����м��η�̪����ʵ�鿪ʼ�۲쵽b�缫��Χ��Һ���ɫ����ԭ���ǣ��õ缫��Ӧʽ��ʾ�� ��a�缫�������ݲ�����������ĵ���ʽΪ ��
��3��������װ�â����ͭ�ľ�������a�缫�IJ���Ϊ ������һ��ʱ���װ�â���Һ��c��Cu2+���� �����������С���������䡱����
��4����װ�â���aΪAg����bΪͭ����WΪAgNO3��Һ������һ��ʱ�����ͭ������2.1.6g����������·�ĵ��ӵ����ʵ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʦ����ѧ������ѧ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��2Fe + 3Br2��2FeBr3��Fe2+�Ļ�ԭ�Դ���Br��������16.8 g����0.3 mol Br2��Ӧ�����ˮ�õ�������Һ��ͨ��a mol Cl2��������������ȷ����
A����a = 0.1ʱ�������ķ�ӦΪ2Fe2++Cl2��2Fe3++2Cl��
B����a = 0.45ʱ�������ķ�ӦΪ2Fe2++4Br��+3Cl2��2Fe3++2Br2+6Cl��
C������Һ��Br����һ�뱻����ʱ�� c(Fe3+): c(Br��):c(Cl��) ��1:1:3
D����0��a��0.15ʱ����Һ��ʼ������2c(Fe2+)+3c(Fe3+)+c(H+)��c(Cl��)+c(Br��)+ c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ͬλ��ʾ�ٷ������ڷ�Ӧ�������о������з�Ӧ��ͬλ��ʾ�ٱ�ʾ��ȷ���ǣ� ��
A.2Na218O2 + 2H2O = 4Na18OH + O2��
B.2KMnO4 + 5H218O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 518O2�� + 8H2O
C.NH3�� 2H2O + HCl =NH4Cl + 2H2O
D.K37ClO3 + 6HCl = K37Cl + 3Cl2 ��+ 3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ�������ĴΣ�12�£��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A���Ʋ�������������п�����������������������е�������ʴ
B��SO2(g) + 2H2S(g) = 3S(s)+2H2O(l) �ڳ��������Է����У���÷�Ӧ�ġ�H��0
C��0.1 mol��L��1CH3COOH��Һ�м�������ˮ��CH3COOH����̶Ⱥ���ҺpH������
D����N2+3H2 2NH3ƽ����ϵ�м���������������Ӧ���ʺ�ƽ�ⳣ��������
2NH3ƽ����ϵ�м���������������Ӧ���ʺ�ƽ�ⳣ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ�ڵڰ˴δ�ѧ�Ծ��������棩 ���ͣ�ѡ����
CO2����ˮ����̼�ᡣ��֪�������ݣ�
������� | H2CO3 |
|
����ƽ�ⳣ����250C�� | Ka1=4.30��10-7 Ka2=5.61��10-11 | Kb=1.77��10-5 |
���г�����1 mol�� L-1��(NH4)2CO3��Һ����֪NH4+��ˮ��ƽ�ⳣ�� 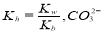 ��һ��ˮ���ƽ�ⳣ��
��һ��ˮ���ƽ�ⳣ��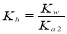 ������˵����ȷ����
������˵����ȷ����
A�������ݿ��жϸ���Һ������
B��c(NH4+)>c(HCO3-)>c(CO32-)>c(NH3��H2O)
C��c(NH4+)+c(NH3��H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
D��c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����������·��һ��ѧ������ѧ��10���¿�����ѧ�Ծ��������棩 ���ͣ������
��ҵ����ȡ����淋�����ͼ��ͼ1����ش��������⣺
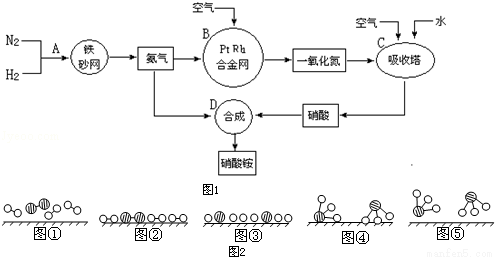
��1����������ҵ������������У�B�豸�������� �����з�����Ӧ�Ļ�ѧ����ʽΪ ��
��2�������������У�N2��H2�ϳ�NH3���õĴ����� ��
1909�껯ѧ�ҹ�����ʵ�����״κϳ��˰���2007�껯ѧ�Ҹ����•���ض��ڹ����о���֤ʵ�������뵪���ڹ����������ϳɰ��ķ�Ӧ���̡�ʾ��ͼ��ͼ2�� �ֱ��ʾN2��H2��NH3��ͼ�ݱ�ʾ���ɵ�NH3�뿪�������棬ͼ�ں�ͼ�۵ĺ���ֱ��� �� ��
�ֱ��ʾN2��H2��NH3��ͼ�ݱ�ʾ���ɵ�NH3�뿪�������棬ͼ�ں�ͼ�۵ĺ���ֱ��� �� ��
��3���ںϳɰ����豸���ϳ������У������Ƚ�������Ŀ���� ���ںϳ��������������ͨ�������Ŀ���� ��
��4����������Ĺ����г������һЩ��������������������ַ���������
��Һ���շ���NO+NO2+2NaOH��2NaNO2+H2O
������ԭ����8NH3+6NO2 7N2+12H2O��NOҲ�����Ƶķ�Ӧ��
7N2+12H2O��NOҲ�����Ƶķ�Ӧ��
�������ַ����У�������ɫ��ѧ���� ��
��5��ij���ʳ���NH3�Ʊ�NH4NO3����֪����NH3��NO�IJ�����96%��NO��HNO3�IJ�����92%������HNO3����ȥ��NH3������ռ�ܺ�NH3������������������ģ��� %��
��6���������һ�ֳ��õĵ��ʣ��������ʹ�øû���ʱ����Ӧע���������������±���
ע������ ����
��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭����Чʵ��ѧ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��A��B���ֶ���������Ԫ�أ�ԭ�Ӱ뾶�ǣ�r��A��<r��B������A��B����Ԫ��ԭ�ӵ�������������ͬ��ѡ���е�m��n��Ϊ��������������˵����ȷ����
A����B��OH��m ��ǿ���A��OH��mһ��Ϊǿ��
B����HnAOm��ǿ�ᣬ��B������������Ӧ��ˮ����һ��Ϊǿ��
C����B�ǽ�������A�����Ƿǽ�������B�Ƿǽ�������A�������ǽ���
D����HnAOm��ǿ�ᣬ��AԪ�ص��⻯���ˮ��Һһ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�챱���г�����������ѧ������ͳ����ѧ�Ծ��������棩 ���ͣ������
��֪�ס��ҡ�������ѧ�������������嵥�ʣ���䷴Ӧ���Ƶû���B����ת����ϵ��ͼ��ʾ��

��1����B������Ԫ����д���±���ǡ��λ���У���Ԫ�ط��ű�ʾ��

��2����֪��Ӧ һ�Ƿ��ȷ�Ӧ������������ϵʾ��ͼ��
һ�Ƿ��ȷ�Ӧ������������ϵʾ��ͼ��

��3��Ϊ�ӿ췴Ӧһ�����ʣ��ɲ�ȡ�Ĵ�ʩ�У��ʵ������¶ȡ�ѡ��ǡ���Ĵ���������ijһ��Ӧ���Ũ�Ⱥ�______________��
��4������һ�Ļ�ѧ����ʽ��_________________��
��5���÷�����Ҳ���Ƶ�B���ͱ���Ӧ�IJ�����A��Ӧ���ɣ������ַ������õ���______(���
��һ����������)��������______________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com