
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 0.2mol/L |
| 5min |
| 0.2 |
| 0.5 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����2molSO3����ͨ��һ�ܱ������У���ƽ�������QkJ��������2SO3��g��?2SO2��g��+O2��g����H=+Q KJ/mol |
| B������0.4molFeBr2����Һ��ͨ��0.2molCl2��ַ�Ӧ��2Fe2++Cl2=2Fe3++2Cl- |
| C��NH4Al��SO4��2��Һ�м���Ba��OH��2��ҺʹSO42-��ȫ������Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4��+2H2O |
| D����FeCl3������Һ�����ˮ����ȡFe��OH��3���壺Fe3++3H2O?Fe��OH��3��+3H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����ͼװ���У���ƿ�г�����������a������ͷ�ι��е�Һ��b������ƿ�ڣ���������ƿ��Ȼ����ɼ�f���ձ��е�Һ��b����Ȫ״��������ռ���������ƿ��a��b�ֱ�����ǣ�������
����ͼװ���У���ƿ�г�����������a������ͷ�ι��е�Һ��b������ƿ�ڣ���������ƿ��Ȼ����ɼ�f���ձ��е�Һ��b����Ȫ״��������ռ���������ƿ��a��b�ֱ�����ǣ�������| ��������a | Һ��b | |
| A | NO2 | ˮ |
| B | C12 | ����ʳ��ˮ |
| C | NH3 | ˮ |
| D | CO2 | 4mol?L-1 NaOH��Һ |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ʵ��������Ҳ��������ͼ��ʾ��װ����ȡ�����������ش��������⣺
��ʵ��������Ҳ��������ͼ��ʾ��װ����ȡ�����������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��H2SO4��Һ�� HSO4- H++SO42- | ��NaHSO4��Һ�� HSO4- H++SO42- | ������ HCl=H++Cl |
| 10% | 29% | 100% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1s22s22p63s23p63d74s2 |
| B��1s22s22p63s23p63d54s1 |
| C��1s22s22p63s23p63d104s24p1 |
| D��1s22s22p63s23p64s2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ | NaF | MgF2 | MgO | SiF4 | SiO2 |
| �۵�/K | 1266 | 1534 | 3125 | 183 | 1983 |
| Ħ��Ӳ�� | 3.2 | 6.0 | 6.5 | 7 |
| CO | C-O | C=O | C��O | ||
���ܣ�kJ?mol
| 357.7 | 798.9 | 1071.9 | ||
| N2 | N-N | N=N | N��N | ||
���ܣ�kJ?mol
| 154.8 | 418.4 | 941.7 |
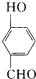 ��
�� 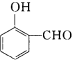 �ķе�
�ķе��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
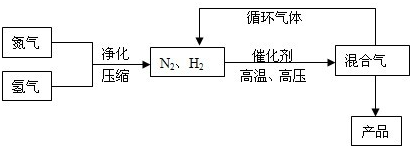
| A�����еķ��ȷ�Ӧ�����ڳ��³�ѹ���Է����� |
| B��Ba��OH��2?8H2O��NH4Cl��Ӧ���ڷ��ȷ�Ӧ |
| C����Ȼ��ȼ��ʱ���仯ѧ��ȫ��ת��Ϊ���� |
| D����Ӧ��ֻ�뷴Ӧ��ϵ��ʼ̬����̬�йأ����뷴Ӧ��;���� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com