
| 化学键 | H-H | Cl-Cl | H-Cl |
| 键能 | 436kJ/mol | 243kJ/mol | 431kJ/mol |
| A. | $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H=-91.5 kJ•mol-1 | |
| B. | H2(g)+Cl2(g)═2HCl(g)△H=-183 kJ•mol-1 | |
| C. | 2HCl(g)═H2(g)+Cl2(g)△H=183 kJ•mol-1 | |
| D. | $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H=91.5 kJ•mol-1 |
分析 根据所给的反应和表格中的键能,先判断出断键吸收的热量和成键放出的热量,然后用断键吸收的热量减去成键放出的热量既得反应热,据此计算.
解答 解:A.$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)=HCl(g)△H=$\frac{1}{2}$×436kJ•mol-1+$\frac{1}{2}$×243 kJ•mol-1-431kJ•mol-1=-91.5kJ•mol-1,故A正确;
B.H2(g)+Cl2(g)=2HCl(g);△H=436kJ•mol-1+243 kJ•mol-1-(2×431)kJ•mol-1=-183 kJ•mol-1,故B正确;
C.2HCl(g)=H2(g)+Cl2(g);△H=(2×431)kJ•mol-1-(436kJ•mol-1+243 kJ•mol-1)△H=+183 kJ/mol故C正确;
D.$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)=HCl(g)△H=$\frac{1}{2}$×436kJ•mol-1+$\frac{1}{2}$×243 kJ•mol-1-431kJ•mol-1=-91.5kJ•mol-1,故D错误;
故选D.
点评 本题从断键和成键的角度考查了热化学方程式的书写,注意热化学方程式中化学计量数只表示该物质的物质的量,不表示物质分子个数或原子个数,因此,它可以是整数,也可以是分数,△H只能写在化学方程式的右边,若为放热反应,则△H为“-”;若为吸热反应,则△H为“+”.其单位一般为kJ/mol.对于同一反应来说,计量系数不同,△H不同,题目难度不大.


科目:高中化学 来源: 题型:实验题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑦ | ||||||
| 3 | ① | ③ | ④ | ⑥ | ⑧ | ⑨ | ⑩ | |
| 4 | ② |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.4 g金属镁变成镁离子时失去的电子数目为0.1NA | |
| B. | 2 g氢气所含原子数目为NA | |
| C. | 1 mol MgCl2固体溶于水中,所得氯离子的数目为NA | |
| D. | 17 g氨气所含电子数目为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该化学反应的过程是吸热的 | |
| B. | 该化学反应的过程是放热的 | |
| C. | 分子运动速率加快,使反应物分子的碰撞机会增多 | |
| D. | 反应物分子的能量增加,活化分子百分数增加,有效碰撞次数增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 固体碳酸钠 | B. | 食醋 | C. | 白酒 | D. | 白糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于25% | B. | 大于25% | C. | 小于25% | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
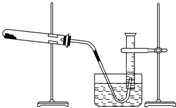 某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量,实验步骤如下:
某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量,实验步骤如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com