
【题目】氯吡格雷是一种用于预防和冶疗因血小板高聚集引起的心、脑及其他动脉循环障碍疾病的药物。以2-氯苯甲醛为原料合成该药物的路线如下:

(1)A分子中“共面的原子数目最多为________个。
(2)C含有多种官能团,能发生缩聚反应。请写出C在一定条件下聚合成高分子化合物的化学方程式____________________。
(3)由E转化为氯吡格雷时,相伴生成的另一种产物的名称为________。
(4)物质G是物质A的同系物,比A多一个碳原子,且能发生银镜反应,除苯环之外无其他环状结构;则符合上述条件的G的同分异构体共有______种。其中核磁共振氢谱中有4个吸收峰,且峰值比为2:2:2:1的结构简式为___________(任写一种)。
(5)已知: ,写出由乙烯、甲醇为有机原料制备化合物
,写出由乙烯、甲醇为有机原料制备化合物 的合成路线流程图___________(无机试剂任选)。合成路线流程图示例如下:
的合成路线流程图___________(无机试剂任选)。合成路线流程图示例如下:

【答案】 14 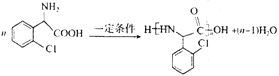 乙二醇 17
乙二醇 17 ![]() 或
或![]()
【解析】(1)苯环、双键均是平面形结构,则A分子中“共面的原子数目最多为14个。(2)C中含有氨基、羧基,二者发生缩聚反应得到高分子化合物,反应的化学方程式为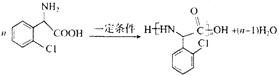 。(3)根据反应前后原子守恒可知由E转化为氯吡格雷时,相伴生成的另一种产物的分子式为HOCH2CH2OH,名称为乙二醇。(4)物质G是物质A的同系物,比A多一个碳原子,即多一个-CH2-原子团,G的一种同分异构体满足:①除苯环之外无其它环状结构;②能发生银镜反应,说明含有醛基,如果苯环上含有一个取代基,则应该是-CHClClO,如果含有2个取代基,应该是-Cl和-CH2CHO或-CH2Cl和-CHO,均有邻间对三种;如果含有3个取代基,应该是-Cl、-CH3、-CHO,根据定一议二可知有10种,共计是17种;其中核磁共振氢谱中有4个吸收峰,且峰值比为2:2:2:1的结构简式为
。(3)根据反应前后原子守恒可知由E转化为氯吡格雷时,相伴生成的另一种产物的分子式为HOCH2CH2OH,名称为乙二醇。(4)物质G是物质A的同系物,比A多一个碳原子,即多一个-CH2-原子团,G的一种同分异构体满足:①除苯环之外无其它环状结构;②能发生银镜反应,说明含有醛基,如果苯环上含有一个取代基,则应该是-CHClClO,如果含有2个取代基,应该是-Cl和-CH2CHO或-CH2Cl和-CHO,均有邻间对三种;如果含有3个取代基,应该是-Cl、-CH3、-CHO,根据定一议二可知有10种,共计是17种;其中核磁共振氢谱中有4个吸收峰,且峰值比为2:2:2:1的结构简式为![]() 或
或![]() 。(5)乙烯与溴发生加成反应生成BrCH2CH2Br,再水解生成乙二醇,甲醇催化氧化生成HCHO,最后乙二醇与甲醛反应生成菁
。(5)乙烯与溴发生加成反应生成BrCH2CH2Br,再水解生成乙二醇,甲醇催化氧化生成HCHO,最后乙二醇与甲醛反应生成菁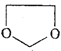 ,合成路线流程图为
,合成路线流程图为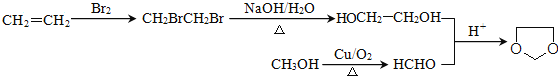 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某学习小组分析实验室制氯气的方法后认为:MnO2与FeCl3·6H2O共热能产生Cl2,于是设计了下列装置验证该结论。
【查阅资料】FeCl3·6H2O是棕黄色晶体,熔点37℃,沸点280~285℃。
【实验设计】
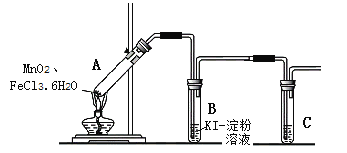
若结论成立,B中发生反应的化学方程式是___,C中的试剂是___。
【实验过程】
操作 | 现象 |
(1)经检查,装置气密性良好。 (2)添加药品,连接装置。 (3)点燃酒精灯。 | i.A中部分固体熔化,上方出现白雾; ii.稍后,产生黄色气体,管壁附着黄色液滴; iii.B中溶液变蓝。 |
【实验分析】
(1)小组讨论一致认为现象i中的白雾是盐酸小液滴,产生白雾的原因是___。
(2)分析现象ii时发生了分歧,有同学认为:FeCl3·6H2O是棕黄色,沸点不高,黄色气体重含有FeCl3也会导致B中溶液变蓝,反应的离子方程式是___。
小组同学通过下列实验证明现象ii的黄色气体中含有Fe3+,将下列实验补充完整:
a.只在A中加入FeCl3·6H2O,加热,开始产生白雾,稍后出现黄色气体,管壁仍有黄色液滴。
b.____________________________________ ,溶液变红。
(3)为进一步确认黄色气体含有 Cl2,小组在A、B 间增加盛有饱和氯化钠溶液的试管,气体依次通过饱和氯化钠溶液、KI淀粉溶液后,KI淀粉溶液变蓝,证实黄色气体中含有Cl2。饱和氯化钠溶液的主要作用是___。
(4)A中固体充分加热后得到Fe2O3和MnCl2,若物质的量之比为1:1,则A中总反应的化学方程式是________。从混合物中分离出Fe2O3的方法是:___。
【安全预案】在实验过程中,若试管B中溶液已经开始发生倒吸,应立即采取的一种措施是___ (填写编号)。
a.移去酒精灯
b.取下B中盛有溶液的试管
c.将A、B间的导管从乳胶管中取出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2和CH4是两种温室气体,研究它们具有重要的意义。
(1)已知CH4、H2和CO的燃烧热(△H)分别为-890.3 kJ· mol-1、-285.8 kJ· mol-1和-283.0 kJ·mol-1。则![]()
![]() △H=_________kJ·mol-1
△H=_________kJ·mol-1
(2)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示为: ![]()
![]() △H=-86.98 kJ·mol-1
△H=-86.98 kJ·mol-1
反应中影响CO2平衡转化率的因素很多,右图为某特定条件下,不同水碳比[n(H2O/n(CO2)]和温度对CO2平衡转化率的影响曲线。

①为提高CO2的平衡转化率,生产中除控制温度外还可以采取的措施有___________________、____________________。
②当温度高于190℃后,CO2平衡转化率出现如图所示的变化趋势,其原因是_______________。
(3)向1.0 L密闭容器中通入0.2 mol NH3(g)和0.1 mol CO2(g),在一定温度下发生反应则![]()
![]() ,反应时间与气体总压强(p)的数据如下表:
,反应时间与气体总压强(p)的数据如下表:
![]() 用起始压强和总压强计算平衡时NH3的转化率为_________,0~80 min内CO2的平均反应速率是__________。
用起始压强和总压强计算平衡时NH3的转化率为_________,0~80 min内CO2的平均反应速率是__________。
(4)氨基甲酸铵(NH2COONH4)极易水解成碳酸铵,在酸性条件水解更彻底。将氨基甲酸铵粉末逐渐加入到1 L 0.1 mol·L-1的盐酸中直到pH=7(室温下,忽略溶液体积变化),共用去0.052 mol氨基甲酸铵,溶液中几乎不含碳元素。此时溶液中c(NH4+)=__________,NH4+水解平衡常数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A. lmol苯乙烯中含碳碳双键数为4NA
B. 28g聚乙烯中含有的碳原子数目为2NA
C. 5.6g乙烯和环丁烷(C4H8)的混合气体完全燃烧需O2为1.2NA
D. 标准状况下,11.2L甲醇中含有的分子数目为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度和压强下,2体积AB2气体和1体积B2气体恰好化合成2体积的C气体,则C的化学式可能为
A.AB2 B. AB3 C.A3B D.A2B3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I:一定条件下,在体积为3 L的密闭容器中化学反应CO(g)+2H2(g)![]() CH3OH(g)达到平衡状态。
CH3OH(g)达到平衡状态。
(1)该反应的平衡常数表达式K=__________;根据下图,升高温度,K值将__________(填“增大”、“减小”或“不变”)。
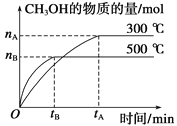
(2)500 ℃时,从反应开始到达到化学平衡,以H2的浓度变化表示的化学反应速率是______________(用nB,tB表示)。
(3)判断该可逆反应达到化学平衡状态的标志是______(填字母)。
a.v生成(CH3OH)=v消耗(CO)
b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变
d.CO、H2、CH3OH的浓度均不再变化
(4)300 ℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是________(填字母)。
a.c(H2)减小 b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加 d.重新平衡时c(H2)/c(CH3OH)减小
II:现有可逆反应.2NO2(g) ![]() N2O4(g),△H<0,试根据下列图象判断t2、t3、t4时刻采取的措施。
N2O4(g),△H<0,试根据下列图象判断t2、t3、t4时刻采取的措施。
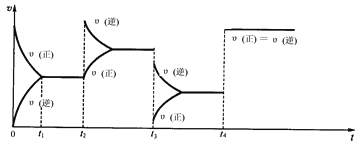
(1)t2:_________________________________________________;
(2)t3:_________________________________________________;
(3)t4:_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国早期研制的PEM低压电解臭氧发生器的结构如图。在电解槽里,最中间的是固体电解质聚合膜,膜两边分别是多孔的阳极和多孔的阴极,纯水从两边进人阳极水箱和阴极水箱。下列说法不正确的是
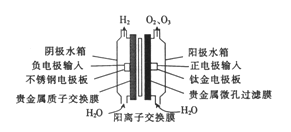
A. 在阳极室发生的反应有2H2O-4e-=4H++O2↑、3H2O-6e-=6H++O3↑
B. 通电时,H+向阴极室移动
C. 相同条件下O2与O3的体积之和小于H2的体积
D. 若用食盐水代替纯水,则对产物成分没有影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】120℃时,2体积某烃和8体积O2混合,完全燃烧后恢复到原来的温度和压强,体积不变,该分子式中所含的碳原子数不可能是( )
A. 1 B. 2 C. 3 D. 5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com