
A题适合使用二期课改新教材的考生解答,B题适合使用一期课改教材的考生解答。
23.(A)现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | M层上有2对成对电子 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
(1)元素T的原子最外层共有 种不同运动状态的电子。元素X的一种同位素可测定文物年代,这种同位素的符号是
(2)元素Y与氢元素形成一种离子![]() ,写出该微粒的电子式 (用元素符号表示)
,写出该微粒的电子式 (用元素符号表示)
(3)元素Z与元素T相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是
a 常温下Z的单质和T的单质状态不同 b Z的氢化物比T的氢化物稳定
c 一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是 ,理由是 。
(B)现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
X | L层p电子数比s电子数多2个 |
Y | 第三周期元素的简单离子中半径最小 |
Z | L层有三个未成对电子 |
(1)写出元素X的离子结构示意图 。
写出元素Z的气态氢化物的电子式 (用元素符号表示)
(2)写出Y元素最高价氧化物的水化物的电离方程式
(3)元素T与氯元素相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是
a 常温下氯气的颜色比T单质的颜色深
b T的单质通入氯化钠水溶液不能置换出氯气
c 氯与T形成的化合物中氯元素呈正价态
(4)探寻物质的性质差异性是学习的重要方法之—。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是 ,理由 。
(A)(1)6 ![]()
(2)![]()
(3)Cl b
(4)H2CO3 弱酸性或非氧化性酸
(B)(1)![]()
![]()
(2)H++![]() +H2O
+H2O![]() Al(OH)3
Al(OH)3![]() A13++3OH-
A13++3OH-
(3)F c
(4)Al 具有金属性
(A)解析:本题考查原子结构及元素的性质。由题意T原子电子排布式为1s22s22p63s23p4最外层上有6种不同运动状态电子,T为硫。X为C,测定文物年代同位素为![]() 。Y为N元素,铵离子电子式为
。Y为N元素,铵离子电子式为![]() 。Z是ⅦA元素,短周期元素,因为氟无+7价,故Z为氯。能证明氯的非金属性强的事实,有与氢气化合难易、气态氢化物的稳定性、最高氧化物对应水化物酸性、非金属间置换反应,故B正确。T、X、Y、Z四种元素的最高价氧化物水化物分别为H2SO4、H2CO3、HNO3、HClO4,只有H2CO3是弱酸。
。Z是ⅦA元素,短周期元素,因为氟无+7价,故Z为氯。能证明氯的非金属性强的事实,有与氢气化合难易、气态氢化物的稳定性、最高氧化物对应水化物酸性、非金属间置换反应,故B正确。T、X、Y、Z四种元素的最高价氧化物水化物分别为H2SO4、H2CO3、HNO3、HClO4,只有H2CO3是弱酸。
(B)解析:本题考查原子结构及元素性质。由题意可知T、X、Y、Z分别是F、O、Al、N四种元素。X的离子结构示意图为O2-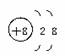 ,氨的电子式为
,氨的电子式为![]() ∶H,Al(OH)3是两性氢氧化物,既存在酸式电离,又存在碱式电离:H++AlO
∶H,Al(OH)3是两性氢氧化物,既存在酸式电离,又存在碱式电离:H++AlO![]() +H2O
+H2O![]() Al(OH)3
Al(OH)3![]() Al3++3OH-。氟的非金属性大于氯,比较F、Cl非金属性a、b不可以,a不能由颜色来判定,b中F2与氯化钠溶液中水反应:2F2+2H2O===4HF+O2,c中Cl呈正价说明氟的非金属性强。F、O、N是非金属,Al是金属。
Al3++3OH-。氟的非金属性大于氯,比较F、Cl非金属性a、b不可以,a不能由颜色来判定,b中F2与氯化钠溶液中水反应:2F2+2H2O===4HF+O2,c中Cl呈正价说明氟的非金属性强。F、O、N是非金属,Al是金属。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:阅读理解
考生注意:此题为分叉题,分A、B两题,考生可任选一题。若两题均做,一律按A题计分。A题适合使用二期课改新教材的考生解答,B题适合使用一期课改教材的考生解答。
(A)四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
| 元素 | A | B | C | D. |
| 性质或结构信息 | 室温下单质呈粉末状固体,加热易熔化。 单质在氧气中燃烧,发出明亮的蓝紫色火焰。 | 单质常温、常压下是气体,能溶于水。 原子的M层上有1个未成对的p电子。 | 单质质软、银白色固体、导电性强。 单质在空气中燃烧发出黄色的火焰。 | 原子最外电子层上s电子数等于p电子数 单质为空间网状晶体,具有很高的熔、沸点。 |
(1)B元素在周期表中的位置是____________,写出A原子的电子排布式____________。
(2)写出C单质与水反应的化学方程式_____________________。A与C形成的化合物溶于水后,溶液的pH____________7(填“大于”“等于”或“小于”)。
(3)D元素最高价氧化物晶体的硬度__________(填“大”或“小”),其理由是____________________________________________________________________。
(4)A、B两元素非金属性较强的是(写元素符号)______________。写出能证明这一结论的一个实验事实________________________________________________________________。
(B)元素A―D是元素周期表中短周期的四种元素,请根据表中信息回答下列问题。
| 元素 | A | B | C | D |
| 性质或结构信息 | 单质制成的高压灯,发出的黄光透雾力强、射程远 | 工业上通过分离液态空气获得其单质。原子的最外层未达到稳定结构。 | 单质常温、常压下是气体,原子的L层有一个未成对的p电子 | +2价阳离子的核外电子排布与氖原子相同 |
(1)上表中与A属于同一周期的元素是___________,写出D离子的电子排布式___________。
(2)D和C形成的化合物属于_______________晶体。
写出C单质与水反应的化学方程式_____________________________________________。
(3)对元素B的单质或化合物描述正确的是_______________。
a.B元素的最高正价为+6
b.常温、常压下单质难溶于水
c.单质分子中含有18个电子
d.在一定条件下镁条能与单质B反应
(4)A和D两元素金属性较强的是___________(写元素符号)。写出能证明该结论的一个实验事实__________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
A题适合使用二期课改新教材的考生解答,B题适合使用一期课改教材的考生解答
26.(A)实验室模拟合成氨和氨催化氧化的流程如下:

已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
(1)从下图中选择制取气体的合适装置:

氮气 、氢气
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有 、 
(3)氨合成器出来经冷却的气体连续通人乙装置的水中吸收氨, (“会”或“不会”)发生倒吸,原因是: 。
(4)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是: ,锥形瓶中还可观察到的现象是: 。
(5)写出乙装置中氨氧化的化学方程式:
(6)反应结束后锥形瓶内的溶液中含有H+、OH-、 、 离子。
(B)某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾。其设计的实验过程为:

(1)铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于
上(用以下所给仪器的编号填入,下同),取用坩埚应使用 ,灼烧后的坩埚应放在 上,不能直接放在桌面上。
实验所用仪器:a 蒸发皿 b 石棉网 c 泥三角 d 表面皿 e 坩埚钳 f 试管夹
(2)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物,用以制取胆矾。灼烧后含有少量铜的可能原因是
a 灼烧过程中部分氧化铜被还原 b 灼烧不充分铜未被完全氧化
c 氧化铜在加热过程中分解生成铜 d 该条件下铜无法被氧气氧化
(3)通过途径Ⅱ实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、 、冷却结晶、 、自然干燥
(4)由粗制氧化铜通过两种途径制取胆矾,与途径Ⅰ相比,途径Ⅱ有明显的两个优点是: 、
(5)在测定所得胆矾(CuSO4·xH2O)中结晶水x值的实验过程中:称量操作至少进行 次
(6)若测定结果x值偏高,可能的原因是
a 加热温度过高 b 胆矾晶体的颗粒较大
c 加热后放在空气中冷却 d 胆矾晶体部分风化
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(A)四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
元素 | A | B | C | D. |
性质或结构信息 | 室温下单质呈粉末状固体,加热易熔化。 单质在氧气中燃烧,发出明亮的蓝紫色火焰。 | 单质常温、常压下是气体,能溶于水。 原子的M层上有1个未成对的p电子。 | 单质质软、银白色固体、导电性强。 单质在空气中燃烧发出黄色的火焰。 | 原子最外电子层上s电子数等于p电子数 单质为空间网状晶体,具有很高的熔、沸点。 |
(1)B元素在周期表中的位置是____________,写出A原子的电子排布式____________。
(2)写出C单质与水反应的化学方程式_____________________。A与C形成的化合物溶于水后,溶液的pH____________7(填“大于”“等于”或“小于”)。
(3)D元素最高价氧化物晶体的硬度__________(填“大”或“小”),其理由是____________________________________________________________________。
(4)A、B两元素非金属性较强的是(写元素符号)______________。写出能证明这一结论的一个实验事实________________________________________________________________。
(B)元素A—D是元素周期表中短周期的四种元素,请根据表中信息回答下列问题。
元素 | A | B | C | D |
性质或结构信息 | 单质制成的高压灯,发出的黄光透雾力强、射程远 | 工业上通过分离液态空气获得其单质。原子的最外层未达到稳定结构。 | 单质常温、常压下是气体,原子的L层有一个未成对的p电子 | +2价阳离子的核外电子排布与氖原子相同 |
(1)上表中与A属于同一周期的元素是___________,写出D离子的电子排布式___________。
(2)D和C形成的化合物属于_______________晶体。
写出C单质与水反应的化学方程式_____________________________________________。
(3)对元素B的单质或化合物描述正确的是_______________。
a.B元素的最高正价为+6
b.常温、常压下单质难溶于水
c.单质分子中含有18个电子
d.在一定条件下镁条能与单质B反应
(4)A和D两元素金属性较强的是___________(写元素符号)。写出能证明该结论的一个实验事实_____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2007年普通高等学校招生全国统一考试(上海卷)化学试题 题型:填空题
考生注意:下题为分叉题,分A、B两题,考生可任选一题。若两题均做,一律按A题计分。A题适合使用二期课改新教材的考生解答,B题适合使用一期课改教材的考生解答。
(A)现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| T | M层上有2对成对电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com