
【题目】科学家在利用无土栽培培养一些名贵花卉时,培养液中添加了多种元素。其配方如下,其中植物吸收量最少的离子是
离子 | K+ | Na+ | Mg2+ | Ca2+ | NO3 | H2PO4- | SO42- | Zn2+ |
培养液浓度(mol/L) | 1 | 1 | 0.35 | 1 | 2 | 1 | 0.25 | 1 |
A.Ca2+ B.SO42- C.Zn2+ D.H2PO4
科目:高中化学 来源: 题型:
【题目】废旧光盘金属层中的少量Ag,某科研小组采用如下方案进行回收(金属层中其他金属含量过低,对实验的影响可忽略)。
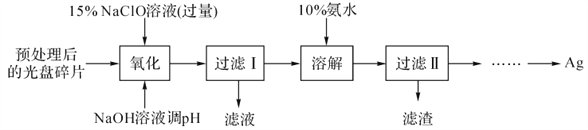
已知:①NaClO溶液在受热或酸性条件下易分解,如:3NaClO =2NaCl+NaClO3
②AgCl可溶于氨水:AgCl+2NH3·H2O =Ag(NH3)2++Cl-+2H2O
③常温时N2H4·H2O(水合肼)能还原Ag(NH3)2+:
4 Ag(NH3)2++N2H4·H2O=4Ag↓+N2↑+4NH4++4NH3↑+H2O
(1)“氧化”阶段需在80℃条件下进行,适宜的加热方式为___________。
(2)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为___________。HNO3也能氧化Ag,从反应产物的角度分析,以HNO3代替NaClO的缺点是________________。
(3)为提高Ag的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并________________。
(4)从“过滤Ⅱ”后的滤液中获取单质Ag的过程中,在加入2 mol/L水合肼溶液后,后续还需选用的试剂有________________(①1 mol/LH2SO4、②10%氨水、③1 mol/LNaOH溶液,填序号)。反应完全后获取纯净的单质银再进行的实验操作过程简述为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,几种弱酸的电离平衡常数如下表所示,下列说法正确的是
化学式 | HCOOH | H2CO3 | HCN |
电离平衡常数 | K=1.8×10-4 | K1=4.3×10-7 K2=5.6×10-11 | K=4.9×10-10 |
A. 酸性强弱顺序是HCOOH>HCN> H2CO3
B. HCOOH的电离平衡常数表达式为
C. Na2CO3溶液显碱性,NaHCO3溶液显酸性
D. H2CO3溶液和NaCN溶液反应的离子方程式为H2CO3+CN-=HCO3-+HCN
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题
(1)相同质量的CO和CO2的物质的量之比为 , 所含的电子个数之比为 , 在标准状况下的体积之比为 .
(2)19g某二价金属氯化物(ACl2)中含有0.4mol Cl﹣ , 则A的相对分子质量是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,向20mL0.1mol·L-1醋酸溶液中不断滴入0.1mol·L-1的NaOH溶液,溶液pH变化如图所示。下列叙述错误的是
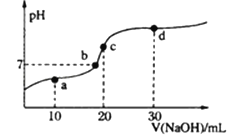
A. a点:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
B. b点:c(Na+)=c(CH3COOH)+c(CH3COO-)
C. c点:c(OH-)=c(CH3COOH)+c(H+)
D. d点:2c (Na+)=3[c(CH3COOH)+c(CH3COO-)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、X均为中学化学常见物质,相互转化关系如图所示(部分物质略去)。

I.若A为气体单质,气体B能使湿润红色石蕊试纸变蓝,E为红棕色气体。
(1)A中所含元素在周期表中的位置是__________________
(2)实验室制取B的化学方程式为_________________________________________
(3)D和CO均是汽车尾气的主要成分,通过汽车尾气催化转化装置生成无污染气体,降低污染物排放,写出该反应的化学方程式:_______________________________
II.若A是淡黄色固体,B中阴、阳离子均为10电子粒子,常温下X是无色气体。
(4)A与X反应的化学方程式:_______________________________________
(5)将一定量的气体X通入B的溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体与HCl物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。a点溶液中所含溶质的化学式为_________________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按照如图所示进行实验,下列有关说法不合理的是

A. 若X烧杯中溶液为饱和氯化铁溶液,则利用过滤的方法,从Z烧杯中可获得氢氧化铁胶体
B. 若X烧杯中溶液为新制的饱和氯水,则三只烧杯液体的漂白性:Y>X>Z
C. 若X烧杯中溶液为饱和氯化铁溶液,则X→Z过程的离子反应有:3CaCO3+ 2Fe3+ + 3H2O=2Fe(OH)3+3CO2↑+3Ca2+
D. 若X烧杯中溶液为新制的饱和氯水,则X→Z过程的离子反应有:2HClO+CO32-=CO2↑+O2↑+H2O+2Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“朴雪”乳酸亚铁口服液可以有效地治疗人类缺铁性贫血症,这是因为其中的 Fe2+进入人体后能
A. 调节血液的酸碱平衡
B. 调节血液的渗透压
C. 参与红细胞血红蛋白的形成
D. 促进更多红细胞的产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素在生物体内虽很少,却是维持正常生命活动不可缺少的,通过下面哪一实例可以说明()
A. Fe是血红蛋白的组成成分
B. 油菜缺少硼时会导致减产
C. 动物血液钙盐含量太低会抽搐
D. 缺Mg会影响叶绿素的合成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com