
����Ŀ������������ȡ�Ļ�ѧ����ʽ�У�������������ԭ��Ӧ����(����)
A.ʵ������ȡ������Zn��H2SO4=ZnSO4��H2��
B.ʵ������ȡ������̼��CaCO3��2HCl=CaCl2��H2O��CO2��
C.ʵ������ȡ������MnO2��4HCl(Ũ)![]() MnCl2��2H2O��Cl2��
MnCl2��2H2O��Cl2��
D.��ҵ����ȡ�������ȣ�2NaClO3��4HCl(Ũ)=2NaCl��2H2O��2ClO2����Cl2��
���𰸡�B
��������
��Ԫ�ػ��ϼ۱仯�ķ�Ӧ��Ϊ������ԭ��Ӧ����֮��������Ԫ�ػ��ϼ۱仯�ķ�Ӧ��Ϊ��������ԭ��Ӧ���ݴ˷������
A��Zn��H2SO4=ZnSO4��H2����Zn��HԪ�صĻ��ϼ۱仯��Ϊ������ԭ��Ӧ����A��ѡ��
B��CaCO3��2HCl=CaCl2��H2O��CO2����û��Ԫ�صĻ��ϼ۱仯��������������ԭ��Ӧ����Bѡ��
C��MnO2+4HCl(Ũ) ![]() MnCl2+Cl2��+2H2O����Ԫ�ء���Ԫ�ػ��ϼ۶������仯����������ԭ��Ӧ����C��ѡ��
MnCl2+Cl2��+2H2O����Ԫ�ء���Ԫ�ػ��ϼ۶������仯����������ԭ��Ӧ����C��ѡ��
D��2NaClO3��4HCl(Ũ)=2NaCl��2H2O��2ClO2����Cl2����Cl�Ļ��ϼ۱仯��Ϊ������ԭ��Ӧ����D��ѡ��
��ѡB��


 ����������ϵ�д�
����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4 L�ܱ������г���6 mol A�����5 mol B���壬��һ�������·�����Ӧ��3A(g)��B(g)![]() 2C(g)��xD(g)���ﵽƽ��ʱ��������2 mol C�����ⶨ��D��Ũ��Ϊ0.5 mol��L��1�������ж���ȷ����( )��
2C(g)��xD(g)���ﵽƽ��ʱ��������2 mol C�����ⶨ��D��Ũ��Ϊ0.5 mol��L��1�������ж���ȷ����( )��
A. x��1
B. B��ת����Ϊ20%
C. ƽ��ʱA��Ũ��Ϊ1.50 mol��L��1
D. �ﵽƽ��ʱ������ͬ�¶��������ڻ�������ѹǿ�Ƿ�Ӧǰ��85%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ������������Ӧʵ��������ǣ� ��
A.������þ����Һ�еμ��Ȼ����Һ�������ܽ⣺Mg(OH)2+2NH![]() =Mg2++2NH3��H2O
=Mg2++2NH3��H2O
B.��ˮ�еμӱ����Ȼ�����Һ�õ����ɫҺ�壺Fe3++3H2O=Fe(OH)3��+3H+
C.��ʳ������ϴˮ����CO![]() +2CH3COOH=2CH3COO-+H2O+CO2��
+2CH3COOH=2CH3COO-+H2O+CO2��
D.84����Һ��������ò����ж����壺ClO-+Cl-+2H+=Cl2��+OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС����ʵ��I��֤Fe2(SO4)3��Cu�ķ�Ӧ���۲쵽���쳣�����������������̽����
ʵ��I��
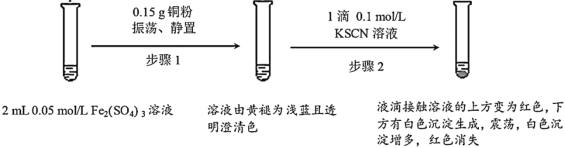
��1��Fe2(SO4)3��Һ�����³����Ե�ԭ����___��
��2��Fe2(SO4)3��KSCN��Һ��Ӧ�����ӷ���ʽΪ___��
��3��ʵ��ǰ��С��ͬѧԤ�⾭������2����Һ��Ӧ�ó��ֺ�ɫ��������__��
��4��ʵ��С���ɫ�����IJ�������������̽��
�������ϣ�i.CuSCNΪ������ˮ�İ�ɫ���塣
ii.SCN-����Ϊ��±�����ӣ�������±����������
����ʵ��ⶨ��ɫ����ΪCuSCN���������Ϻ�С��ͬѧ�²�CuSCN���������������ֿ���
�²�1��Cu2+��KSCN������������ԭ��Ӧ
�²�2���������ӽ��仹ԭCu2++Fe2+=Cu++Fe3+��Cu++SCN-=CuSCN��
Ϊ֤ʵ����С��ͬѧ����ʵ��II��III����FeSO4��CuSO4��ҺŨ��Ϊ0.1mol/L��KSCN��ҺŨ��Ϊ0.4mol/L��
ʵ����� | �Ա�ʵ�鼰�Լ� | ʵ�鲽�� | ʵ������ |
II |
| ����1mLKSCN��Һ | ��ʼʱ��Һ���Ϸ���Ϊ��ɫ��һ��ʱ����ɫ�������ӣ���������֧�Թ� |
| ����1mLKSCN��Һ | ��Һ�����ɫ |
�ٲ²�1�����ӷ���ʽ____��
��ʵ��II���Թ�__������ĸ���е��������֤ʵ�²�1��������
ʵ����� | �Ա�ʵ�鼰�Լ� | ʵ�鲽�� | ʵ������ |
| ����2mLCuSO4��Һ | ��Һ��Ϊ����ɫ | |
�ټ���1mLKSCN��Һ | ��Һ���ϲ��Ϊ��ɫ���а�ɫ����������һ��ʱ�����֧�Թ���Һ�ʺ�ɫ | ||
| ����4mLCuSO4��Һ | ��Һ��Ϊ����ɫ | |
�ټ���1mLKSCN��Һ | ��Һ���ϲ��Ϊ��ɫ���а�ɫ����������һ��ʱ�����֧�Թ���Һ��dz��ɫ | ||
| ����2mLCuSO4��Һ | ��Һ��Ϊ����ɫ | |
�ټ���1mLKSCN��Һ | ��Һ���ϲ��Ϊ��ɫ���а�ɫ����������һ��ʱ�����֧�Թ���Һ�����ɫ |
��5��Fe3+�������Ա�Ӧǿ��Cu2+�����ʵ��III�е��������Cu2++Fe2+=Cu++Fe3+����������ԭ����___��
��6��ʵ��С��������ϲ����ۺ�ó�����Һ�������ڷ�Ӧʱ�����ֵ�������ǿ������Ӧ��ԭ����ļ�̬��״̬�йء��ɴ˷�������CuSCN����ʹCu2+����������ǿ��������ʵ���һ��֤���������ʵ����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾ�IJ������裬�����������������ķ�Ӧ��ʵ�顣
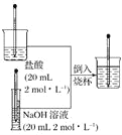
�ش��������⣺
(1)��Ӧ������Һ���¶��뷴Ӧǰ���������������Һ���¶���Ƚ���仯��___________________________________��
(2)����Ϊ����кͷ�Ӧ�Ƿ��ȷ�Ӧ�������ȷ�Ӧ____________________________________��
(3)д���÷�Ӧ�����ӷ���ʽ��____________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W����������������Ķ���������Ԫ�أ������γɵ�ij�ֻ�����Q�Ľṹʽ��ͼ��ʾ��X��W�γɵĻ�����M��������Һ�塣����˵����ȷ����
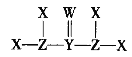
A.X��Z���γ�������������������ͬ��ZX3��![]()
B.M���ȶ���ǿ�Ҿ�����������
C.Q�����и�ԭ��������Ӳ���ﵽ�ȶ��ṹ
D.X��Y��Z��W����Ԫ�ؼ�ֻ���γɹ��ۻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��2012���ذ��˻�����ñ���Ϊȼ�ϡ�������ֵ�ϸߣ���Ⱦ��С����һ��������ȼ�ϡ��Իش��������⣺

����ͼ��һ����������ȫȼ������CO2��1 mol H2O(l)�����е������仯ͼ������ͼ�е����������롰����������
��д����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ��___________________________________��
��������(CH3OCH3)��һ������ȼ�ϣ�Ӧ��ǰ��������1 mol��������ȫȼ������CO2��Һ̬ˮ�ų�1 455 kJ��������1 mol����Ͷ����ѵĻ��������ȫȼ������CO2��Һ̬ˮ���ų�1 645 kJ���������������У�����Ͷ����ѵ����ʵ���֮��Ϊ________��
��2����˹������Ϊ�����ܻ�ѧ������һ����ɻ�ּ�����ɣ��������̵�����ЧӦ��ͬ�������ø�˹���ɻش��������⣺
����֪��H2O(g)=H2O(l)����H1����Q1 kJ/mol C2H5OH(g)=C2H5OH(l)����H����Q2 kJ/mol
C2H5OH(g)��3O2(g)=2CO2(g)��3H2O(g)����H3����Q3 kJ/mol
��ʹ46 gҺ̬��ˮ�ƾ���ȫȼ�գ����ָ������£������������зų�������Ϊ________kJ��
��̼(s)��������Ӧ������ʱ������COͬʱ����������CO2�������ͨ��ʵ��ֱ�Ӳ�÷�Ӧ�� C(s)��![]() O2(g)=CO(g)�Ħ�H���������ʵ�顢���ø�˹���ɼ�����÷�Ӧ�Ħ�H������ʱ��Ҫ��õ�ʵ��������________��
O2(g)=CO(g)�Ħ�H���������ʵ�顢���ø�˹���ɼ�����÷�Ӧ�Ħ�H������ʱ��Ҫ��õ�ʵ��������________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶���22% ��������Һ150 mL������100 gˮϡ�ͺ���������������Ϊ14%��
��1��ԭ��������Һ��������__________��
��2��ԭ��������Һ�����ʵ���Ũ����____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������1mol��ѧ�������γ���̬ԭ������Ҫ��������![]() ��ʾ����ϱ�����Ϣ�ж�����˵������ȷ����( )
��ʾ����ϱ�����Ϣ�ж�����˵������ȷ����( )
���ۼ� | H-H | F-F | H-F | H-Cl | H-I |
E(kJ/mol) | 436 | 157 | 568 | 432 | 298 |
A. 432kJ/mol>E(H-Br)>298kJ/mol B. �������ȶ��Ĺ��ۼ���H-F��
C. H2(g)��2H(g) ��H=+436kJ/mol D. H2(g)+F2(g)=2HF(g) ��H=-25kJ/mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com