
����Ŀ�������仯����֮����ת��������ʽ��ʾ��
![]()
�ش������й����⣺
��1����Ԫ�������ڱ��е�λ����_____________��
��2��Fe�����ϡ���ᷴӦ������ȡFeSO4�����÷�Ӧ���õ�������Һ��ʵ����������ת����Ҫ����﴿������ѡ�õ��Լ���__________--��ѡ����ţ���
A��Cl2B��FeC��HNO3D��H2O2
��3������ת���õ��������������ڵ绯������ͭ���գ����������������ķ�Ӧ�Ƚϸ��ӣ�������һ��Ҫ��ӦCuFeS2+4Fe3+=Cu2++5Fe2++2S��CuFeS2��SΪ-2�ۣ�������˵����ȷ����_____��ѡ����ţ���
A�������ʷ���ĽǶȿ�����ͭ�����ںϽ�
B����Ӧ�У�������Ԫ�ؾ�����ԭ
C����Ӧ�У�CuFeS2����������������ԭ��
D����ת��1mol����ʱ��46gCuFeS2�μӷ�Ӧ
��4��������Ӧ�У���FeSO4��O2��ϵ����Ϊ2��1������ƽ���з���ʽ��_______FeSO4+_______K2O2��_______K2FeO4+_______K2O+ _______K2SO4+_______O2��
_____________
��5��ijͬѧ������ˮ�������·�Ӧ��Ĺ��������ܽ��ڹ��������У�����ж�������Һ���Ƿ���Fe3+�� _____________________________________
��6����4 mol HNO3��ϡ��Һ�������������������������ɵ�����ֻ��һ�֣���������ϵ�л���n(Fe2+)��n(Fe)�仯��ʾ��ͼ������;�б�����������ֵ��______________

���𰸡� ��������VIII�� D D 2 6 2 2 2 1 ȡ������Һ�����Թ��У��μ�����KSCN��Һ������Һ��ΪѪ��ɫ������Fe3+ 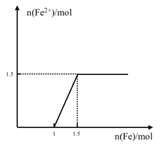
����������1������26��Ԫ�أ������ڱ���λ�ڵ�������VIII����
��2������Ҫʵ��Fe2������Fe3����ת��������Ӧ���������������ų�B�������Cl2������FeCl3������HNO3������Fe(NO3)3���ֱ�����Cl����NO3�����ʣ����ų�A��C����H2O2��������ʱ�����ɵĻ�ԭ������H2O�������������ʣ���ѡD��
��3����A��Ͻ���ָ�����ֻ��������ϵĽ������������ǽ�������һ���������ϳɵľ��н������Ե����ʣ����Ի�ͭ���ǺϽ𣬹�A����B�������������Ԫ����Fe3������CuFeS2����Ԫ�صĻ��ϼ��ǣ�2�ۣ�����CuFeS2����Ԫ�صĻ��ϼ����ߣ�����ԭ�����������ʲ���������������ԭ�����B����C��������з���ʽ��֪��CuFeS2������+2�۱��+3�������-2�۱��0�ۣ����CuFeS2����Ԫ�غ���Ԫ�صĻ��ϼ۾����ߣ���CuFeS2ֻ����ԭ�������C����D����ݷ�Ӧ����ʽ��֪������1molCuFeS2��Ӧʱ��ת�Ƶ�������4mol�����Ե�ת��1mol����ʱ���μӷ�Ӧ��CuFeS2���ʵ�����0.25mol��m��CuFeS2��=0.25mol��184g/mol=46g������D��ȷ�������ѡD��
��4����FeSO4��Fe�Ļ��ϼ��ǣ�2�ۣ�K2FeO4��Fe�Ļ��ϼ��ǣ�6�ۣ�����һ��FeSO4ʧȥ4�����ӣ�K2O2��O�Ļ��ϼ��ǣ�1�ۣ�O2��O�Ļ��ϼ���0�ۣ�������һ��O2ʱ��K2O2ʧȥ2�����ӣ�K2O2��O�Ļ��ϼ��ǣ�1�ۣ�K2FeO4��K2O��O�Ļ��ϼ��ǣ�2�ۣ�����һ��K2O2���ɣ�2��Oʱ���õ�������Ϊ2�������Ը÷���ʽ�е�ʧ���ӵ���С������Ϊ6����˸÷���ʽ�ļ������ֱ�Ϊ��2��6��2��2��2��1��������ʽ�ǣ�2FeSO4��6K2O2=2K2FeO4��2K2O��2K2SO4+ O2������˴���2 6 2 2 2 1��
��5����������Һ���Ƿ���Fe3+������ͨ������KSCN��Һ���м���������Һ��ΪѪ��ɫ������Fe3+������Fe3+��
��6������ϡ������Һ��������������������ʼʱ��������������Fe��4HNO3=Fe(NO3)3��NO����2H2O�����ݷ���ʽ��֪��������1mol����ʱ��4mol HNO3ǡ����ȫ��Ӧ������1mol Fe3�����ټ������ۣ�����Fe��2Fe3��=3Fe2������ʱ��ʼ����Fe2�������ݷ���ʽ��֪��������0.5mol����ʱ����������Һ�е�1mol Fe3����ȫ��Ӧ������1.5mol��Fe2��������n(Fe2+)��n(Fe)�仯��ʾ��ͼΪ��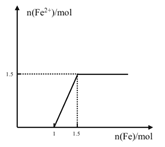


 �ִʾ��ƪϵ�д�
�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��M��W��ԭ��������С�������е����ֶ���������Ԫ�أ�����X��Z��M��W����Ԫ�ص�ԭ������֮��Ϊ32����Ԫ�����ڱ���X��ԭ�Ӱ뾶��С��Ԫ�أ�Yԭ�ӵ�����������������Ӳ�����2����Z��M�������ڣ�M��Wλ��ͬ���塣�ش��������⣺
(1)Y�����ڱ��е�λ����________, W�������ӷ�����_____��
(2) Z�ĵ��ʵĽṹʽΪ________����״���£��Թ����ռ���Z�ļ��⻯�������ˮ�У��������ʲ����Թ�����ɢ����һ��ʱ����Թ�����Һ�����ʵ����ʵ���Ũ��Ϊ_______��
(3����X��Z��M����Ԫ����ɵĻ��������ᡢ��εĻ�ѧʽ�ֱ�Ϊ________������һ������
(4��д������ʱY�ĵ�����W������������ˮ�����Ũ��Һ������Ӧ�Ļ�ѧ����ʽ��____________��
(5�����������X��Z��M��W��Fe����Ԫ����ɣ���Ħ������Ϊ392g��mol-1, 1 mol���к���6 mol�ᾧˮ���Ի������������ʵ�飺
a��ȡ��ˮ��Һ���������������ŨNaOH��Һ�����ȣ�������ɫ��״��������ɫ���д̼�����ζ�����壻��ɫ��״����Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ��
b����ȡ��ˮ��Һ���������������BaCl2��Һ��������ɫ�������ټ����ᣬ��ɫ�������ܽ⡣
�� �Ļ�ѧʽΪ________��
�� ��֪100 mL 1 mol��L-1�ļ���Һ����20 mL 1 mol��L-1������KMnO4��Һǡ�÷�Ӧ��д����Ӧ�����ӷ���ʽ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ��NO3�������ʵ���Ũ��������(����)
A. 500 mL 1 mol��L��1��KNO3��Һ
B. 500 mL 1 mol��L��1��Ba(NO3)2��Һ
C. 1000 mL 0.5 mol��L��1��Mg(NO3)2��Һ
D. 1000 mL 0.5 mol��L��1��Fe(NO3)3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ʯ�͵�˵����ȷ���ǣ� ��
A.ʯ����ú̿����Ȼ���������ܶ��ǻ�ʯ��Դ
B.ʯ����Ҫ����̼��������Ԫ��
C.ʯ�����ڿ�����������Դ
D.ʯ�ͷ���ĸ���־��Ǵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1 molij��̬����2 mol Cl2�����ӳɷ�Ӧʱ�������еIJ�����̼ԭ��ȫ��ת��Ϊ����̼ԭ�ӣ����ò�������2 mol Cl2����ȡ����Ӧ������ֻ��C��Cl����Ԫ�صĻ���������̬����(����)
A. ��ϩ B. ��Ȳ C. ��ϩ D. ��Ȳ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������±�����зе���͡��ܶ���С���ǣ� ��
A. CH3CH2CHCl2 B. CH3CH (Cl )CH3 C. CH3CH2CH2Br D. CH3CH (Br)CH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[Cu(NH3)4]SO4��H2O��һ��ɱ�����Ԫ��N��O��S�ĵ�һ�������ɴ�С���е�˳��Ϊ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��25 ����101 kPa�£�0.5 mol����C8H8ȼ�����ɶ�����̼��Һ̬ˮʱ�ų�2 759 kJ��������ʾ������Ӧ���Ȼ�ѧ����ʽ��ȷ����(����)
A. C8H18(l)��![]() O2(g)===8CO2(g)��9H2O(g) ��H����48.40 kJ��mol��1
O2(g)===8CO2(g)��9H2O(g) ��H����48.40 kJ��mol��1
B. C8H18(l)��![]() O2(g)===8CO2(g)��9H2O(l) ��H����5 518 kJ��mol��1
O2(g)===8CO2(g)��9H2O(l) ��H����5 518 kJ��mol��1
C. C8H18(l)��![]() O2(g)===8CO2(g)��9H2O(l) ��H����5 518 kJ��mol��1
O2(g)===8CO2(g)��9H2O(l) ��H����5 518 kJ��mol��1
D. 2C8H18(l)��25O2(g)===16CO2(g)��18H2O(l) ��H����11 036 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2011�꣬ijý�屨������Ƥ�������¼����������̽�Ƥ���½���ˮ�������̷�������̷��������ʵĺ���������˵������ȷ����
A������Ƥ�����Ҫ�ɷ��ǵ�����
B����Ȼ������ˮ������ղ���������������
C��Ƥ�����ƹ�����ʹ�õ�K2Cr2O7��ʹ����������
D����Ƥ����������ʱ���ս���ë����ζ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com