
 ij����С�������ʳ��ˮ��̽��ʵ�飬������ͼ��ʾ����ʵ��װ�ã��������ѡ���ʵ���װ�ò�������װ��Ҫ����������������ԣ����ⶨ���������������
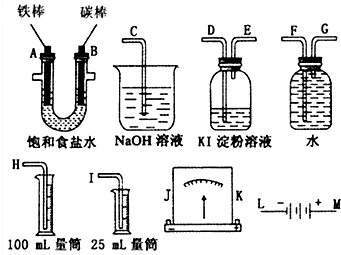
ij����С�������ʳ��ˮ��̽��ʵ�飬������ͼ��ʾ����ʵ��װ�ã��������ѡ���ʵ���װ�ò�������װ��Ҫ����������������ԣ����ⶨ������������������� ��1����ⱥ��ʳ��ˮ��������������ʧ���ӣ�����Ե缫��������������̼��Ϊ������������������FeΪ�������븺�������������������ӵõ��ӣ�
��2��B���������������������������ԣ���Ҫβ��������
��3��A����������������ˮ�����������������
��4����Դ�����ӵ��ص�������̼���ӵ����ơ�-���ˣ���+���˽ӵ�Դ������
��5�������������������ƵĹ�ϵ�Ǽ����������Ƶ����ʵ������ٸ���c=$\frac{n}{V}$������������Ũ�ȣ��ٽ�����ӻ���������������Ũ�ȣ��Ӷ��ó���Һ��pH���ڵ���ǿ��ΪI A��ͨ��ʱ��Ϊt min�������Һ��ת�Ƶĵ��ӵ����ʵ��������ݵ���غ���ʽ���㣮
��� �⣺��1����ⱥ��ʳ��ˮ��������������ʧ���ӣ�����Ե缫����������������̼��Ϊ�����������ĵ缫��ӦΪ��2Cl--2e-=Cl2����FeΪ�������븺�������������������ӵõ��ӣ������ĵ缫��ӦΪ��2H++2e-�TH2����
�ʴ�Ϊ������M��2Cl--2e-=Cl2��������L��2H++2e-�TH2����
��2��B���������������������������ԣ�Ӧͨ��KI������Һ��������ɫ��˵��������KI����Ϊ���ʵ⣬�������������ԣ������ж���Ҫβ��������������������Һ���ն������������������װ�õ�˳����B��D��E��C��
�ʴ�Ϊ��B��D��E��C�����������������ԣ���ȥʣ�����������ֹ��Ⱦ������
��3��A����������������ˮ������������������������������Ϊ16.8mL��Ϊ�˼�����ѡ��25mL����Ͳ��������װ�õ�˳����A��G��F��I��
�ʴ�Ϊ��A��G��F��I��ȷ�����������������������
��4����Դ�����ӵ��ص�������̼���ӵ����ơ�-���ˣ���+���˽ӵ�Դ����������������˳���ǣ�L��A��B��J��K��M��
�ʴ�Ϊ��A��B��J��K��
��5������2NaCl+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2NaOH+H2��+Cl2�����������ƺ������Ĺ�ϵʽ֪��n��NaOH��=$\frac{0.0168L}{22.4L/mol}$��2=0.0015mol����c��OH-��=$\frac{0.0015mol}{0.05L}$=0.03mol/L��
c��H+��=$\frac{1{0}^{-14}}{0.03}$=$\frac{1}{3}$��10-12 mol/L��pH=12.41��
�ڵ���ǿ��ΪI A��ͨ��ʱ��Ϊt min����60ts����Һ�����ɵ���������Ϊ0.0015mol����ת�Ƶĵ���Ϊ0.0015mol��
���ݵ���غ�õ���I•60t=NA��0.0015��1.6��10-19����NA=2.5��1021It��
�𣺴�ʱ��Һ��pHΪ12.41�������ӵ������ı���ʽΪ2.5��1021It��
���� �����Ե��ԭ��Ϊ���忼�����������ȡ�����ʵļ����֪ʶ�㣬���ݵ��ԭ�������ʵ����ʡ����ʼ�Ĺ�ϵ����������ɣ��ѵ�����������˳����������ȡװ�á�����װ�á��ռ�װ�á�β������װ�������ɣ��Ѷ��еȣ�


 Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д�
Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
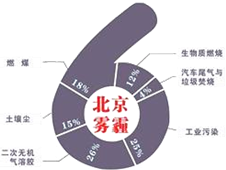 �п�Ժ�����о����о�Ա���ʽ���������ͬ�к������Ա�������PM2.5��6����Ҫ��Դ�����У�����β����ȼú�ֱ�ռ4%��18%�����ھ�������β���ķ�ӦΪ2NO��g��+2CO��g��$\stackrel{����}{?}$ 2CO2��g��+N2��g������֪�÷�Ӧ��570Kʱƽ�ⳣ��Ϊ1��1059������Ӧ����������˵����ȷ���ǣ�������
�п�Ժ�����о����о�Ա���ʽ���������ͬ�к������Ա�������PM2.5��6����Ҫ��Դ�����У�����β����ȼú�ֱ�ռ4%��18%�����ھ�������β���ķ�ӦΪ2NO��g��+2CO��g��$\stackrel{����}{?}$ 2CO2��g��+N2��g������֪�÷�Ӧ��570Kʱƽ�ⳣ��Ϊ1��1059������Ӧ����������˵����ȷ���ǣ�������| A�� | װ��β������װ�õ������ų��������в��ٺ���NO��CO | |
| B�� | ���β������Ч�ʵij��÷����������¶� | |
| C�� | ����ѹǿ������ƽ�����ƣ���ʵ�ʲ����п�ͨ����ѹ�ķ�ʽ����侻��Ч�� | |
| D�� | ���β������Ч�ʵ����;����ʹ�ø�Ч���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�����Һ�ڵ��������µ���������Ӻ������ӣ� | |
| B�� | ���ᱵ������ˮ�������ᱵ�ǵ���� | |
| C�� | ����ˮ�����������ӵĻ����ﶼ���� | |
| D�� | ������̼��ˮ��Һ�ܵ��磬�ʶ�����̼���ڵ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
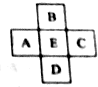 ԭ������Ϊx��Ԫ��E�����ڱ���λ��A��B��C��D����Ԫ���м䣨��ͼ��ʾ������A��B��C��D����Ԫ�ص�ԭ������֮�Ͳ������ǣ���ϵ���ϵ��O��Ԫ�س��⣩��������
ԭ������Ϊx��Ԫ��E�����ڱ���λ��A��B��C��D����Ԫ���м䣨��ͼ��ʾ������A��B��C��D����Ԫ�ص�ԭ������֮�Ͳ������ǣ���ϵ���ϵ��O��Ԫ�س��⣩��������| A�� | 4x | B�� | 4x+6 | C�� | 4x+10 | D�� | 4x+14 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
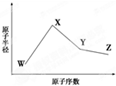 W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯����ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ18��������Ϊ10��X��Neԭ�ӵĺ�����������1��Y�ĵ�����һ�ֳ����İ뵼����ϣ�Z�ĵ縺����ͬ��������Ԫ�������
W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯����ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ18��������Ϊ10��X��Neԭ�ӵĺ�����������1��Y�ĵ�����һ�ֳ����İ뵼����ϣ�Z�ĵ縺����ͬ��������Ԫ�������| ��ѧ�� | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| ����/ kJ•mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �����Ļ�ѧ�����ڹ��ۼ����������Ӽ����ۼ��Ļ�����Ļ�ѧʽΪNa2O2��
�����Ļ�ѧ�����ڹ��ۼ����������Ӽ����ۼ��Ļ�����Ļ�ѧʽΪNa2O2��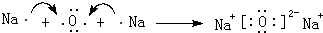 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����Ԫ���������о�Ԫ�ؼ��仯��������ʾ�����Ҫ���壮
����Ԫ���������о�Ԫ�ؼ��仯��������ʾ�����Ҫ���壮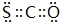 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʡ����ۡ���ά�ء������ǵȶ�����������ˮ�Ⲣ�ṩ���� | |
| B�� | ���������ϩ�Ļ������ͨ��ʢ����ˮ��ϴ��ƿ�������ᴿ���� | |
| C�� | C2H6����������ȡ����Ӧ��C2H4��HCl�����ӳɷ�Ӧ�����ɵõ�C2H5Cl | |
| D�� | ����ˮһ���Լ��Ϳɽ�����CCl4�����ᡢ�Ҵ����� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com