
 ,它的化学键属于共价键;含有离子键和共价键的化合物的化学式为Na2O2.
,它的化学键属于共价键;含有离子键和共价键的化合物的化学式为Na2O2.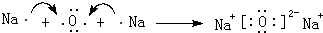 .
. 分析 X、Y、Z、W四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大,Z原子最外层电子数是次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故Z为O元素;Y、Z为同周期的相邻元素,Y的原子序数小于氧,则Y为N元素;Y与X形成的分子中有3个共价键,则X为H元素;X、W同主族,处于ⅠA族,W的原子序数大于氧,故W为Na元素,W原子的质子数等于Y、Z原子最外层电子数之和,据此解答.
解答 解:X、Y、Z、W四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大,Z原子最外层电子数是次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故Z为O元素;Y、Z为同周期的相邻元素,Y的原子序数小于氧,则Y为N元素;Y与X形成的分子中有3个共价键,则X为H元素;X、W同主族,处于ⅠA族,W的原子序数大于氧,故W为Na元素,W原子的质子数等于Y、Z原子最外层电子数之和.
(1)由上述分析可知,X为H元素、Y为N元素、Z为O元素、W为Na,
故答案为:H;N;O;Na;
(2)由以上元素中两两形成的化合物中,溶于水显碱性的气态氢化物为NH3,其电子式为 ,它的化学键属于共价键;含有离子键和非极性共价键的化合物Na2O2,
,它的化学键属于共价键;含有离子键和非极性共价键的化合物Na2O2,
故答案为: ;共价;Na2O2;
;共价;Na2O2;
(3)由H、N、O所形成的常见离子化合物是NH4NO3,W最高价氧化物对应水化物为NaOH,两种化合物的浓溶液混合共热的离子反应方程式为 NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O,H与Na形成的化合物为NaH,将该化合物溶于水,发生反应:NaH+H2O═NaOH+H2↑,其中水中氢元素化合价降低,水做氧化剂,
故答案为:NH4NO3;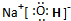 ;NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O;氧化剂;
;NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O;氧化剂;
(4)用电子式表示Na2O化合物的形成过程: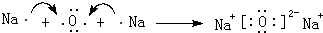 ,
,
故答案为: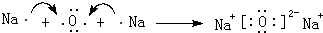 .
.
点评 本题考查结构性质位置关系,推断元素是解题关键,难度中等,(3)中根据水解原理NaH与水的反应,掌握用电子式表示化学键或物质的形成.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大于 57.3 kJ | B. | 等于 57.3 kJ | C. | 小于 57.3 kJ | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
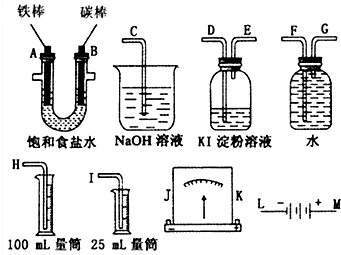 某课外小组做电解食盐水的探究实验,现有如图所示所列实验装置,请从其中选择适当的装置并加以组装,要求检验氯气的氧化性,并测定产生氢气的体积.
某课外小组做电解食盐水的探究实验,现有如图所示所列实验装置,请从其中选择适当的装置并加以组装,要求检验氯气的氧化性,并测定产生氢气的体积.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
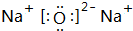 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
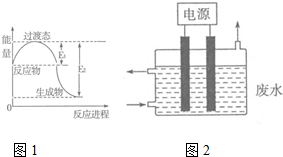 氮元素的化合物种类繁多,性质也各不相同.
氮元素的化合物种类繁多,性质也各不相同.| t/s | 0 | 120 | 180 | 240 | 330 | 530 | 600 | 700 | 800 |
| α/% | 0 | 33 | 42 | 49 | 59 | 73 | 74 | 75 | 75 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com