
 ③
③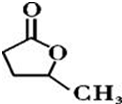 、
、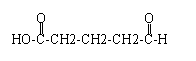 .
.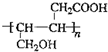 .
.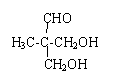 .
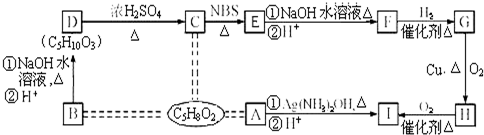
. 分析 有机物A、B、C互为同分异构体,分子式为C5H8O2,A的碳链无支链,且A中只有一种官能团(-CHO);可确定A为戊二醛,结构简式为OHC(CH2)3CHO,可得I为HOOC(CH2)3COOH,B的分子式为C5H8O2,属于五元环酯,说明环上有4个碳原子和1个氧原子,且环上还有一个甲基,B转化为D,D为一种羟基酸,D中含有羟基能发生消去反应生成C,C中含有一个碳碳双键和羧基,C能和NBS发生取代反应得到E,E发生水解反应生成F,F与氢气发生加成反应生成G,G可以连续发生氧化反应生成I,由I的结构可知,则E中溴原子处于碳链一端,根据题目中的已知,可知C中必有CH3-CH=CH-结构,结合上述分析C的结构简式为CH3CH=CHCH2COOH,由此可以确定D中羟基的位置,即D的结构简式为CH3CH(OH)CH2CH2COOH,进而可得B的结构简式为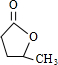 ,E为CH2Br-CH=CH-CH2COOH,CH2Br-CH=CH-CH2COOH在氢氧化钠水溶液、加热反应后即发生碱性水解,再酸化生成F,F为HO-CH2-CH=CH-CH2COOH,F与氢气发生加成反应生成G,G为HOCH2CH2CH2CH2COOH,G催化氧化生成H,H为OHC(CH2)3COOH,从而解决此题.
,E为CH2Br-CH=CH-CH2COOH,CH2Br-CH=CH-CH2COOH在氢氧化钠水溶液、加热反应后即发生碱性水解,再酸化生成F,F为HO-CH2-CH=CH-CH2COOH,F与氢气发生加成反应生成G,G为HOCH2CH2CH2CH2COOH,G催化氧化生成H,H为OHC(CH2)3COOH,从而解决此题.
解答 解:(1)根据题中的信息 ,HOOCCH2CH=CHCH3与NBS在加热的条件下发生取代反应生成HOOCCH2CH=CHCH2Br,HOOCCH2CH=CHCH2Br含有溴元素,能发生水解反应生成醇,既得到F的结构简式HOOCCH2CH=CHCH2OH,然后与H2发生加成反应生成G,既得G的结构简式为HOOCCH2CH2CH2CH2OH,HOOCCH2CH2CH2CH2OH中含有-OH,因此能发生氧化反应生成醛,既得H的结构简式为:HOOCCH2CH2CH2CHO,结合(1)中推出的B的结构简式得到B为
,HOOCCH2CH=CHCH3与NBS在加热的条件下发生取代反应生成HOOCCH2CH=CHCH2Br,HOOCCH2CH=CHCH2Br含有溴元素,能发生水解反应生成醇,既得到F的结构简式HOOCCH2CH=CHCH2OH,然后与H2发生加成反应生成G,既得G的结构简式为HOOCCH2CH2CH2CH2OH,HOOCCH2CH2CH2CH2OH中含有-OH,因此能发生氧化反应生成醛,既得H的结构简式为:HOOCCH2CH2CH2CHO,结合(1)中推出的B的结构简式得到B为 ,H为
,H为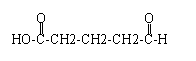 ,
,
故答案为: ;
;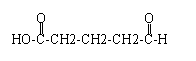 ;
;
(2)根据F的结构简式为:HOOCCH2CH=CHCH2OH知,它能发生加聚反应,生成高分子化合物,方程式为nHOOCCH2CH=CHCH2OH→ ,故得出HOOCCH2CH=CHCH2OH发生加聚反应生成
,故得出HOOCCH2CH=CHCH2OH发生加聚反应生成 ,
,
故答案为: ;
;
(3)根据上面的分析得知,E的结构简式为:HOOCCH2CH=CHCH2Br,HOOCCH2CH=CHCH2Br含有羧基、碳碳双键、卤素原子三种官能团,根据官能团的性质,推出它具有以下化学性质:能发生取代反应、加成反应、水解反应、消去反应、聚合反应、氧化反应、还原反应、酯化反应.不能发生银镜反应,
故答案为:③;
(4)A为戊二醛,结构简式为OHC(CH2)3CHO,A→I的反应方程式(只写①条件下的反应)为:OHCCH2CH2CH2CHO+4Ag(NH3)2OH$\stackrel{△}{→}$NH4OOCCH2CH2CH2COONH4+4Ag↓+6NH3+2H2O,故答案为:OHCCH2CH2CH2CHO+4Ag(NH3)2OH$\stackrel{△}{→}$NH4OOCCH2CH2CH2COONH4+4Ag↓+6NH3+2H2O;
(5)根据题中的信息M是D的同分异构体D的化学式为C5H10O3可知M中应有5个C原子、10个H原子、3个O原子,结合题中的信息,①分子中只含有一个甲基(-CH3);②能发生银镜反应;③1mol M与足量Na反应能产生标准状况下22.4L的气体;④除官能团上的氢原子外,还有两种不同类型的氢原子条件,写出符合要求的结构简式有:HOOCC(CH3)(OH)CH2CHO、HOOCCH(OH)CH(CH3)CHO、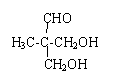 ,从中选出任意一种即可.
,从中选出任意一种即可.
故答案为: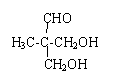 .
.
点评 本题系统全面的考查了有机化合物合成推断,解决这类题目要把握住官能团、有机基本反应类型,要系统的把握官能团的性质、有机基本反应类型,知识体系一定要系统.在根据官能团的性质结合反应类型推断时很容易出错,要注意有机化合物的合成推断题,解决这类问题,主要是依据有机反应的基本类型,官能团的性质,有机物的性质,结合题中给出的信息,找出解题的突破口解决.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:选择题
| A. | NCl3分子中N-Cl键的键长比CCl4分子中C-Cl键的键长长 | |
| B. | NCl3分子是非极性分子 | |
| C. | 分子中的所有原子均达到8电子稳定结构 | |
| D. | NCl3不含孤电子对 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定有H2、CO2和HCl | B. | 一定有CO、CO2和水蒸气 | ||
| C. | 一定没有CO2,肯定有H2 | D. | 可能有CO2、NH3和水蒸气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
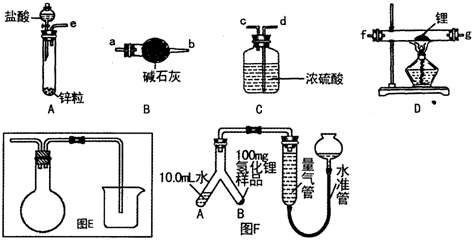
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 不纯物质 | 除杂试剂 | 分离方法 | |
| A | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 过滤 |
| B | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| C | 苯(Br2) | KOH溶液 | 分液 |
| D | 苯(苯酚) | 浓溴水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
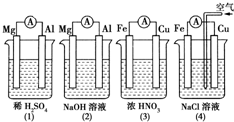
| A. | (1)(2)中Mg作负极,(3)(4)中Fe作负极 | |
| B. | (2)中Mg作正极,电极反应式为:6H2O+6e-═6OH-+3H2↑ | |
| C. | (3)中Fe作电池负极,电极反应式为:Fe-3 e-═Fe3+ | |
| D. | (4)中Cu作正极,电极反应式为:2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150mL | B. | 200mL | C. | 450mL | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有的放热反应不加热都能进行 | |
| B. | 任何化学反应的发生一定伴有能量变化 | |
| C. | 吸热反应和放热反应都需要加热才能发生 | |
| D. | 化学反应吸收或放出热量的多少与参加反应的物质的多少无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com