
某化学兴趣小组的同学用如图所示装置研究电化学问题。当闭合该装置的电键时,观察到电流计的指针发生偏转。下列有关说法不正确的是
( )
A.甲装置是原电池,乙装置是电解池
B.当甲中产生0.1 mol气体时,乙中析出固体的质量为3. 2 g
C.实验一段时间后,甲烧杯中溶液的pH增大
D.将乙中的C电极换成铜电极,则乙装置可变成电 镀装置
镀装置
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
下列有关铁及其化合物的说法中不正确的是
A.工业上在高温下用CO还原含Fe2O3的铁矿石炼铁
B.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4
C.工业上可用铁质容器储存、运输浓硝酸和浓硫酸
D.氯化铁溶液有较强氧化性,故可用作净水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关金属腐蚀与防护的说法不正确的是( )
A.钢铁在弱碱性条件下发生电化学腐蚀的正极反应是:O2+2H2O+4e-===4OH-
B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
D.可将地下输油钢管与外加直流电源的负极相连以保护它不受腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解某溶液时,发现两极只有H2和O2生成。则电解一段时间后,下列有关该溶液(与电解前同温度)的说法中,正确的有( )
①该溶液的pH值可能增大 ②该溶液的pH值可能减小 ③该溶液的pH值可能不变 ④该溶液的浓度可能增大 ⑤该溶液的浓度可能不变 ⑥该溶液的浓度可能减小
④该溶液的浓度可能增大 ⑤该溶液的浓度可能不变 ⑥该溶液的浓度可能减小
A.三种 B.四种
C.五种 D.六种
查看答案和解析>>
科目:高中化学 来源: 题型:
请从下图中选用必要的装置进行电解饱和食盐水的实验,要求测定产生氢气的体积(大于25 mL),并检验氯气的氧化性。

(1)A极发生的电极反应式是______ ____________________________,
____________________________,
B极发生的电极反应式是__________________________________________。
电解饱和食盐水的化学方程式____________________________________________。
(2)电源、电流表与A、B两极的正确连接顺序为:
L→( )→( )→( )→( )→M。
(3)设计上述气体实验装置时,各接口的正确连接顺序为:________接________、________接A、B接________、________接________。
(4)在实验中,盛有KI淀粉溶液的容器中发生反应的离子方程式为______________。
(5)已知饱和食盐水50 mL,某时刻测得H2体积为5.6 mL(标准状况)。此时溶液pH约为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示。下列描述正确的是( )
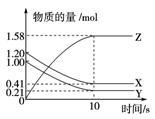
A、反应开始到10 s,用Z表示的反应速率为0.158 mol·(L·s)-1
B、反应开始到10 s,X的物质的量浓度减少了0.79 mol·L-1
C、反应开始到10 s时,Y的转化率为79.0 %
D、反应的化学方程式为:X(g)+Y(g)  Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
在200 mL氯化镁和氯化铝的混合液中,Mg2+的物质的量浓度为0.2 mol·L-1,Cl-的物质的量浓度为1.3 mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需要加入4 mol·L-1 NaOH溶液的体积为
A.40 mL B.72 mL C.80 mL D.128 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
浓H2SO4 密度1.84g/mL,物质的量浓度为18.4 mol/L , 质量分数为98% ,取10mL浓H2SO4和amL水混合得物质的量浓度为Cmol/L,质量分数为b%。下列组合正确的是
(1). 若b=49 则a=18.4 C>9.2 (2) 若b=49 则a=18.4 C<9.2
(3). 若C=9.2 则a>10 b>49% (4) 若C=9.2 则a>10 b<49%
A.(1) (3) B.(1) (4) C.(2) (3) D.(2) (4)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com