
| A. | 原子半径r(X)<r(Y),离子半径r(X-)>r(Y2+) | |
| B. | X的简单气态氢化物的稳定性比W的弱 | |
| C. | X分别与Y、W形成的化合物中化学键类型相同 | |
| D. | Z是活泼的金属,其最高价氧化物对应的水合物为强碱 |
分析 短周期元素X、Y、Z、W的原子序数依次增大,X-与Y2+电子层结构与Ne原子的电子层结构相同,则X为F元素、Y为Mg;W的最外层电子数是内层电子总数的一半,W原子序数比X至少大3,可知W只能处于第三周期,故原子最外层电子数为5,则W为P元素;Z单质是金属,原子序数介于Mg、P之间,故Z为Al,据此解答.
解答 解:短周期元素X、Y、Z、W的原子序数依次增大,X-与Y2+电子层结构与Ne原子的电子层结构相同,则X为F元素、Y为Mg;W的最外层电子数是内层电子总数的一半,W原子序数比X至少大3,可知W只能处于第三周期,故原子最外层电子数为5,则W为P元素;Z单质是金属,原子序数介于Mg、P之间,故Z为Al.
A.同周期自左而右原子半径减小、同主族自上而下原子半径增大,故原子半径r(F)<r(Mg),电子层结构相同,核电荷数越大离子半径越小,故离子半径r(F-)>r(Mg2+),故A正确;
B.非金属性F>S,非金属性越强,氢化物越稳定,故氢化物稳定性HF>H2S,故B错误;
C.F与Mg形成MgF2,含有离子键,而F与P元素形成共价键,故C错误;
D.Al是活泼金属,但氢氧化铝为弱碱,故D错误,
故选A.
点评 本题考查原子结构与元素性质、元素周期律等,推断元素是解题关键,有利于基础知识的巩固.


科目:高中化学 来源: 题型:选择题
| A. | 镭的金属性比钙弱 | B. | 单质能与水反应生成氢气 | ||
| C. | 在化合物中呈+2价 | D. | 碳酸镭难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
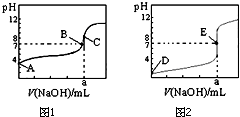 如图1、2为常温下用0.10mol•L-1 NaOH溶液滴定20.00mL 0.10mol•L-1 盐酸和20.00mL 0.10mol•L-1醋酸的曲线.若以HA表示酸,下列判断和说法正确的是( )
如图1、2为常温下用0.10mol•L-1 NaOH溶液滴定20.00mL 0.10mol•L-1 盐酸和20.00mL 0.10mol•L-1醋酸的曲线.若以HA表示酸,下列判断和说法正确的是( )| A. | 图1是滴定盐酸的曲线 | |
| B. | E点时溶液中离子浓度为c(Na+ )=c(A- ) | |
| C. | B点时,反应消耗溶液体积:V(NaOH)>V(HA) | |
| D. | 当0mL<V(NaOH)<20.00mL时,溶液中一定是c(A-)>c(Na+ )>c(H+ )>c(OH- ) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=5的H2S溶液中,c(H+)=c(HS一)=1×10-5mol•L-1 | |
| B. | 含有AgCl和AgI固体的悬浊液中,c(Ag+)>c(Cl-)=c(I-) | |
| C. | 在新制氯水中加入氯化钠固体,水的电离平衡不移动 | |
| D. |  若R为Zn,则如图采用了牺牲阳极的阴极保护法 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| X | Y | ||
| Z | W |
| A. | 原子半径由小到大的顺序为X<Z<Y<W | |
| B. | Y元素最高价氧化物对应的水化物化学式为HYO3 | |
| C. | X、Z两种元素的氧化物中所含化学键类型相同 | |
| D. | Y最简单气态氢化物比Y相邻周期同主族元素气态氢化物沸点高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在NH4Cl饱和溶液中加入金属镁可以得到两种气体 | |
| B. | pH=12Ba(OH)2溶液中c(OH-)是0.001mol/LNaOH溶液c(OH-)的10倍 | |
| C. | 常温下,CH3COONa和CH3COOH的混合溶液中(pH=7):c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) | |
| D. | 常温下,Cd(OH)2和Co(OH)2的混合悬浊液中,c(Cd2+)是c(Co2+)的4倍,已知:KSP[Cd(OH)2]=7.2×10-15,Ksp[Co(OH)2]=1.8×10-15 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | I1 | I2 | I3 | I1+I2+I3 | I4 |
| Sc(钪) | 633 | 1235 | 2389 | 4257 | 7019 |
| Y(钇) | 616 | 1181 | 1980 | 3777 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 3455 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3523 | 3547 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度(℃) | 10 | 40 | 75 |
| 剩余固体质量(g) | 201 | 132 | 72 |
| 温度(℃) | 10 | 40 | 75 |
| 溶解度 | 81 | 104 | 150 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N层比M层少8个电子的元素 | B. | L层比M层多一个电子的元素 | ||
| C. | 最高价为+6价的元素 | D. | 无负化合价的元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com