
【题目】在元素周期表前四周期中原子序数依次增大的六种元素A、B、C、D、E、F中,A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C的氧化物是导致酸雨的主要物质之一,D原子核外电子有8种不同的运动状态,E的基态原子在前四周期元素的基态原子中单电子数最多,F元素的基态原子最外能层只有一个电子,其它能层均已充满电子.
(1)写出基态E原子的价电子排布式 .
(2)B、C、D三元素第一电离能由小到大的顺序为(用元素符号表 示) ;A与C形成CA3型分子,分子中C原子的杂化类型为 ,分子的立体结构为 ;C的单质与 BD化合物是等电子体,据等电子体的原理,写出BD化合物的电子式 ; A2D由液态形成晶体时密度 (填增大,不变或减小),分析主要原因(用文字叙述)
(3)已知D、F能形成一种化合物,其晶胞的结构如图所示,则该化合物的化学式为(用元素符号表示) ;若相邻D原子和F原子间的距离为a cm,阿伏伽德罗常数为NA,则该晶体的密度为 g/cm3(用含a、NA的符号表示).

【答案】(1)3d54s1;(2)C<O<N;sp3;三角锥形;![]() ;水形成晶体时,每个水分子与4个水分子形成氢键,构成空间正四面体网状结构,水分子空间利用率低,密度反而减小;(3)Cu2O;
;水形成晶体时,每个水分子与4个水分子形成氢键,构成空间正四面体网状结构,水分子空间利用率低,密度反而减小;(3)Cu2O;![]() .
.
【解析】在元素周期表前四周期中原子序数依次增大的六种元素A、B、C、D、E、F中,B的一种核素在考古时常用来鉴定一些文物的年代,则B为碳元素,D原子核外电子有8种不同的运动状态,则D为氧元素,C的氧化物是导致酸雨的主要物质之一,且C的原子序数小于D,所以C为氮元素,E的基态原子在前四周期元素的基态原子中单电子数最多,其原子外围电子排布式为1s22s22p63s23p63d54s1,则E为铬元素,F元素的基态原子最外能层只有一个电子,其它能层均已充满,则F原子外围电子排布为3d104s1,所以F为铜元素,A与其余五种元素既不同周期也不同主族,所以A为氢元素.
(1)E为铬元素,基态E原子的价电子排布为3d54s1,故答案为:3d54s1;
(2)C、O、N元素都是第二周期非金属元素,同一周期元素自左而右第一电离能呈增大趋势,但N元素原子2p能级是半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能:C<O<N;
A与C形成NH3分子,分子中N原子形成3个N﹣H、含有1对孤对电子,故N原子杂化类型为sp3,分子的立体结构为三角锥形;
C的单质为N2,化合物CO是等电子体,二者结构相似,CO分子中C原子与O原子之间形成三对共用电子对,故CO的电子式为![]() ;
;
H2O形成晶体时,每个水分子与4个水分子形成氢键,构成空间正四面体网状结构,水分子空间利用率低,密度反而减小,
(3)根据晶胞的结构图可知,晶胞中含有氧原子数为1+8×![]() =2,铜原子数为4,所以该化合物的化学式为Cu2O,晶胞质量为(4×
=2,铜原子数为4,所以该化合物的化学式为Cu2O,晶胞质量为(4×![]() +2×
+2×![]() )g,若相邻氧原子和铜原子间的距离为a cm,则晶胞的体对角线为4acm,所以边长为
)g,若相邻氧原子和铜原子间的距离为a cm,则晶胞的体对角线为4acm,所以边长为![]() cm,所以体积为(
cm,所以体积为(![]() cm)3cm3,该晶体的密度为(4×
cm)3cm3,该晶体的密度为(4×![]() +2×
+2×![]() )g÷(
)g÷(![]() cm)3=
cm)3=![]() g/cm3
g/cm3


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】黑火药的爆炸反应为:2KNO3+3C+S=A+N2↑+3CO2↑(已配平)
(1)除S以外,上述所及元素的电负性从大到小依次为____________________。
(2)在生成物中,A的电子式为____________;含极性共价键的分子的中心原子轨道杂化类型为________。
(3)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对物质用途的描述中,错误的是( )
A.铝可用于冶炼某些熔点较高的金属
B.Na2O2可用作漂白剂
C.碱石灰可用于干燥CO2、NH3等气体
D.NaClO可用作消毒剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是

A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
C. 上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠、碳酸氢钠是日常生产生活中常用的两种盐。在实验室中制取NaHCO3的方法有多种。请
依据下列方法回答问题:
方法一:模拟工业“侯氏制碱法”制取:(原理NaCl+H2O+CO2+NH3 = NaHCO3↓+NH4Cl)
第一步:连接好装置,检验气密性,在仪器内装人药品。
第二步:让某一装置先发生反应,直到产生的气体不能再在Ⅲ中溶解,再通入另一装置中产生的气体,片刻后,Ⅲ中出现固体。继续向Ⅲ中通入两种气体,直到不再有固体产生。
第三步:分离Ⅲ中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的某固体粉末,有NH4Cl晶体析出。

(1)图中所示装置的连接顺序是:a接f;e接________;b接_________(填接口编号)。
(2)I中盛放稀盐酸的仪器名称是_____________,IV中应选用的液体为________________。
(3)第二步中让_____________ (填序号)装置先发生反应。
(4)第四步中所加固体粉末为________。所得的晶体中常含有少置的NaCl和NaHCO3(约占5%~8%),请设计一个简单的实验,不使用其他任何试剂,证明所得晶体大部分是NH4Cl。简要写出操作和现象______________________。
方法二:把CO2通人饱和Na2CO3溶液制取NaHCO3。装置如下图所示(气密性已检验,部分夹持装置略):

(5)请结合化学平衡移动原理解释B中溶液的作用_________________。
(6)当C中有大量白色固体析出时,停止实验,将固体过滤、洗涤、干燥备用。为确定固体的成分,实验小组设计方案如下(取一定量的固体,配成溶液作为样液,其余固体备用):
①方案1:取样液与澄清的Ca(OH)2溶液混合,出现白色沉淀。
实验小组对现象产生的原理进行分析,认为该方案不合理,理由是________________。
②方案2:取样液与BaCl2溶液混合,出现白色沉淀并有气体产生。
实验小组认为固体中存在NaHCO3,其离子方程式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关N(NO2) 3的说法正确的是
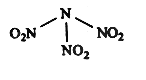
A.分子中N、O间形成的共价键是非极性键 B.分子中四个氮原子共平面
C.该物质既有氧化性又有还原性 D.15.2g该物质含有6.02×1022个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素A、B、C、D的性质或结构信息如下:
信息:①原子半径:A>B>C>D ②四种元素之间形成的某三种分子的比例模型及部分性质如下:
甲:![]() 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.
乙:![]() 无色,无气味并且易燃.是常见的一种基础能源,17年5月18日,我国首次开采成功它的水合物并连续产量,可解千年能源之忧。
无色,无气味并且易燃.是常见的一种基础能源,17年5月18日,我国首次开采成功它的水合物并连续产量,可解千年能源之忧。
丙:![]() 有强氧化性的弱酸,可以用于消毒杀菌.
有强氧化性的弱酸,可以用于消毒杀菌.
请根据上述信息回答下列问题.
(1)B元素在元素周期表中的位置为_____,请写出BC2分子的电子式:______.
(2)A、E、F在同一周期,E元素的单质还原性最强,F元素的某些盐类常用作净水剂.E单质与甲反应有化合物X生成.请写出以下两个反应的离子方程式:
①A元素的单质与物质甲发生反应:________________________________.
②F、C两种元素组成的化合物Y可作为耐高温结构的材料,X与Y两种化合物在溶液中发生反应的离子方程式:_________________________________________________.
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构.向盛有一定浓度丁溶液的试管中,逐滴加入硫酸酸化的硫酸亚铁溶液.滴加过程中的现象为:①试管中溶液变成深棕黄色,②开始有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,继续滴加溶液,静置一段时间,试管底部出现红褐色沉淀.请回答“片刻后反应变得剧烈”的原因
a_____________________b_________________.
(4)物质戊的元素组成和乙相同,戊分子具有18电子结构.与乙互为同系物,则戊的氯取代有机物的共________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞。NaCl晶体的晶胞如图所示。随着科学技术的发展,测定阿伏伽德罗常数的手段越来越多,测定精确度也越来越高。现有一简单可行的测定方法,具体步骤如下:①将固体食盐研细,干燥后,准确称取mgNaCl固体并转移到定容仪器A中。②用滴定管向仪器A中加苯,并不断振荡,继续加苯至A仪器的刻度线,计算出NaCl固体的体积为VmL。回答下列问题:
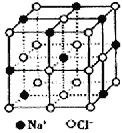
(1)步骤①中A仪器最好用_________(填仪器名称)
(2)能否用胶头滴管代替步骤②中的滴定管________,其原因是____________。
(3)经X射线衍射测得NaCl晶胞中最邻近的Na+和Cl-平均距离为acm,则利用上述方法测得的阿伏伽德罗常数的表达式为NA=________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com