

 ?CO2(g)��NO(g)��Ӧ�����������仯ʾ��ͼ��һ�������£��ڹ̶��ݻ����ܱ������и÷�Ӧ�ﵽƽ��״̬�����ı�����һ������X��Y��X�ı仯��ϵ������ͼ�������й�˵����ȷ����(����)
?CO2(g)��NO(g)��Ӧ�����������仯ʾ��ͼ��һ�������£��ڹ̶��ݻ����ܱ������и÷�Ӧ�ﵽƽ��״̬�����ı�����һ������X��Y��X�ı仯��ϵ������ͼ�������й�˵����ȷ����(����)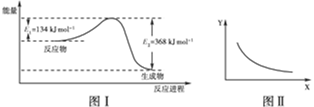
| A���÷�Ӧ���ʱ䦤H����234 kJ��mol��1 |
| B����X��ʾ��ϵ��ѹǿ����Y��ʾ�Ŀ�����NO2��ת���� |
| C����X��ʾ�¶���Y��ʾ�Ŀ�����CO2���ʵ���Ũ�� |
| D������CO����ʼŨ�ȣ�ƽ��������Ӧ�����ƶ�����Ӧ������ |
 ��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д� �����������Ż�ѧϰϵ�д�
�����������Ż�ѧϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ơ��ƿ��ƿ�����Ϸ��������ĭ |
| B��������ˮ����ɫ��dz |
| C����ҵ����������Ĺ�����ʹ�ù����Ŀ�������߶��������ת���� |
| D����H2��I2��g����HI��ɵ�ƽ����ϵ����ѹ����ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
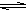 2C(g) + D(g) ��H>0�������淴Ӧ���ʵ�Ӱ�죬���߽����ʾ����ƽ��ʱ���¶Ȼ�ѹǿ��������ȷ����
2C(g) + D(g) ��H>0�������淴Ӧ���ʵ�Ӱ�죬���߽����ʾ����ƽ��ʱ���¶Ȼ�ѹǿ��������ȷ����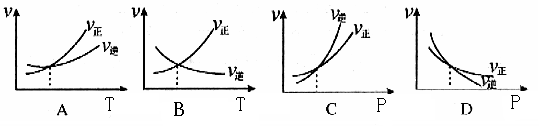
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
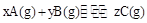
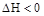 ���ﵽ��ѧƽ�����A�����Ũ��Ϊ
���ﵽ��ѧƽ�����A�����Ũ��Ϊ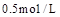 ���������½��ܱ��������ݻ�����һ�����ٴδﵽƽ��ʱ�����A�����Ũ��Ϊ
���������½��ܱ��������ݻ�����һ�����ٴδﵽƽ��ʱ�����A�����Ũ��Ϊ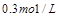 ��������������ȷ���ǣ� ��
��������������ȷ���ǣ� ��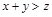
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3OH
CH3OH
 CH3OH��g����ƽ�ⳣ��Ϊ ��10min�������ڵ�ѹǿ��Ϊԭ���� �����ı����������������COת���ʵ��� ��
CH3OH��g����ƽ�ⳣ��Ϊ ��10min�������ڵ�ѹǿ��Ϊԭ���� �����ı����������������COת���ʵ��� ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����Ӧ������Ũ�� | B�������淴Ӧ���� �� | C����Ӧ������ѹǿ | D����Ӧ������и����ʵİٷֺ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
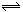 2C(g)�ﵽƽ��ı�־�ǣ� ��
2C(g)�ﵽƽ��ı�־�ǣ� ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
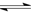 2NH3(g) ��H =��92.4 kJ��mol-1�����¶ȡ��ݻ���ͬ��2���ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������£�
2NH3(g) ��H =��92.4 kJ��mol-1�����¶ȡ��ݻ���ͬ��2���ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������£�| ���� | ����1 | ����2 |
| ��Ӧ��Ͷ����ʼ̬ | 1mol N2��3mol H2 | 2mol NH3 |
| NH3��ƽ��Ũ��/mol��L-1 | cl | c2 |
| ��Ӧ�������仯 | �ų�a kJ | ����b kJ |
| ��ϵѹǿ/Pa | p1 | p2 |
| ��Ӧ��ת���� | ��1 | ��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
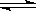 mZ(g)����H����a kJmol��1(a>0)�����мס������ݻ�����ҹ̶����ܱ��������ڱ��ָ��¶Ⱥ㶨�������£����ܱ���������ͨ��2 mol X��1 mol Y���ﵽƽ��״̬ʱ���ų�����b kJ�����ܱ���������ͨ��1 mol X��0.5 mol Y���ﵽƽ��ʱ���ų�����c kJ����b>2c����a��b��m��ֵ���ϵ��ȷ����
mZ(g)����H����a kJmol��1(a>0)�����мס������ݻ�����ҹ̶����ܱ��������ڱ��ָ��¶Ⱥ㶨�������£����ܱ���������ͨ��2 mol X��1 mol Y���ﵽƽ��״̬ʱ���ų�����b kJ�����ܱ���������ͨ��1 mol X��0.5 mol Y���ﵽƽ��ʱ���ų�����c kJ����b>2c����a��b��m��ֵ���ϵ��ȷ����| A��m��4 | B��a��b | C��a< | D��m��2 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com