
| A、向氢氧化钡溶液中加硫酸溶液:Ba2++SO42-=BaSO4↓ | ||||
| B、通常情况下铁与稀硝酸反应:Fe+2H+=Fe2++H2↑ | ||||
C、二氧化锰与浓盐酸共热:MnO2+4 HCl (浓)
| ||||
| D、碳酸氢钠溶液中加入少量的澄清石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
| ||


科目:高中化学 来源: 题型:
| A、吸热 | B、放热 | C、熵减 | D、熵增 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化亚铁溶液跟氯气反应:2Fe2++Cl2═2Fe3++2Cl- |
| B、向碳酸氢钠溶液中滴加少量的稀硝酸:CO32-+2H+═CO2↑+H2O |
| C、铜与稀硝酸反应:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
| D、碳酸氢铵溶液和足量氢氧化钠溶液反应:NH4++OH-═NH3?H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2晶体中的阴离子和阳离子 |
| B、NaHCO3晶体中的钠离子和碳酸氢根离子 |
| C、24 12Mg2+离子中的质子数和中子数 |
| D、NaCl溶液中的钠离子和氯离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在合成氨工业中不断补充N2和H2并将生成的NH3及时地从混合气中分离出来 |
| B、合成氨的反应需要加入催化剂 |
| C、增大压强有利于合成氨的反应 |
| D、开启啤酒瓶后,瓶中马上泛起大量泡沫 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、V2=10V1 |
| B、V1<10 V2、 |
| C、10V1>V2 |
| D、V2>10V1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、萤石可溶于水,氟化银也可溶于水 |
| B、碱金属元素单质均为银白色固体,且在一定条件下与氧气反应均可得到过氧化物 |
| C、在金属活动性顺序表中钠比铜活泼,所以钠可以从硫酸铜溶液中置换出铜单质 |
| D、虽然氟元素的非金属性强于氯元素,氟单质也不能从氯化钠溶液中置换出氯单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
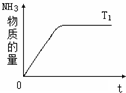 在一定温度下,向容积不变的容器中加入2mol N2、8mol H2及固体催化剂,使之反应.已知:N2(g)+3H2(g)?2NH3(g);△H=-92.2kJ?mol-1.平衡时,容器内气体压强为起始时的80%.
在一定温度下,向容积不变的容器中加入2mol N2、8mol H2及固体催化剂,使之反应.已知:N2(g)+3H2(g)?2NH3(g);△H=-92.2kJ?mol-1.平衡时,容器内气体压强为起始时的80%.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com