
【题目】氯化亚铜(CuCl)是白色粉末,不溶于水、乙醇及稀硫酸,在空气中迅速被氧化成绿色,常用作有机合成工业中的催化剂。实验室拟以下列方法制取CuCl:在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl。试回答以下问题:
(1)CuCl制备过程中需配制物质的量浓度为2.0 mol/L的CuSO4溶液。
①配制950 mL 2.0 mol/L的CuSO4溶液应称取胆矾的质量为____ ___g。
②某学生实际配制CuSO4溶液的浓度为1.8 mol/L,原因可能是__ ___。
A.托盘天平的砝码生锈 B.容量瓶中原来存有少量蒸馏水
C.溶解后的烧杯未经多次洗涤 D.胶头滴管加水定容时仰视刻度
(2)写出用上述方法制备CuCl的离子方程式_____ ____。
(3)在上述制取过程中,经过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却,密封包装即得产品。其中“于70℃真空干燥”的目的是 ; _。(回答两点)
(4)据世界卫生组织统计,最常用的避孕环含金属铜,避孕过程中生成了CuCl。其原因是铜与人体分泌物中的盐酸以及子宫内的空气反应:Cu+HCl+O2=CuCl+HO2,HO2(超氧酸) 不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是____ __ ___。
A. 氧化产物是HO2
B. HO2在碱中能稳定存在
C. HO2的电离方程式是HO2![]() H+ + O2-
H+ + O2-
D. 1mol Cu 参加反应有2mol电子发生转移
【答案】(1)①500;②CD;(2)2Cu2++SO32—+2Cl—+H2O![]() 2CuCl↓+SO42—+2H+;
2CuCl↓+SO42—+2H+;
(3)加快乙醇和水的蒸发,防止CuCl被空气氧化;(4)C。
【解析】试题分析:(1)①实验室没有950mL的容量瓶,应用1000mL容量瓶,因此需要的胆矾的质量为m(CuSO4·5H2O)=1000×10-3×2×250=500g;②浓度偏小,根据c=m/MV,A、砝码生锈,砝码质量增加,因此所配浓度偏大,故错误;B、含有少量水,对溶液浓度无影响,故错误;C、未洗涤烧杯和玻璃棒,造成溶质的质量减少,浓度偏小,故正确;D、定容时仰视刻度,所配溶液体积增大,浓度偏小,故正确;(2)根据题目中信息,离子反应方程式为:2Cu2++SO32-+2Cl-+H2O![]() 2CuCl↓+2H++SO42-;(3)乙醇易挥发,水易蒸发,70℃有利于乙醇和水的蒸发,根据信息CuCl在空气中迅速被氧化,真空的目的防止CuCl的氧化,因此70℃真空干燥的目的:加快乙醇和水的蒸发,防止CuCl被空气氧化;(4)A、HO2由O2产生,O2是氧化剂,则HO2属于还原产物,故错误;B、HO2是超氧酸,和碱发生中和反应,故错误;C、HO2是弱酸,应是部分电离,HO2
2CuCl↓+2H++SO42-;(3)乙醇易挥发,水易蒸发,70℃有利于乙醇和水的蒸发,根据信息CuCl在空气中迅速被氧化,真空的目的防止CuCl的氧化,因此70℃真空干燥的目的:加快乙醇和水的蒸发,防止CuCl被空气氧化;(4)A、HO2由O2产生,O2是氧化剂,则HO2属于还原产物,故错误;B、HO2是超氧酸,和碱发生中和反应,故错误;C、HO2是弱酸,应是部分电离,HO2![]() H+O2-,故正确;D、Cu由0价→+1价,因此1molCu参加反应转移1mole-,故错误。
H+O2-,故正确;D、Cu由0价→+1价,因此1molCu参加反应转移1mole-,故错误。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)从海水得到的粗食盐水中常含Ca2+、Mg2+、SO42﹣ , 需要分离提纯.现有含少量CaCl2、MgSO4的粗食盐水,在除去悬浮物和泥沙之后,要用4种试剂①盐酸;②Na2CO3;③NaOH;④BaCl2来逐一除去食盐水中Ca2+、Mg2+、SO42﹣ . 提纯的操作步骤和加入试剂的情况如图: 
图中a、b、c、d分别表示上述4种试剂中的一种,试回答:
(i)沉淀A的名称是;
(ii)试剂d是;判断试剂d已经足量的方法是;
(iii)现有下列仪器,过滤出沉淀A、B、C时必须用到(填序号),仪器③的名称是 . 
(2)海水蒸馏是由海水获得淡水的常用方法之一,在实验室里组成一套蒸馏装置肯定需要上述仪器中的一部分,则正确的是(填序号).
(3)海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要上述仪器中的(填序号),该仪器名称为 , 向该碘水中加入四氯化碳以提取碘单质的实验操作为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”简化表示.
(1)物质X:CH3CH=CHCH3可表示为![]()
X可以与溴水反应,该反应的化学方程式是_________________________;
X可以发生加聚反应,其产物分子的结构简式是______________________.
(2)一种有机物Y的键线式如图所示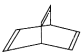
①Y的分子式为___________;
②有机物Z是Y的同分异构体,且属于芳香族化合物,则Z的结构简式是______________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 干冰升华时要吸收热量,所以这是吸热反应
B. 浓硫酸可用来干燥SO2、CO、Cl2等气体
C. 浓硫酸具有强氧化性,常温下不可用铝罐盛装
D. 二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,体现了其漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在火箭推进器中装有还原剂肼(N2H4)和强氧化剂H2O2,当它们混合时,即产生大量的氮气和水蒸气,并放出大量的热。已知0.4 mol液态肼和足量H2O2反应生成氮气和水蒸气时放出256.64 kJ的热量。
(1) 写出肼和H2O2反应的热化学方程式:______________________。
(2)已知H2O(l)=H2O(g) △H=+44 kJ/mol,则16 g液态肼与足量双氧水反应生成氮气和液态水时,放出的热量是_________________________。
(3)上述反应应用于火箭推进器,除释放出大量热量和快速产生大量气体外,还有一个很突出的优点是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 气体的摩尔体积为22.4 L·mol-1
B. 1 mol H2的质量是2 g,它所占的体积是22.4 L
C. 在标准状况下,1 mol任何物质所占的体积都为22.4 L·mol-1
D. 在标准状况下,1 mol任何气体所占的体积都约为22.4 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com