
下列有关实验的说法正确的是
A.除去铁粉中的铜粉,加入足量浓硫酸加热反应后进行过滤
B.不用任何其他试剂就可以鉴别NaOH溶液和Al2(SO4)3溶液
C.制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中
D.某溶液加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液一定含有大量CO32-
科目:高中化学 来源: 题型:
下列各组物质:①12C和14C ②CH3(CH2)5CH3和CH3CH=CHCH(CH3)C2H5
③CH3CH2CH2CH3和(CH3)2CHCH3 ④H2、D2、T2 ⑤癸烷和十六烷
|
|
|
⑥O2和O3
A.互为同位素的是(填序号,下同) ;B.互为同系物的是 ;
C.互为同分异构体的是 ; D.为同一种物质的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在BaCl2溶液中通入下列气体后,溶液中一定会出现白色沉淀的是( )
A. SO2 B. 先通NO2 ,后通SO2 C. 先通SO2,后通H2S D. NH3,CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
对于常温下0.1 mol·L-1氨水和0.1 mol·L-1醋酸,下列说法正确的是
A.0.1 mol·L-1氨水,溶液的pH=13
B.0.1 mol·L-1氨水加水稀释,溶液中c(H+)和c(OH-)都减小
C.0.1 mol·L-1醋酸溶液中:c(H+)=c(CH3COO-)
D.0.1 mol·L-1醋酸与0.1 mol·L-1NaOH溶液等体积混合所得溶液中:
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z三种主族元素,已知X+和Y-具有相同电子层结构,Z元素原子核电荷数比Y元素原子核电荷数少9,Y-在一定条件下可被氧化成YZ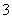 ,则下列说法正确的是
,则下列说法正确的是
A.X、Y、Z均属于短周期元素 B.离子半径X+>Y-
C.Y的气态氢化物可形成氢键
D.X、Y、Z三种元素组成的化合物中既含有离子键又含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学原理表述正确的是
A.氢硫酸溶液加水稀释,电离程度增大,H+浓度增大
B.同体积同pH的盐酸和醋酸与足量的锌反应,醋酸的反应速率快,生成H2的
物质的量多
C.NaHCO3溶液不显中性的原因:HCO3-+H2O ≒ CO32-+H3O+
D.Na2CO3溶液中满足:2c(Na+)=c(CO32-)+ c(HCO3-)+ c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E同主族,且D的氢化物常温时为液态。A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子。
(1)C的元素符号是 ;元素F在周期表中的位置 。
 (2)B、D、E元素的氢化物的沸点高低顺序为 > > (用化学式表示)。
(2)B、D、E元素的氢化物的沸点高低顺序为 > > (用化学式表示)。
(3)C4气态分子结构如图所示,已知断裂1molC-C吸收l67KJ的热量,
生成lmol C C放出942KJ热量。试写出由C4气态分子变成C2气态分
C放出942KJ热量。试写出由C4气态分子变成C2气态分
子的热化学方程式 。
(4)某盐x (C2A6F2)的性质与CA4F类似,是离子化合物,其水溶液因分
步水解而呈弱酸性。
① 盐x显酸性原因(用离子方程式表示) 。
② 写出足量金属镁加入盐x的溶液中所发生反应的化学方程式
。
(5)E所在周期中原子半径最大的元素与D元素可形成化合物у,酚酞试液遇у先变红后褪色,写出等物质的量的у与FeSO4投入水中恰好完全反应的离子反应方程式
。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验装置进行的相应实验,能达到实验目的的是


图1 图2 图3 图4
A.用图1所示装置除去Cl2中含有的少量HCl
B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图3所示装置制取少量纯净的CO2气体
D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com