
【题目】现有下列九种物质:①盐酸溶液 ②石墨 ③蔗糖 ④CO2⑤熔融NaHSO4⑥Ba(OH)2固体 ⑦氨水 ⑧纯硫酸 ⑨NaCl固体
(1)属于电解质的有__________;属于非电解质的有________;能导电的物质有________。
(2)②和SiO2在高温下可发生如下反应:3C+SiO2![]() SiC+2CO↑ (已知SiC中Si元素为+4价),上述反应中还原产物是_______;氧化剂与还原剂物质的量之比为_______。
SiC+2CO↑ (已知SiC中Si元素为+4价),上述反应中还原产物是_______;氧化剂与还原剂物质的量之比为_______。
(3)上述九种物质中有两种物质之间可发生离子反应:H++OH-===H2O,该离子反应对应的化学方程式为________________________
(4)⑤的电离方程式为______________________。
【答案】⑤⑥⑧⑨ ③④ ①②⑤⑦ SiC 1:2 Ba(OH)2+2HCl=BaCl2+2H2O NaHSO4=Na++HSO4-
【解析】
试题本题考查电解质和非电解质的判断,物质导电性的分析,氧化还原反应的分析,离子方程式和电离方程式的书写。
(1)①盐酸溶液属于混合物,既不是电解质也不是非电解质,盐酸溶液中含自由移动的阴、阳离子,能导电;②石墨属于单质,既不是电解质也不是非电解质,石墨能导电;③蔗糖属于化合物,蔗糖溶于水和熔融时都不能导电,属于非电解质,蔗糖不能导电;④CO2属于化合物,虽然其水溶液能导电,但导电的离子是由CO2与水反应生成的H2CO3电离产生的,CO2属于非电解质,CO2不能导电;⑤熔融NaHSO4属于化合物,溶于水和熔融时都能导电,属于电解质,熔融NaHSO4中含自由移动的阴、阳离子,能导电;⑥Ba(OH)2固体属于化合物,溶于水和熔融时都能导电,属于电解质,Ba(OH)2固体中的阴、阳离子不自由移动,不能导电;⑦氨水属于混合物,既不是电解质也不是非电解质,氨水中含自由移动的阴、阳离子,能导电;⑧纯硫酸属于化合物,溶于水能导电,属于电解质,纯硫酸中只存在分子,不能导电;⑨NaCl固体属于化合物,溶于水和熔融时都能导电,属于电解质,NaCl固体中阴、阳离子不自由移动,不能导电;属于电解质的有⑤⑥⑧⑨;属于非电解质的有③④;能导电的物质有①②⑤⑦。
(2)反应中C元素的化合价由0价升至CO中的+2价,CO为氧化产物;SiC中Si的化合价为+4价,则C的化合价为-4价,C元素的化合价由0价降至SiC中的-4价,SiC为还原产物。C既是氧化剂又是还原剂,氧化剂与还原剂物质的量之比为1:2。
(3)H++OH-=H2O代表强酸溶液与强碱溶液生成可溶性盐的中和反应,对应的化学方程式为2HCl+Ba(OH)2=BaCl2+2H2O。
(4)NaHSO4属于强酸的酸式盐,熔融时的电离方程式为NaHSO4=Na++HSO4-。


科目:高中化学 来源: 题型:
【题目】放热反应CO(g)+H2O(g) ![]() CO2(g)+H2(g)在温度t1时达到平衡,平衡时C1(CO)=C1(H2O)=1.0 mol/L,其平衡常数为K1。升高反应体系的温度至t2时,反应物的平衡浓度分别为C2(CO)和C2(H2O),平衡常数为K2,则
CO2(g)+H2(g)在温度t1时达到平衡,平衡时C1(CO)=C1(H2O)=1.0 mol/L,其平衡常数为K1。升高反应体系的温度至t2时,反应物的平衡浓度分别为C2(CO)和C2(H2O),平衡常数为K2,则
A. K1和K2的单位均为mol/L B. K1 < K2
C. C2(CO) = C2(H2O) D. C1(CO) > C2(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述不符合生产实际的是( )
A.电解熔融的氯化钠制取金属钠,用铁作阳极
B.电解法精炼粗铜,用纯铜作阴极
C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极
D.在锌锰干电池中,用锌作负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述错误的是( )
A. 17gH2O2所含非极性键数目为0.5NA
B. 标准状况下,H2和CO混合气体8.96L在足量O2中充分燃烧消耗O2分子数为0.2NA
C. n(H2CO3)和n(HCO3-)之和为1mol的NaHCO3溶液中,含有Na+数目为NA
D. 100gCaS和CaSO4的混合物中含有32g硫,则含有的氧原子数为1.75NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在湿法炼锌的电解循环溶液中,较高浓度的![]() 会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去
会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去![]() 。根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是
。根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是

A. ![]() 的数量级为
的数量级为![]()
B. 除![]() 反应为Cu+Cu2++2
反应为Cu+Cu2++2![]() =2CuCl
=2CuCl
C. 加入Cu越多,Cu+浓度越高,除![]() 效果越好
效果越好
D. 2Cu+=Cu2++Cu平衡常数很大,反应趋于完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球。关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应开始时,A、B的体积相同。已知:2NO2(g)![]() N2O4(g)△H<0。
N2O4(g)△H<0。
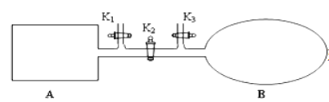
(1) 一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是v(A)______________v(B) (填“<”、“>”或“=”);若打开活塞K2,气球B将______________(填“变大”、“变小”或“不变”,下同)。
(2)若在A、B中再充入与初始量相等的NO2,则达到平衡时,NO2的转化率α(A)将______________ 。若通入等量的Ne气,则达到平衡时,A中NO2的转化率将______________,B中NO2的转化率将______________。
(3)若在容器A中充入4.6g的NO2,达到平衡后容器内混合气体的压强为原来的80%,试求出平衡时NO2的转化率______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NOx(主要指NO和NO2)是大气主要污染物之一。有效去除大气中的NOx是环境保护的重要课题。
(1)用水吸收NOx的相关热化学方程式如下:
2NO2(g)+H2O(l)![]() HNO3(aq)+HNO2(aq) ΔH=116.1 kJ·mol1
HNO3(aq)+HNO2(aq) ΔH=116.1 kJ·mol1
3HNO2(aq)![]() HNO3(aq)+2NO(g)+H2O(l) ΔH=75.9 kJ·mol1
HNO3(aq)+2NO(g)+H2O(l) ΔH=75.9 kJ·mol1
反应3NO2(g)+H2O(l)![]() 2HNO3(aq)+NO(g)的ΔH=___________kJ·mol1。
2HNO3(aq)+NO(g)的ΔH=___________kJ·mol1。
(2)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。现将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应。

反应相同时间NOx的去除率随反应温度的变化曲线如图所示,在50~250 ℃范围内随着温度的升高,NOx的去除率先迅速上升后上升缓慢的主要原因是______________________ ;
当反应温度高于380 ℃时,NOx的去除率迅速下降的原因可能是___________________ 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是
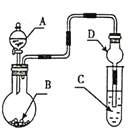
A. 若A为浓盐酸,B为KMnO4晶体,C中盛有紫色石蕊溶液,则C中溶液最终呈红色
B. 实验仪器D可以起到防止溶液倒吸的作用
C. 若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,则C中溶液中先产生白色沉淀,然后沉淀又溶解
D. 若A为浓H2SO4,B为Cu,C中盛有澄清石灰水,则C中溶液变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
X | Y | |
Z | W |
请回答下列问题:
(1)元素Z位于周期表中第_______周期,_______族;
(2)这些元素的氢化物中,水溶液碱性最强的是_____________(写化学式);
(3)XW2的电子式为________________________;
(4)Y的最高价氧化物的化学式为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com