

| ||
| 5.6L |
| 22.4L/mol |
| 5.6L |
| 22.4L/mol |
| 0.25mol |
| 0.25L |


科目:高中化学 来源: 题型:
(分)膜技术原理在化工生产中有着广泛的应用。有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5,装置图如下。
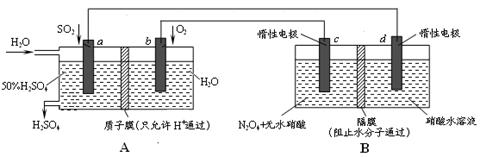
⑴A装置是________,B装置是_________(填“原电池”或“电解池”)。
⑵N2O5在电解池的______区生成,其电极反应式为_____________________________。
⑶通入O2一极的电极反应式为_______________________________。
⑷若通入SO2的速率为2.24 L·min-1(标准状况),为稳定持续生产,硫酸溶液的浓度应维持不变,则左侧水的流入速率应为_________mL·min-1。
查看答案和解析>>
科目:高中化学 来源:2013届湖南省师大附中高三第五次月考化学试卷(带解析) 题型:填空题
(11分)Ⅰ:在H2O2作用下可实现Fe(CN)63-与Fe(CN)64-之间的相互转化,在酸性溶液中H2O2可使Fe(CN)64-转化为Fe(CN)63-;在碱性溶液里H2O2可使Fe(CN)63-转化为Fe(CN)64-。写出以上相互转化的离子方程式。
① 酸性溶液中: ,
②碱性溶液中: 。
Ⅱ:膜技术原理在化工生产中有着广泛的应用。有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5,装置图如下。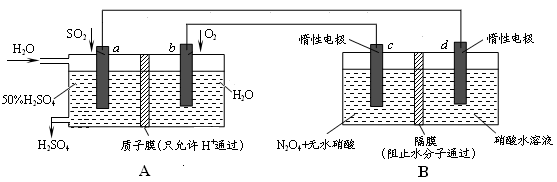
(3)A装置是________,B装置是_________(填“原电池”或“电解池”)。
(4)N2O5在装置中的______区(填“正、负极”或“阴、阳极”)生成,其电极反应式为______________。
(5)通入O2一极的电极反应式为_______________________________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年湖南省高三第五次月考化学试卷(解析版) 题型:填空题
(11分)Ⅰ:在H2O2作用下可实现Fe(CN)63-与Fe(CN)64-之间的相互转化,在酸性溶液中H2O2可使Fe(CN)64-转化为Fe(CN)63-;在碱性溶液里H2O2可使Fe(CN)63-转化为Fe(CN)64-。写出以上相互转化的离子方程式。
① 酸性溶液中: ,
②碱性溶液中: 。
Ⅱ:膜技术原理在化工生产中有着广泛的应用。有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5,装置图如下。

(3)A装置是________,B装置是_________(填“原电池”或“电解池”)。
(4)N2O5在装置中的______区(填“正、负极”或“阴、阳极”)生成,其电极反应式为______________。
(5)通入O2一极的电极反应式为_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com