
| A. | 从组成上来说,Na2SO4 是钠盐、硫酸盐、正盐 | |
| B. | 氧化物不是碱性氧化物就是酸性氧化物 | |
| C. | 非金属氧化物一定是酸性氧化物 | |
| D. | 不含杂质的盐酸是纯净物 |
分析 对物质进行分类是研究物质的重要方法,常见的分类方法是按着物质的组成、结构和性质进行分类的.
A、根据硫酸钠的微粒构成判断;
B、氧化物分为碱性氧化物、酸性氧化物、两性氧化物;
C、CO、NO属于不成盐氧化物;
D、盐酸是氯化氢的水溶液,属于混合物.
解答 解:A、Na2SO4是钠盐,是硫酸盐,而且是正盐,是根据其组成来划分的,故A正确;
B、氧化物分为碱性氧化物、酸性氧化物、两性氧化物,氧化物不是碱性氧化物、酸性氧化物,还可以是两性氧化物,故B错误;
C、非金属氧化物不一定是酸性氧化物,如CO、NO属于不成盐氧化物,故C错误;
D、不含杂质的盐酸是混合物,故D错误.
故选A.
点评 本题考查学生物质的分类知识,注意知识的归纳和梳理是解题的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 6g SiO2晶体中含有0.4NA个Si-O键 | |
| B. | PH=12的Na2CO3中有0.01NA个水分子发生了电离 | |
| C. | 标况下,11.2LHF含有的HF分子数大于0.5NA | |
| D. | 把含1molFeCl3的饱和溶液滴入沸水煮沸至红褐色透明,停止加入后,小于1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该反应的热化学方程式为:3X(g)+Y(g)?4Z(g);△H>0 | |
| B. | 若其它条件不变,平衡后又加入一定量X,正速率增大、逆速率减小,X的转化率减小 | |
| C. | 达到平衡后,若其他条件不变,升高温度,平衡向逆反应方向移动 | |
| D. | 达到平衡后,若其他条件不变,减小容器体积,平衡不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
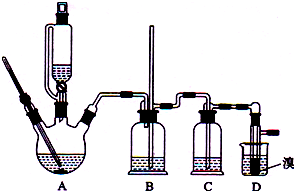
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .在工业上,用氯化钠为原料,在碱性溶液中,通过电解的方法可制得NaClO,用离子方程式表示制取NaClO的电解总反应:Cl-+H2O$\frac{\underline{\;通电\;}}{\;}$ ClO-+H2↑;.将等浓度等体积的NaClO与Na2SO3溶液混合后,两者恰好完全反应,写出混合过程的离子反应方程式ClO-+SO32-=Cl-+SO42-.
.在工业上,用氯化钠为原料,在碱性溶液中,通过电解的方法可制得NaClO,用离子方程式表示制取NaClO的电解总反应:Cl-+H2O$\frac{\underline{\;通电\;}}{\;}$ ClO-+H2↑;.将等浓度等体积的NaClO与Na2SO3溶液混合后,两者恰好完全反应,写出混合过程的离子反应方程式ClO-+SO32-=Cl-+SO42-.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com