
����Ŀ��I.��ͼ�Ǹ�����ij��ͯ��Ԫ����챨�浥�IJ������ݣ�
������ijҽ�ƻ����ٴ����������浥 | ||||
������Ŀ | ����� | ��λ | ����ֵ�ο���Χ | |
1 | �Zn�� | 109.62 | ��mol/L | 66-120 |
2 | ����Fe�� | 5.92�� | mmol/L | 7.52-11.82 |
3 | �ƣ�Ca�� | 1.68 | mmol/L | 1.55-2.10 |
���� | ||||
�����ϱ������ݣ��ش��������⣺
��1���ö�ͯ_____Ԫ�غ���ƫ�͡�
��2�����浥������mol/L����__________�������������������������Ũ�������ĵ�λ��
��3������ά����C��ʹʳ���е�Fe3+ת��ΪFe2+�����������������ά����C��________��������������������ԭ��������
II. ������أ�K2FeO4����Ԫ��Ϊ+6�ۣ���һ�����͡���Ч�������ɫˮ��������������Ⱦ���Ʊ�������ص����ӷ�Ӧ����ʽΪ��___Fe(OH)3+__ClO-+___OH- = ___FeO42-+___Cl-+ __H2O
�ش��������⣺
��4����ƽ�����ӷ���ʽ��
��5��ÿ����1molFeO42-ת�Ƶĵ�����Ϊ___________������Ӧ������ת����0.3mo1���ӣ���ԭ��������ʵ���Ϊ________mo1��
���𰸡�������Fe�� Ũ�� ��ԭ�� 2 3 4 2 3 5 3NA����1.806��1024 �� 0.15
��������
(1)������챨�浥��֪��(��Fe)Ԫ�غ���ƫ�ͣ�
��2����mol/L��Ũ�ȵĵ�λ��
��3������ά����C��ʹʳ���е�Fe3+ת��ΪFe2+��FeԪ�صĻ��ϼ۽��ͱ���ԭ��
��4����δ��ƽ��ѧ����ʽ��֪��Ӧ��ClԪ�صĻ����ϼ۽��ͣ�FeԪ�صĻ��ϼ����ߣ�Fe(OH)3Ϊ��ԭ����ClO-Ϊ���������ɵ����غ��ԭ���غ�ɵ���ƽ����ʽ��
��5������ƽ�Ļ�ѧ����ʽ����ɵá�
(1)������챨�浥����(��Fe)Ԫ�غ���ƫ�ͣ��ʴ�Ϊ��(��Fe)��
(2)���浥�Ц�mol/L��Ũ�ȵĵ�λ���ʴ�ΪŨ�ȣ�
��3������ά����C��ʹʳ���е�Fe3+ת��ΪFe2+��FeԪ�صĻ��ϼ۽��ͱ���ԭ����ά����C����ԭ���ã��ʴ�Ϊ��ԭ�ԣ�
��4����δ��ƽ��ѧ����ʽ��֪��Ӧ��ClԪ�صĻ����ϼ۽��ͣ�FeԪ�صĻ��ϼ����ߣ�Fe(OH)3Ϊ��ԭ����ClO-Ϊ���������ɵ����غ��ԭ���غ��֪���÷�ӦΪ2Fe��OH��3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O���ʴ�Ϊ2��3��4��2��3��5��
��5������ƽ�Ļ�ѧ����ʽ��֪������2molFeO42-����Ӧת�Ƶĵ�����Ϊ6mol������3mol Cl-����ÿ����1molFeO42-ת�Ƶĵ��ӵ����ʵ���Ϊ3mol����ĿΪ3NA����1.806��1024 ��������Ӧ������ת����0.3mo1���ӣ�������Cl-�����ʵ���Ϊ![]() =0.15mol���ʴ�Ϊ3NA����1.806��1024 ����0.15��
=0.15mol���ʴ�Ϊ3NA����1.806��1024 ����0.15��


 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƣ���ѧʽΪ NaNO2����һ�ֳ��õķ��������ش���������:
��1��NaNO2 �� N Ԫ�صĻ��ϼ�Ϊ_________.
��2������������ 320��C ʱ�ֽܷ���������ƹ��塢һ��������һ�ֳ�������ȼ�����塣�÷�Ӧ�Ļ�ѧ����ʽ_________________��
��3���ҹ��涨���ȳ��������������ӱ�Ϊÿǧ��ʳƷ���������� 150 ���ˣ��Դ˼��㣬200g 15��������������Һ���ٿ������������ȳ�______ǧ�ˡ�
��4�������������£�NaNO2�밴���ʵ��� 1:1 ǡ����ȫ��Ӧ����I��������Ϊ I2ʱ�������к���������Ϊ________���ѧʽ����
��5����ҵ��ˮ�е� NaNO2 �������۳�ȥ����֪����ϵ�а��� AI��NaAlO2��NaNO2��NaOH��NH3��H2O �������ʡ��÷�Ӧ�Ļ�ѧ����ʽΪ____________��
��6��ijͬѧ���ʵ��Թ�ҵ��Ʒ�� NaNO2 �ĺ������вⶨ����ȡ������Ʒ 2g����ȫ�ܽ����Ƴ���Һ 100mL ȡ�� 25mL ��Һ�� 0.100 mol/L ���� KMnO4 ��Һ���еζ������ʲ��� KMnO4 ��Ӧ����ʵ�������������±���ʾ:
����� | 1 | 2 | 3 | 4 |
����KMnO4��Һ���/mL | 20.70 | 20.02 | 20.00 | 19.98 |
����Ʒ���������Ƶ���������Ϊ_________.����֪:5NO2-+2MnO4-+6H+ = 5NO3-+2Mn2++3H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һ���ۺϴ���SO2�����Ĺ�������.����˵����ȷ����( )
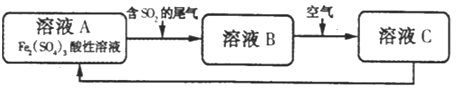
A����B��Һ�еμ�KSCN��Һ����Һ���ܱ�ΪѪ��ɫ
B����ҺBת��Ϊ��ҺC�����ı仯�����ӷ���ʽΪ4H+ + 2Fe2++O2=2Fe3++2H2O��
C����Һ����:A>B>C
D����������������ʹ��ҺCת��Ϊ��ҺA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.�����������Ȼ�����Һ�����ˮ�У�������У����Ƶ�Fe(OH)3���壬��Ӧ�ķ���ʽΪ��FeCl3 �� 3H2O ![]() Fe(OH)3(����) �� 3HCl
Fe(OH)3(����) �� 3HCl
��1������Һ��________ʱ��ֹͣ���ȣ����Ƶ�Fe(OH)3���塣
��2�����������������������������ı���������____________________��
��3�����������������________��
A�������ڽ��壬�ܲ��������ЧӦ
B������ɫ��������FeCl3��Һ��Fe(OH)3����
C�������������ھ�ˮ����ˮԭ���ͽ����й�
D������±�㶹���뽺�������й�
��.��A��B��C��D���ֿ������Σ����ǵ������ӷֱ���Ba2����Ag����Na����Cu2���е�ijһ�֣������ӷֱ���NO3����SO42����Cl����CO32���е�һ��(�����������в��ظ�����)��
�����������ηֱ�����ʢ������ˮ����֧�Թ��У�ֻ��C�ε���Һ����ɫ��
��������֧�Թ��зֱ�������ᣬB�ε���Һ�г������ɣ�D�ε���Һ����ɫ��ζ�������ݳ�����ش��������⣺
��4��A�Ļ�ѧʽΪ____________��B�Ļ�ѧʽΪ____________��
��5��д��D������CH3COOH��Һ��Ӧ�����ӷ���ʽ_____________________________��
��6��д��A��Һ�������ӵļ��鷽��______________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ĵ��ʼ�������������;�dz��㷺���ش��������⣺
(1)BF3�������л���Ӧ�Ĵ���������Bԭ�ӵ����Ų�ͼ��ʾ��״̬�У�������ͺ���ߵķֱ�Ϊ____________��_______________��(����)
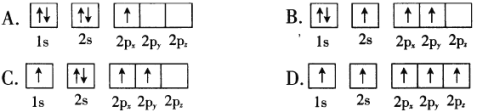
(2)NH4HF2(���⻯�)��̬ʱ��������������_______________(����)��
a.���Ӽ� b.![]() �� c.
�� c.![]() �� d.���
�� d.���
(3)�ɷ�Ӧ2F2+2NaOH��OF2+2NaF+H2O���Ʊ�OF2��OF2�Ŀռ乹��Ϊ___________����ԭ�ӵ��ӻ���ʽ��_____________________________
(4)CsF�����Ӿ��壬�侧���ܿ�ͨ��ͼ(a)��born��Haberѭ������õ���
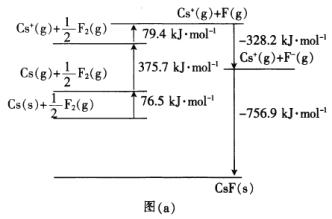
��ͼ��a����֪��Csԭ�ӵĵ�һ������Ϊ_______________________kJ��mol��1��F��F���ļ���Ϊ________kJ��mol��1��CsF�ľ�����Ϊ________kJ��mol��1��
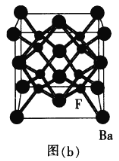
(5)BaF2������һ�����õ���˸����[��ͼ(b)��ʾ]��Ba2������λ��Ϊ_________������֪���ܶ�Ϊ![]() ����BaF2�ľ�������Ϊa=____________(��NAΪ�����ӵ���������ֵ���г�����ʽ) nm��
����BaF2�ľ�������Ϊa=____________(��NAΪ�����ӵ���������ֵ���г�����ʽ) nm��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��a��b��c��ʾ��Ӧ�����м�����Լ���������ͼװ����ȡ���������ռ���������(����)
��� | ���� | a | b | c |
|
A | NH3 | Ũ��ˮ | ��ʯ�� | ��ʯ�� | |
B | CO2 | ���� | ̼��� | ����NaHCO3��Һ | |
C | NO | ϡ���� | ͭм | H2O | |
D | NO2 | Ũ���� | ͭм | NaOH��Һ |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�ص��ʼ��仯�����й㷺��;����������ڱ��е�������Ԫ�����֪ʶ�ش��������⣺
(1)��ԭ������������˳��(ϡ���������)������˵����ȷ����_______��
a.���ʵ��۵㽵��
b.ԭ�Ӱ뾶�ͼ����Ӱ뾶����С
c.Ԫ�صĽ����Լ������ǽ�������ǿ
d.�������Ӧ��ˮ������Լ�����������ǿ
(2)�����������ļ���������_______�����ȶ��ԣ�H2O____H2S(��>��<��=)��
(3)д��SiCl4�ĵ���ʽ��________��
(4)��֪������M�ɵ������ڵ���������Ԫ�ذ�ԭ�Ӹ�����1:1��ɣ����ȶ�����ˮ��Ӧ����̸��ɫ����A��������ɫ�д�������ζ����B��C����Ӧ���ʵ�ת����ϵ��ͼ��

����֪M��Ħ������Ϊ135g/mol��д��M�Ļ�ѧʽ_____��
����ѡһ�ֺ��ʵ�������Y��д��C��Ũ��Һ��Y��Ӧ����D�����ӷ�Ӧ����ʽ_______��
��M�е�һ��Ԫ�ؿ��γɻ�����KXO3��������ʵ������O2�������Ӵ�����400��ʱKXO3�ֽ�ֻ���������Σ�����һ�����������Σ���һ���ε��������Ӹ�����Ϊ1��1��д���÷�Ӧ�Ļ�ѧ����ʽ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���һ��2L���ܱ������У�����4molA�� 2molB�������·�Ӧ��3A(g)��2B(g)![]() 4C(s)��2D(g)����Ӧһ��ʱ���ﵽƽ�⣬�������1.6molC��������˵����ȷ���ǣ� ��
4C(s)��2D(g)����Ӧһ��ʱ���ﵽƽ�⣬�������1.6molC��������˵����ȷ���ǣ� ��
A.�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ�� K=![]()
B.��ʱ��B��ƽ��ת������40%
C.�������ϵ��ѹǿ��ƽ�������ƶ�����ѧƽ�ⳣ������
D.���� B��ƽ�������ƶ���B��ƽ��ת��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڿ��淴Ӧ��2A(g)��3B(g)![]() xC(g)��D(g)�У���֪����ʼŨ��AΪ5mol/L��BΪ3mol/L��C�ķ�Ӧ����Ϊ0.5mol/(L��min)��2min���D��Ũ��Ϊ0.5mol/L������ڴ˷�Ӧ������˵����ȷ����(����)
xC(g)��D(g)�У���֪����ʼŨ��AΪ5mol/L��BΪ3mol/L��C�ķ�Ӧ����Ϊ0.5mol/(L��min)��2min���D��Ũ��Ϊ0.5mol/L������ڴ˷�Ӧ������˵����ȷ����(����)
A. 2minĩʱA��B��Ũ��֮��Ϊ5��3
B. x��1
C. 2minĩʱB��Ũ��Ϊ1.5mol/L
D. 2minĩʱA������Ũ��Ϊ0.5mol/L
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com