
����Ŀ��ij��Һ�п��ܺ�������5�������е�ij���֣�Na+��NH4+��Mg2+��Al3+��Cl����Ϊȷ�ϸ���Һ��ɽ�������ʵ�飺��ȡ20.0mL����Һ������25.0mL 4.00molL-1NaOH��Һ���а�ɫ���������ݼ���ζ�������ɣ����ˡ�ϴ�ӡ�����ó���1.16g���ٽ���Һϡ����100mL�������Һ��c(OH��)Ϊ0.20molL-1������ȡ20.0mL����Һ������������AgNO3��Һ�����ɰ�ɫ����11.48g���ɴ˿ɵó�����ԭ��Һ��ɵ���ȷ������
A��һ������Mg2+��Al3+��Cl��������Na+��NH4+
B��һ������Na+��Mg2+��Cl��������NH4+�����ܺ���Al3+
C��c(Cl��)Ϊ 4.00molL-1��c(Al3+)Ϊ1.00 molL-1
D��c(Mg2+)Ϊ 1.00molL-1��c(Na+)Ϊ 0.50 molL-1
���𰸡�D
��������
�����������25.0mL 4.00molL-1NaOH��Һ������0.1mol�������ƣ�����1.16gΪ������þ�����ʵ�����0.02mol�����ɳ�������0.04mol�������ƣ���Һ�е�n(OH-)=0.2molL-1��0.1L=0.02mol���ʻ���0.04mol�������ƺ�0.01molAl3+��Ӧ������ƫ�����ƣ���һ������Mg2+��Al3+���̼���ζ�������ɣ�һ��û��NH4+������ɫ����11.48g���Ȼ��������ʵ����ǣ�![]() =0.08mol����һ�����������ӣ����ݵ���غ㣬������У�(0.02mol��2+0.01mol��3)=0.07mol��������У�0.08mol����һ������������0.01mol��A���������Ϸ�����֪����Һ��һ�����ڣ�Na+��Mg2+��Al3+��Cl-������һ������Na+����A����B����Һ��һ�����ڣ�Na+��Mg2+��Al3+��Cl-����һ������Al3+����B����C��c(Al3+)=
=0.08mol����һ�����������ӣ����ݵ���غ㣬������У�(0.02mol��2+0.01mol��3)=0.07mol��������У�0.08mol����һ������������0.01mol��A���������Ϸ�����֪����Һ��һ�����ڣ�Na+��Mg2+��Al3+��Cl-������һ������Na+����A����B����Һ��һ�����ڣ�Na+��Mg2+��Al3+��Cl-����һ������Al3+����B����C��c(Al3+)=![]() =0.5 molL-1��c(Cl-)=
=0.5 molL-1��c(Cl-)=![]() =4mol/L����C����D��c(Mg2+)=
=4mol/L����C����D��c(Mg2+)=![]() =1.00 molL-1��c(Na+) =
=1.00 molL-1��c(Na+) =![]() =0.50 molL-1����D��ȷ����ѡD��
=0.50 molL-1����D��ȷ����ѡD��


 ��һ������ĩ�ٷֳ�̾�ϵ�д�
��һ������ĩ�ٷֳ�̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ȷ����(����)
A. ʯӢ��������������Ʒ
B. �赥�ʿ���������̫���ܵ��
C. �赥�������첣������Ҫԭ��
D. �����������������IJ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݹ����ð�ͭ�����ʳз������з�˼�������Ҫ�ɷ���ͭ���Ͻ�Ni����CO�γ����������ε������Ni(CO)4��CuSO4���ڰ�ˮ�γ�[Cu(NH3)4]SO4����ɫ��Һ��
��1��Cu��̬ԭ�Ӻ�������Ų�ʽΪ________________��
��2��1 mol Ni(CO)4�к�����������ĿΪ_______________��
��3��[Cu(NH3)4]SO4�������ӵĿռ乹����___________����SO42-��Ϊ�ȵ�����ķ���Ϊ_______________�����ѧʽ��
��4�� NH3�ķе�_______________����ѡ����ڡ����ڡ���PH3��ԭ����_______________��
��5��ij��ͭ�Ͻ��ṹ����ͼ��ʾ.������ͭԭ������ԭ�ӵĸ�����Ϊ_______________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��80��ʱ��NO2(g)+SO2(g)![]() SO3(g)+ NO (g)�����¶��£��ڼס��ҡ��������������Һ��ݵ��ܱ������У�Ͷ��NO2��SO2����ʼŨ�����±���ʾ�����м�2min��ƽ��ʱ��NO2��ת����Ϊ50%������˵����ȷ����
SO3(g)+ NO (g)�����¶��£��ڼס��ҡ��������������Һ��ݵ��ܱ������У�Ͷ��NO2��SO2����ʼŨ�����±���ʾ�����м�2min��ƽ��ʱ��NO2��ת����Ϊ50%������˵����ȷ����
��ʼŨ�� | �� | �� | �� |
c(NO2)/mol L-1 | 0.10 | 0.20 | 0.20 |
C(SO2)/ mol L-1 | 0.10 | 0.10 | 0.20 |
A. �������еķ�Ӧ��ǰ2 min��ƽ������v(SO2)=0.05 mol L-1 min-1
B. �ﵽƽ��ʱ��������������Ӧ���������������
C. �¶�����90����������Ӧƽ�ⳣ��Ϊ1.56����Ӧ����H>0
D. ������������ʼʱ�ij�0.10 molL-1 NO2��0.20molL-1 SO2���ﵽƽ��ʱc(NO)��ԭƽ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������أ�����˵��������ǣ�
A. ��ά���������ڲ���ˮ��������ǣ�������Ϊ�����Ӫ�����ʣ���������������
B. ����������ɱ��ù����ϸ����������ʳ��ɹ��ķ�����
C. ȼú�м���CaO���Լ���������γɼ�����������ŷ�
D. ���������߲˱�����߲˸������ڻ�ȡά����C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йس��и�����ȾԴ������ɵĶ����Ӧ��ȷ����( )
A.����β�������⻯ѧ���� ��ҵ������������ ��ҵ��ˮ��������������
B.����β���������� ��ҵ������������������ ��ҵ��ˮ�����⻯ѧ����
C.����β���������������� ��ҵ������������ ��ҵ��ˮ�����⻯ѧ����
D.����β�������⻯ѧ���� ��ҵ������������������ ��ҵ��ˮ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E�Ǻ˵����������������ֶ���������Ԫ�أ�AԪ�ص�ԭ�Ӻ���ֻ��1�����ӣ�BԪ�ص�ԭ�Ӱ뾶����������������С�ģ�B������������Ӧˮ����Ļ�ѧʽΪHBO3��CԪ��ԭ�ӵ������������ȴ�����4��C����������D�������Ӿ�����ͬ�ĵ����Ų�����Ԫ�ؿ��γɻ�����D2C��C��Eͬ���塣
(1)B�����ڱ��е�λ��Ϊ��______���ڵ�_______�塣
(2)EԪ���γɵ��������Ӧ��ˮ����Ļ�ѧʽΪ______��
(3)Ԫ��B��C��D��E�γɵļ����Ӱ뾶��С��ϵ��_________���������ӷ��ű�ʾ����
(4)�õ���ʽ��ʾ������D2C���γɹ��̣�_________��
(5)��A��B��C����Ԫ���γɵ����ӻ�����Ļ�ѧʽΪ_________������ǿ����Һ���ȣ�������Ӧ�����ӷ���ʽ��_________��
(6) D2EC3һ�������¿��Է����ֽⷴӦ���������Σ�����һ�ֲ���Ϊ�������Σ���˷�Ӧ�Ļ�ѧ����ʽΪ
_________������ѧʽ�þ����Ԫ�ط��ű�ʾ����
(7)E��ij���������Ǵ�����Ⱦ��֮һ��Ҳ��ij��ҵ�����е���Ҫβ��֮һ��ijУ��ȤС�����������з����ⶨ�˹�ҵβ���е�E��������ĺ�����
 ͨ����β�����ΪVL���ѻ���ɱ�״����ʱ����β����E�������ﺬ�������������Ϊ_______���ú���V��m�Ĵ���ʽ��ʾ����
ͨ����β�����ΪVL���ѻ���ɱ�״����ʱ����β����E�������ﺬ�������������Ϊ_______���ú���V��m�Ĵ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֡�

��֪A��B��C��D��E��X��Y���ɱ��и���Ԫ����ɵij������ʻ����������ͼ��ʾ��ת����ϵ(����������ͷ�Ӧ��������ȥ)��
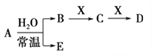
��1��Ԫ�آ������������Ӧˮ����Ļ�ѧʽ��_________________________��
��2��Ԫ�آ���As����Ԫ���У�����̬�⻯����ȶ�����___________���ѧʽ����
��3��Ԫ�آڢޢߵļ����Ӱ뾶�ɴ�С��˳����___________���û�ѧ���ű�ʾ����
��4��Ԫ�آ۵ĵ�����Ԫ�آڵ�����������Ӧ��ˮ���ﷴӦ�����ӷ���ʽ��________________��
��5����AΪ����ɫ���壬��X��D�Ļ�ѧʽ�ֱ�Ϊ___________��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ҫ�Ľ���������������(��Ҫ�ɷ���Al2O3��������SiO2��Fe2O3����)�ǹ�ҵ����ȡ����ԭ�ϡ�ʵ����ģ�ҵ����������Ϊԭ����ȡAl2(SO4)3�����������[NH4Al(SO4)2��12H2O]�Ĺ���������ͼ��ʾ��
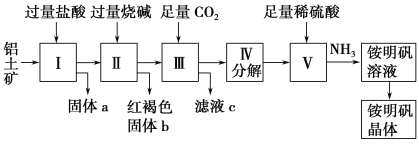
��ش��������⣺
(1)����a�Ļ�ѧʽΪ ������ͨ������CO2���巢����Ӧ�����ӷ���ʽΪ ��
(2)������ȡ�������Һ�Ļ�ѧ����ʽΪ �����������Һ�л������������ʵ���������Ϊ(���������) ����ȴ�ᾧ������ϴ�ӡ�
(3)��1 000 kg��������36%��������Ϊԭ����ȡAl2(SO4)3����������������98%������(�ܶ�1.84 g��cm��1 L(����һλС��)��
(4)��ͬʱ��ȡ���������������ͨ����������������������ֲ�Ʒ�IJ���������ʹ�Ƶõ�������������������ʵ���֮��Ϊ1��1����Ͷ��ʱ�������е�Al2O3��H2SO4�����ʵ���֮��Ϊ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com