
【题目】A~H等八种物质存在如下转化关系(反应条件、部分产物未标出).已知:A为正盐,B是能使品红溶液褪色的气体,E是碱性气体,G是红棕色气体.按要求回答问题: 
(1)写出下列物质的化学式:
B , D , E , F .
(2)设计实验检验A溶液中的阳离子,写出实验操作、现象和结论. .
【答案】
(1)SO2;H2SO4;NH3;NO
(2)取少量溶液于试管中,向其中加入加入浓NaOH溶液并加热,若产生能使湿润的红色石蕊试纸变蓝的气体,则证明有NH4+ , 否则没有
【解析】解:(1)G是红棕色气体,则G是NO2 , F和氧气反应生成二氧化氮,所以F是NO;A是正盐,和氢氧化钠反应生成E,E和氧气反应生成NO,则E是NH3 , A是铵盐;二氧化氮和水反应后能生成H,是和水反应生成硝酸和NO,所以H是硝酸;B能使品红溶液褪色,且B能和氧气反应生成C,所以B是SO2 , C是SO3 , 三氧化硫和水反应生成D为H2SO4 , A是正盐且是铵盐,反应后能生成二氧化硫,所以A是(NH4)2SO3 .
所以答案是:SO2;H2SO4;NH3;NO;(2)A中阳离子为NH4+ , 检验NH4+离子方法是:取少量该溶液于试管中,加入氢氧化钠溶液,加热,如果生成的气体能使湿润的红色石蕊试纸变蓝色,则证明有NH4+ , 所以答案是:取少量溶液于试管中,向其中加入加入浓NaOH溶液并加热,若产生能使湿润的红色石蕊试纸变蓝的气体,则证明有NH4+ , 否则没有.


科目:高中化学 来源: 题型:
【题目】下面关于化学反应的限度的叙述中,正确的是
A. 化学反应的限度都相同
B. 可以通过改变温度控制化学反应的限度
C. 可以通过延长化学反应的时间改变化学反应的限度
D. 当一个化学反应在一定条件下达到限度时,反应即停止
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃的混合物共1L,在空气中完全燃烧得到1.5L CO2和2L水蒸气(体积均在同温同压下测定),关于此混合烃的判断正确的是( )
A.肯定是甲烷和乙烯的混合物
B.一定不是甲烷和乙烯的混合物
C.一定含乙烯,不含甲烷
D.两种烃分子中氢原子数都是4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含H+、SO42﹣、NO3﹣三种离子,其中H+、SO42﹣的物质的量浓度分别为7.0molL﹣1和2.0molL﹣1 . 取该溶液20mL,加入3.2g铜粉,加热使它们充分反应,产生的气体在标准状况下的体积约为( )
A.0.75 L
B.0.336 L
C.1.5 L
D.0.448 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“一碳化学”是指以含一个碳原子的化合物(如:CO2、CO、CH4、CH3OH等)为初始反应物,合成一系列重要的化工原料和燃料的化学。
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应I:2NH3(g)+CO2(g)=NH2COONH4(s)△H1
反应II:NH2COONH4(s)=CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol
总反应:2NH3(g)+CO2(g)==CO(NH2)2(s)+H2O(g) △H3=-86.98kJ/mol
请回答下列问题:
①反应I的△H1=______ kJ/mol
②反应II一般在_________(填“高温”或“低温”)情况下有利于该反应的进行。
③一定温度下,在体积为固定的密闭容器中按计量比进行反应I,下列能说明反应达到了平衡状态的是__________(填序号)。
A.混合气体的平均相对分子质量不再变化 B.容器内气体总压强不再变化
C.2V正(NH3)=V逆(CO2) D.容器内混合气体的密度不再变化
④环境为真空时,在一敞开容器(非密闭容器)中加入NH2COONH4固体,足够长时间后,反应是否建立平衡状态? ___________(填“是”或“否”)
(2)将CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。测得CH3OH的物质的量随时间的变化如下图。
CH3OH(g)+H2O(g)。测得CH3OH的物质的量随时间的变化如下图。
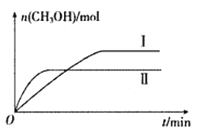
①曲线I.II对应的平衡常数大小关系为KI_______KII(填“ >”、“<”或“=”)。
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容器 | 甲 | 乙 |
反应物投入量 | 1molCO2、3molH2 | amolCO2、bmolH2 cmol CH3OH(g)、cmolH2O(g)(a、b、c均不为零) |
若甲容器平衡后气体的压强为开始的0.8倍,则甲容器平衡混合气体中CH3OH(g)的体积分数为_______,要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,乙容器中c的取值范围为________。
(3)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如下图,乙酸的生成速率主要取决于温度影响的范围是________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分
A | |||||||||||||||||
B | C | D | E | F | |||||||||||||
H | I | J | K | ||||||||||||||
L | M | O |
(1)元素L的价电子排布图为__________,元素M的原子结构示意图为________,位于元素周期表五个区域中的_______区。上述元素中电负性最强的是_______(用元素符号表示),C、D、E、F第一电离能的大小顺序为____________(用元素符号表示)。
(2)D的氢化物和J氢化物沸点较高的是______(填化学式),稳定性更强的是______(填化学式)。
(3)某些不同族元素的性质也有一定的相似性,如上表中元素I与元素B的单质有相似的性质。写出元素单质B与NaOH溶液反应的离子方程式___________________________。
(4)A、E、H、J四种元素的原子半径由大到小的排列顺序为___________________;E、F、H、K四种元素简单离子的半径由大到小的排列顺序为________________用元素符号表示)。
(5)能证明元素K比元素J的非金属性强的事实是______________(填序号)。
A.常温下K单质的密度小于J单质的密度
B.K元素的气态氢化物比J元素的气态氢化物更稳定
C.K单质与氢气反应的程度比J单质与氢气反应的程度更剧烈
D.K元素的氧化物对应的水化物酸性强于J元素的氧化物对应的水化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中NO3-的物质的量浓度最大的是
A.500 mL 1 mol/L的KNO3溶液B.500 mL1 mol/L的Ba(NO3)2溶液
C.1000 mL 0.5 mol/L的Mg(NO3)2溶液D.1 L 0.5 mol/L的Fe(NO3)3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com