
【题目】广东是滨海砂矿储量最大的省份,滨海砂矿中含有丰富的石英砂(主要成分为SiO2)。关于SiO2的说法正确的是( )
A. 能与水反应 B. 硬度小,熔点低
C. 能与盐酸反应 D. 能与NaOH溶液反应
科目:高中化学 来源: 题型:
【题目】某合金(仅含铜、铁)中铜和铁的物质的量之和为y mol,其中Cu的物质的量分数为a,将其全部投入50 mL b mo1·L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。下列说法正确的是 ( )
A. 若金属有剩余,在溶液中再滴入硫酸后,金属不会再溶解
B. 若金属全部溶解,则溶液中一定含有Fe3+
C. 若金属全部溶解,且产生336 mL气体(标准状况),则b=0.3
D. 当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80 y (1—a/3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程涉及化学变化的是( )
A. 将I2溶于酒精制备碘酊
B. 将NaCl溶于水中制备生理盐水
C. 被果汁沾污的衣服浸入漂白液中清洗
D. 用激光笔照射鸡蛋清溶液产生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由单质A与化合物B两种粉末组成的混合物, 在一定条件下可按下图所示发生转化:

请回答:
(1)A的化学式__________________,B的名称______________________;
(2)反应①的化学方程式________________________________________;
(3)反应②的离子方程式________________________________________;
(4)反应③的离子方程式________________________________________;
(5)反应④的离子方程式________________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法正确的是( )

A. 该混合气体中一定含有乙烯
B. 该混合气体一定含有甲烷和乙炔
C. 在110℃条件下,混合气体与氧气混合,总混合气燃烧前后体积不变
D. 若混合气体由CH4和C2H4组成,则其体积比为1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应I2(g)+H2(g)=2HI(g),在密闭容器中进行,下列哪些条件能加快该反应的速率
A.缩小体积,使压强增大B.体积不变,充入H2使压强增大
C.体积不变,充入He使压强增大D.压强不变,充入He使体积增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W的原子序数依次增大。在下图所示物质转化关系中,b是Y元素的单质,其余为由上述的两种或三种元素组成的化合物。常温时,0.1mol·L-1的a溶液的pH为1, d为红棕色气体,e为无色气体。下列说法正确的是

A. 元素的非金属性:Y>Z>X
B. 反应①中消耗lmola时转移电子数与反应②中生成1mol a时转移电子数相等
C. 原子半径的大小:Y<Z<W
D. Y的氢化物常温常压下为气态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用含锰废料(主要成分MnO2,含有少量Fe2O3、Al2O3、CuO、CaO等)与烟气脱硫进行联合处理并制备MnSO4的流程如下:

已知:25℃时,部分氢氧化物的溶度积常数(Ksp)如下表所示。
氢氧化物 | Al(OH)3 | Fe(OH)3 | Cu(OH)2 | Mn(OH)2 |
Ksp | 1.0×10-33 | 4.0×10-38 | 2.0×10-20 | 4.0×10-14 |
请回答:
(1)沉淀1的化学式为__________________。
(2)(NH4)2S的电子式为________________;“净化”时,加入(NH4)2S的作用为___________________。
(3)“酸化、还原”中,发生的所有氧化还原反应的离子方程式为__________________。
(4)已知:滤液3中除MnSO4外,还含有少量(NH4)2SO4。(NH4)2SO4、MnSO4的溶解度曲线如下图所示。
据此判断,操作“I”应为蒸发浓缩、____________、洗涤、干燥。

(5)工业上可用电解酸性MnSO4溶液的方法制备MnO2,其阳极反应式为________________。
(6)25.35 g MnSO4·H2O样品受热分解过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
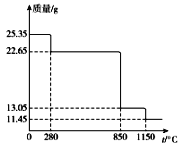
①300℃时,所得固体的化学式为______________________。
②1150℃时,反应的化学方程式为___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com