
【题目】关于下列各装置图的叙述中,不正确的是 ( )
A.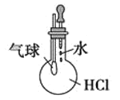 可验证HCl气体在水中的溶解性
可验证HCl气体在水中的溶解性
B.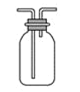 可用于收集H2、NH3、Cl2、HCl、NO2、NO等
可用于收集H2、NH3、Cl2、HCl、NO2、NO等
C.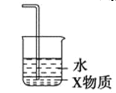 中X为四氯化碳,可用于氨气或氯化氢的尾气处理
中X为四氯化碳,可用于氨气或氯化氢的尾气处理
D. 可用于干燥、收集氨气,并吸收多余的氨气
可用于干燥、收集氨气,并吸收多余的氨气
科目:高中化学 来源: 题型:
【题目】实验室有一未知浓度的盐酸,某同学在实验室中进行实验测定盐酸的浓度。请完成下列填空:
配制100mL0.10molL-1NaOH标准溶液。需用托盘天平称量___g的氢氧化钠固体。
取20.00mL待测盐酸放入锥形瓶中,并滴加 2~3滴酚酞作指示剂,用配制的标准 NaOH溶液进行滴定。重复上述滴定操作 2~3次,记录数据如下:
滴定次数 | 待测盐酸的体积/mL | 0.10 mol/L NaOH 溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
第一次 | 20.00 | 2.00 | 28.15 |
第二次 | 20.00 | 1.50 | 29.50 |
第三次 | 20.00 | 0.20 | 26.55 |
①该实验滴定达到终点的标志是_________
②根据上述数据,可计算出该盐酸的浓度约为______。(保留两位有效数字)
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_______。(双选)
A 滴定终点读数时俯视读数 B 酸式滴定管使用前,水洗后未用待测盐酸润洗
C 锥形瓶水洗后未干燥 D 碱式滴定管尖嘴部分有气泡,滴定后消失
E 称量NaOH 固体时,混入少量KOH杂质
④现用以上实验配制的0.10molL-1NaOH溶液滴定未知浓度的CHCOOH溶液,反应恰好完全时,下列叙述中正确的是_____
A 溶液呈中性,可选用甲基橙或酚酞作指示剂
B 溶液呈中性,只能选用石蕊作指示剂
C 溶液呈碱性,可选用甲基橙或酚酞作指示剂
D 溶液呈碱性,只能选用酚酞作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列水解方程式的书写不正确的是( )
A.NH4++H2O![]() NH3·H2O+H+
NH3·H2O+H+
B.S2-+2H2O![]() H2S+2OH-
H2S+2OH-
C.CH3COONa+H2O![]() CH3COOH+NaOH
CH3COOH+NaOH
D.MgCO3 + H2O![]() Mg(OH)2 + CO2
Mg(OH)2 + CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向2 L恒容密闭容器中充入1 mol A,发生A(g)![]() B(g) + C(g)反应。反应过程中c(C) 随时间变化的曲线如下图所示,下列说法不正确的是
B(g) + C(g)反应。反应过程中c(C) 随时间变化的曲线如下图所示,下列说法不正确的是

A.反应在0 ~50 s的平均速率v(C) =1.6×10-3mol/(L·s)
B.该温度下,反应的平衡常数K = 0.025
C.保持其他条件不变,升高温度,平衡时c(B)=0.11mol/L,则该反应的ΔH<0
D.反应达平衡后,再向容器中充入1 mol A,该温度下再达到平衡时,0.1 mol/L<c(C)<0.2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组利用下图装置制取少量氯化铝,已知氯化铝熔沸点都很低(178℃升华),且易水解。下列说法中完全正确的一组是
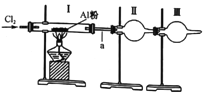
①氯气中含的水蒸气和氯化氢可通过盛有苛性钠的干燥管除去
②装置I中充满黄绿色气体后,再加热盛有A铝粉的硬质玻璃管
③装置II是收集装置,用于收集氯化铝
④装置III可盛放碱石灰也可盛放无水氯化钙,二者的作用相同
⑤a处使用较粗的导气管实验时更安全
A. ①② B. ②③⑤ C. ①④ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL混合液中,HNO3和H2SO4物质的量浓度分别是0.4mol/L和0.1mol/L,向该混合液中加入1.92gCu粉,加热充分反应后,所得溶液中Cu2+的物质的量浓度是( )
A.0.15 mol/LB.0.3 mol/LC.0.1 mol/LD.0.225 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学课上围绕浓硫酸的化学性质进行如下实验探究,将适量的蔗糖放入烧杯中,加几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质。请回答下列问题:
(1)生成的这种黑色物质(单质)是(填化学式)________。
(2)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的污染物之一,这种刺激性气味气体为(填化学式)___,反应的化学方程式为________。
(3)根据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有(填字母) _______。
A 酸性 B 吸水性 C 脱水性 D 强氧化性
(4)将(2)中产生的有刺激性气味的气体通入品红溶液中,探究SO2与品红作用的可逆性,请写出实验操作及现象______。;将(2)中产生的有刺激性气味的气体通入氯水中,发生反应的化学方程式为_______。
(5)工厂煤燃烧产生的烟气若直接排放到空气中,引发的主要环境问题有_____。
A 温室效应 B 酸雨 C 粉尘污染 D 水体富营养化
工业上为实现燃煤脱硫,常通过煅烧石灰石得到生石灰,以生石灰为脱硫剂,与烟气中SO2反应从而将硫固定,其产物可作建筑材料。写出其中将硫固定的化学方程式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2X(g)+Y(g)2Z(s) △H= -M kJ·mol-1。T℃,将2 mol X(g)和1 mol Y(g)加入体积为1L的恒容密闭容器中进行反应, 10 min后达到平衡,生成0.2 mol Z,共放出热量N kJ,下列说法不正确的是
A.其他条件不变,压缩容器,逆反应速率不变
B.在10 min内,X的反应速率为0.02 mol·L-1·min-l
C.在5 min末,X、Y的转化率不相等
D.在0~10 min内,Y的反应速率为![]() mol·L-1·min-l
mol·L-1·min-l
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正丁烷的二氯取代产物为A(C4H8Cl2),A分子中又有一个H原子被Cl原子取代,生成的C4H7Cl3有四种同分异构体,则A的结构有( )
A. 1种B. 2种C. 3种D. 4种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com