
【题目】请回答下列问题:
I.工业生产纯碱的工艺流程示意图如下:

(1)为除去粗盐水中的Mg2+、Ca2+、SO42-等杂质离子,加入试剂顺序合理的是________。
A.碳酸钠、氢氧化钠、氯化钡 B.碳酸钠、氯化钡、氢氧化钠
C.氢氧化钠、碳酸钠、氯化钡 D.氯化钡、氢氧化钠、碳酸钠
(2)工业生产纯碱工艺流程中,碳酸化时产生的现象是________________。
(3)碳酸化后过滤,滤液A最主要的成分是______________(填写化学式),检验这一成分的阴离子的具体方法是:________________________________。
(4)煅烧制取Na2CO3在_______(填字母序号)中进行。
a.瓷坩埚 b.蒸发皿 c.铁坩埚 d.氧化铝坩埚
II.纯碱在生产生活中有广泛的用途。
(5)工业上,可能用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与氯气反应可制得有效成分为次氯酸钠的消毒液,其反应的离子方程式为________________________。
(6)纯碱可制备重铬酸钠(Na2Cr2O7),铬铁矿中的1molCr2O3反应时需要通入标准状况下O2的体积为_________________________________。
【答案】 D 有晶体析出(或出现浑浊) NH4Cl 取样,加硝酸酸化,加硝酸银,有白色沉淀,该阴离子是氯离子 c 2CO32—+Cl2+H2O=2HCO3—+Cl—+ClO— 33.6L
【解析】(1)Ca2+用碳酸钠除去,Mg2+用氢氧化钠除去,SO42-用氯化钡除去,将生成的沉淀过滤后,向滤液中加入盐酸酸化即可实现除杂的目的。但由于过量的氯化钡要用碳酸钠来除,所以碳酸钠必需放在氯化钡的后面,而氢氧化钠可以随意调整,所以正确的顺序可以是氯化钡、氢氧化钠、碳酸钠,答案选D。(2)由于碳酸氢钠的溶解度较小,所以工业生产纯碱工艺流程中,碳酸化时产生的现象是有晶体析出(或出现浑浊)。(3)氨气、二氧化碳、氯化钠在溶液中生成碳酸氢钠和氯化铵,则酸化后过滤,滤液A最主要的成分是NH4Cl,检验氯离子的具体方法是取样,加硝酸酸化,加硝酸银,有白色沉淀,该阴离子是氯离子。(4)煅烧制取Na2CO3在坩埚中进行,由于高温下二氧化硅、氧化铝能与碳酸钠反应,所以应该用铁坩埚,答案选c。(5)由于次氯酸的酸性强于碳酸氢根离子,因此氯气与饱和纯碱溶液反应的离子方程式为2CO32-+Cl2+H2O=2HCO3-+Cl-+ClO-。(6)Cr元素化合价从+3价升高到+6价,失去3个电子,则1molCr2O3反应时失去6mol电子,根据电子得失守恒可知消耗氧气是6mol÷4=1.5mol,标准状况下O2的体积为1.5mol×22.4L/mol=33.6L。


科目:高中化学 来源: 题型:
【题目】已知A为金属单质,它们之间能发生如下反应(部分产物未标出)

请根据以上信息回答下列问题:
(1)写出物质B的化学式:___________
(2)写出下列反应的化学方程式:
反应①______________________________________________________________________
反应②______________________________________________________________________
(3)写出下列反应的离子方程式:
反应C→D______________________________________________________________________
反应D→C _____________________________________________________________________
(4)检验D中阳离子的方法: _________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是单质,其中A是金属,各种物质间的转化关系如图:
根据图示转化关系回答:
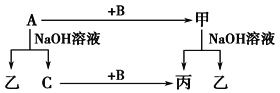
(1)写出下列物质的化学式。
A________,B________,甲_________,乙________。
(2)写出下列变化的化学方程式。
①A与NaOH溶液反应的化学方程式________________________________。
②甲与NaOH溶液反应的离子方程式________________________________。
(3)将一定量的A加入到NaOH溶液中,产生的C在标准状况下的体积为3.36 L,则消耗的A的物质的量为________,转移电子的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为V L的恒容密闭容器中盛有一定量H2 , 通入Br2(g)发生反应H2(g)+Br2(g)2HBr(g)△H<0.当温度分别为T1、T2 , 平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法正确的是( ) 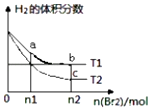
A.若b、c两点的平衡常数分别为K1、K2 , 则K1>K2
B.a、b两点的反应速率:b>a
C.为了提高Br2(g)的转化率可采取增加Br2(g)通入量的方法
D.b、c两点的HBr的体积分数b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.饮用水就是纯水,是纯净物
B.有机食品,就是有机合成的食品
C.将化工厂的烟囱建高,不能缓解大气污染
D.燃煤时,鼓入过量的空气可以减少酸雨的产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题
肼是一种高能燃料.已经各共价键键能(断裂或形成1mol共价键时吸收或释放的能量)如下:
N≡N | O=O | N﹣N | N﹣H | O﹣H | |
键能(KJmol﹣1) | 946 | 497 | 154 | 391 | 463 |
(1)N2H4(g)+O2(g)N2(g)+2H2O(l)△H=KJmol﹣1
(2)Ⅱ.密闭容器中进行反应:3Fe(s)+4H2O(g)Fe3O4(s)+4H2(g)△H<02反应的化学平衡表达式为K= .
(3)已知:600℃时,上述反应的平衡常数K=16.现有如图1甲(恒温恒压)和如图1乙(恒温恒容)两容器,起始时按下表所示分别加入各物质,体积为2L,在600℃时反应经过一段时间后均达平衡.
Fe | H2O(g) | Fe3O4 | H2 | |
甲/mol | 2.0 | 1.0 | 2.0 | 0.5 |
乙/mol | 2.0 | 2.0 | 2.0 | 1.0 |
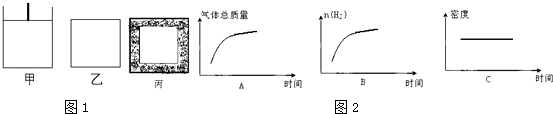
①关于甲、乙容器,下列说法正确的是
A.反应开始时两容器内的逆反应速率:甲<乙
B.若甲容器内气体的密度不再变化,则说明反应已达到平衡状态
C.若乙容器内气体的压强不再变化,则说明反应已达到平衡状态
D.平衡后添加Fe3O4 , 两容器内的平衡均逆向移动
②投料后甲5min达平衡,则此段时间内的平均反应速率v(H2)=
③平衡后若将乙容器体系温度突然降低100℃,如图2下述图象中能正确反映平衡移动过程中容器内变化情况的是 .
(4)为恒容绝热容器,进行上述反应,起始与平衡时的各物质的量见下表:
Fe | H2O(g) | Fe3O4 | H2 | |
起始/mol | 3.0 | 3.0 | 0 | 0 |
平衡/mol | m | n | p | q |
若在达到平衡后的容器丙中,分别按照下列A、B、C三种情况继续添加各物质,则再次达平衡时,容器丙中H2的百分含量按由大到小的顺序(用A、B、C表示).
Fe | H2O(g) | Fe3O4 | H2 | |
A/mol | 3.0 | 3.0 | 0 | 0 |
B/mol | 0 | 0 | 3.0 | 3.0 |
C/mol | m | n | p | q |
25℃时,Fe(OH)3的ksp=4ⅹ10﹣38 , 现有盐酸酸化的0.08mol/L的FeCl3溶液,其PH=1,向其中加入等体积的mol/L的NaOH溶液,可恰好开始析出沉淀(混合时溶液体积可直接加和).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是中学化学实验室的常见药品,回答下列实验问题。
Ⅰ.配制一定物质的量浓度的硫酸溶液:
(1)某次实验大约需要1mol/L硫酸溶液435ml。同学们发现实验室内没有450ml的容量瓶,某同学提议用1个200ml容量瓶和1个250ml容量瓶来配制,你认为该提议_________(填“合理”、“不合理”)。
(2)实验中要配制0.5mol/L H2SO4溶液250ml。则需量取密度为1.84g/ml、98%的浓硫酸________ml。

Ⅱ.蔗糖与浓硫酸的炭化实验会产生大量的有刺激性气味的气体,会对环境造成污染。某实验小组利用如下装置对该实验进行改进。回答下列问题:
注:硬质玻璃管中①、②、③处分别为滴有Na2S溶液的滤纸、滴有品红溶液的滤纸、滴有酸性KMnO4溶液的滤纸,a和b分别为两个小气球。
(1)图中盛装浓硫酸的仪器名称为________________。
(2)实验开始后先关闭活塞K,硬质玻璃管中①号试纸变黄,②号和③号滤纸均褪色,a处气球变大。硬质玻璃管中实验现象说明炭化实验产生的刺激性气味气体是SO2,①、②、③处发生的变化分别说明SO2具有_____________、_____________和_____________(填SO2表现出的性质)。
(3)打开活塞K,a处气球变小,b处气球变大。使三颈烧瓶内气体缓慢通过B瓶和C瓶,一段时间之后,发现澄清石灰水变浑浊。为证明有CO2生成,可以在④号位置的滤纸滴加______________溶液,该试剂的作用是_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列说法中正确的是( )
A.1 mol FeCl3跟水完全反应转化为氢氧化铁胶体后,其中胶体粒子的数目为NA
B.由2H和18O所组成的水11 g,其中所含的中子数为4NA
C.常温下丁烯和环丙烷组成的42 g混合气体中H原子数为6NA
D.1 mol FeI2与足量氯气反应时转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项有机化合物的命名或分类正确的是( )
A.2,3﹣二甲基﹣2﹣乙基己烷
B.CH3CH2CH2Cl 氯丙烷
C.![]() 属于芳香化合物
属于芳香化合物
D.![]() 属于羧酸
属于羧酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com