
【题目】下列晶体由原子直接构成,但属于分子晶体的是( )
A.固态氢 B.固态氖
C.磷 D.三氧化硫
科目:高中化学 来源: 题型:
【题目】如图所示,水槽中的试管内有一枚铁钉,放置数天观察:
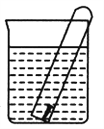
(1) 铁钉在逐渐生锈,铁钉的腐烛属于______________________腐蚀。
(2) 若试管内的液面下降,则原溶液呈________性,发生________腐蚀;电极反应为负极:______________________,正极:_________________。
(3)若试管内的液面上升,则原溶液呈________性,发生________腐蚀;负极反应式为_____________,正极反应式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)已知:CH3OH(g)=HCHO(g)+H2(g)△H=+84kJmol1
2H2(g)+O2(g)═2H2O(g)△H=484kJmol1
工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式: ________________________________
(2)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应CO(g)+2H2(g)CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。

①A,B两点对应的压强大小关系是PA________PB(填“>,<,=”)
②A,B,C三点的平衡常数KA,KB,KC的大小关系是 __________________
③下列叙述能说明上述反应能达到化学平衡状态的是___(填代号)
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.CO和CH3OH的物质的量之和保持不变
(3)在P1压强、T1°C时,该反应的平衡常数K=_________,再加入1.0molCO后重新到达平衡,则CO的转化率___________(填“增大,不变或减小”),CH3OH的体积分数_________(填“增大,不变或减小”)
(4)T1°C、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下:CO:0.1mol H2 :0.2mol CH3OH:0.2mol。
此时v正 ________ v逆(填> 、 < 或 =)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组模拟喷泉实验原理并探究NH3的有关性质。实验过程如下,如图所示,在干燥的圆底烧瓶里充满氨气,用带有玻璃管和滴管(滴管里预先吸入水)的塞子塞紧瓶口。倒置烧瓶,使玻璃管插入盛有水的烧杯中(预先在水里滴入少量酚酞溶液)。轻轻挤压滴管,使少量水进入烧瓶,打开活塞f。回答下列问题:
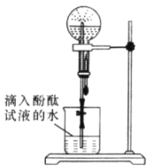
(1)本实验的现象是_________,本实验得到NH3的哪些性质_______
(2)下列可以产生类似现象的组合为____________
a(干燥气体) | b(液体) | ||
A | NO | 水 | |
B | CO2 | 4mol/LNaOH溶液 | |
C | Cl2 | 饱和NaCl溶液 | |
D | NH3 | 1mol/L盐酸 | |
(3)同温同压下,分别充满①NO2②NH3进行喷泉实验,经充分反应后,圆底烧瓶内溶液的物质的量浓度①_____②(填“<”“>”或“=”)
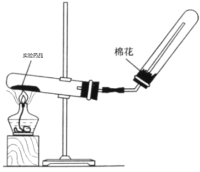
(4)实验室制备氨气的装置如图所示,反应方程式为____________________________,该装置_____(“能”或“不能”)用于加热碳酸氢铵固体来制备纯净的氨气,原因________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)营养平衡、科学使用食品添加剂有助于健康和提高免疫力。
①向食品中加入调味剂,能改善或改变食品的口味,下列不属于调味剂的_________________(填字母)。
a. 食盐 b. 辣椒粉 c. 小苏打
②人体如果缺乏某种微量元素将导致血液输送氧气的能力下降,人体内就无法获得充足的氧气,生理机能就会下降,儿童还可能会智力发育迟缓,该微量元素是_________________(填字母)。
a. 碘 b. 锌 c. 铁
③抗生素是能抑制某些微生物生长或能杀灭某些微生物的一类物质,下列属于抗生素的是____________________(填字母)
a. 阿莫西林 b. 胃舒平 c. 阿司匹林
④在酶的作用下,淀粉水解为葡萄糖,葡萄糖又在酶的作用下转化为乙醇和二氧化碳。写出葡萄糖转化为乙醇的化学方程式___________________________________________________。
(2)材料是人类文明的物质基础和先导,是直接推动社会发展的动力。
①下列材料中属于复合材料的是___________________(填字母)。
a.有机玻璃 b.玻璃钢 c.石英玻璃
②全世界每年都有大量的钢铁因生锈而损失,下列不能防止铁被腐蚀的是________________(填字母)。
a.在自行车车轮钢圈的表面镀一层铬
b.在轮船的外表焊一些铜块
c.汽车车身外壳喷涂油漆
③下列有机物属于天然高分子材料的是__________________(填字母)。
a.油脂 b.聚乙烯 c.纤维素
(3)促进生态文明,保护生态环境,是实现“中国梦”的重要组成部分。
①生活垃圾的成分多种多样,下列不属于可回收垃圾的是____________________(填字母)。
a.瓜皮果壳 b.废纸 c.塑料
②下列物质尚未列入我国空气质量报告的是_____________________(填字母)。
a.二氧化碳 b.二氧化硫 c.可吸入颗粒物
③煤燃烧产生的SO2所形成的酸雨中,SO2最终转化成的酸是______________________(填化学式)。在燃煤时加入适量石灰石,可以大大减少煤燃烧时SO2的排放,最终生成CaSO4,写出发生该反应的化学方程式____________________________________________________________。
④处理废水中重金属铊(Tl),需在废水中加入NaClO溶液,将Tl+转变为Tl3+,同时加入熟石灰,将Tl3+转变为难溶物________________________(填化学式),最后加入明矾沉降除去,明矾作_________________________剂。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示(部分物质和条件已略去)。A是由两种元素组成的难溶于水的物质,两种元素的质量比为7:4;B是强酸;C的摩尔质量为34g·mol-1; F是最常见的无色液体;无色气体G能使品红溶液褪色;向含有I的溶液中滴加KSCN溶液,溶液出现血红色。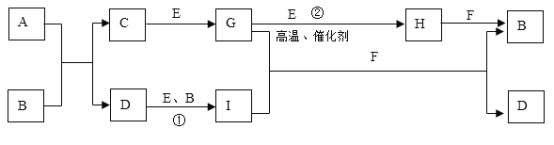
请回答下列问题:
(1)A的化学式____________________________。
(2)C的电子式____________________________。
(3)反应①的离子方程式_______________________________________________________。
(4)反应②的化学方程式_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向NaOH和Na2CO3混合溶液中滴加0.1mol/L稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示。下列判断正确的是( )

A. 在0-a范围内,只发生中和反应
B. ab段发生反应的离子方程式为:CO32-+2H+=H2O+CO2↑
C. a=0.3
D. 原混合溶液中NaOH与Na2CO3的物质的量之比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
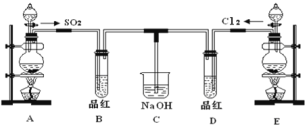
(1)实验室用装置E制备Cl2,其反应的离子方程式为__________________________;若有8mol的HCl参加反应,则转移的电子总数为________。
(2)该装置中氢氧化钠溶液的作用是___________________。
(3)通气后B、D两个试管中的现象______________。停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:________,D:________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用离子方程式表示)____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com