
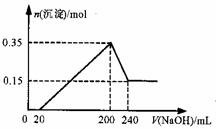
 将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固 体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正确的是( )
将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固 体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正确的是( )
A.Mg和Al的总质量为8g
|
C.生成的H2在标准状况下的体积为11.2L
D.NaOH溶液的物质的量浓度为5mol/L
【知识点】物质分离
【答案解析】D 解析:由图可知,0~20mL发生酸碱中和,20~200mL发生离子与碱生成沉淀的反应,200~240mL发生Al(OH)3+NaOH=NaAlO2+2H2O,200mL时生成沉淀最多,溶液中的溶质为硫酸钠。A、由图象可知,n(Mg)=0.15mol,n(Al)=0.2mol,则Mg和Al的总质量为0.15mol×24g/mol+0.2mol×27g/mol=9g,故A错误;B由200~240mL发生Al(OH)3+NaOH=NaAlO2+2H2O,c(NaOH)=0.2mol/0.04L=5mol/L,200mL时生成沉淀最多,溶液中的溶质为硫酸钠,则c(H2SO4)=0.2L*5mol/L/0.5L*2=1mol/L,故B错误;C、与硫酸反应生成的氢气的体积应为(0.15mol+0.3mol)×22.4 L•mol-1=10.08L,故C错误;D、在加入240mLNaOH溶液时,Al(OH)3恰好全部转化为NaAlO2,由B的计算可知氢氧化钠溶液的浓度为5mol•L-1,故D正确。
故答案选D
【思路点拨】本题考查金属的化学性质及图象,明确图象中点、线、面的意义及发生的化学反应为解答的关键,注意氢氧化铝能溶解在NaOH溶液中,侧重分析及计算能力的考查,题目难度中等。


 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
取一定质量的均匀固体混合物Cu、Cu2O和 CuO,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少6.40g,另一份中加入500mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体4.48L,则所用硝酸的物质的量浓度为
A.2.8mol·L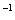 B.3.2mol·L
B.3.2mol·L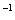 C.3.6mol·L
C.3.6mol·L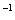 D.无法判断
D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
能把Na2SO4、NH4NO3、KCl、(NH4)2SO4四瓶无色溶液加以区别的一种试剂是(必要时可加热)( )
|
| A. | BaCl2 | B. | NaOH | C. | Ba(OH)2 | D. | AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮用水处理的新技术。
已知反应Fe2O3+3Na2O2===2Na2FeO4+Na2O,下列说法正确的是( )
A.Na2O2既是氧化剂又是还原剂
B.Fe2O3在反应中得到电子
C.3 mol Na2O2发生反应,有12 mol e-发生转移
D.Na2FeO4能消毒杀菌是因其具有强氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
)已知:(X代表卤素原子,R代表烃基)
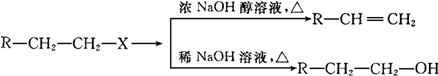
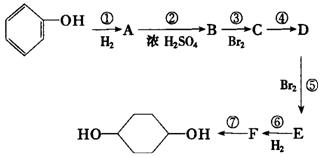 利用上述信息,按以下步骤从
利用上述信息,按以下步骤从 合成
合成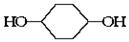 。(部分试剂和反应条件已略去)
。(部分试剂和反应条件已略去)
请回答下列问题:
(1)分别写出B、D的结构简式:B____ 、D_ ____ __。
(2)反应①~⑦中属于消去反应的是____ _____。(填数字代号)
(3)如果不考虑⑥、⑦反应,对于反应⑤,得到的E可能的结构简式为:
_ 。
(4)试写出C D反应的化学方程式(有机物写结构简式,并注明反应条件)
D反应的化学方程式(有机物写结构简式,并注明反应条件)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列措施对增大反应速率明显有效的是
A.在炭粉燃烧中加入KClO3
B.Zn与25%的稀硫酸反应制取H2时,改用98%的浓硫酸
C.在K2S04与BaCl2两溶液反应时,增大压强
D.Na与乙醇反应时增大乙醇的用量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒夏特利原理来解释的是:
A.用排饱和食盐水的方法收集氯气
B.合成氨工业选择高温(合成氨反应为放热反应)
C.增大压强,有利于SO2和O2反应生成SO3
D.在Fe3++3SCN -  Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
离子方程式:RO3n—+F2+2OH-==RO4—+2F—+H2O,由此可知在RO3n—中,元素R的化合价是
A.+4 B.+5 C.+6 D.+7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com