
已知A为中学化学中的常见金属,X、Y为常见非金属。X、E、F、G、J常温下为气体,C为无色液体,B是一种盐,受热易分解。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图(部分反应的条件、生成物被略去):

请填写下列空白:
⑴金属A为 ;操作a是将D溶液在HCl气流中蒸干,原因是
⑵反应②的化学方程为: ;
反应⑤的化学方程: 。
⑶原电池反应①中,正极反应式为: 。
科目:高中化学 来源: 题型:
 (2012?琼海一模)已知A为中学化学中的一种盐,B、C为日常生活中常见的金属.通常条件下D、G为无色无味气体.已知用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液.各物质之间的转化关系如图(部分反应产物已略去).
(2012?琼海一模)已知A为中学化学中的一种盐,B、C为日常生活中常见的金属.通常条件下D、G为无色无味气体.已知用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液.各物质之间的转化关系如图(部分反应产物已略去).查看答案和解析>>
科目:高中化学 来源:2012届海南省琼海市高考模拟测试(一)化学试卷 题型:填空题
(10分)已知A为中学化学中的一种盐,B、C为日常生活中常见的金属。通常
条件下D为无色无味气体,无色气体G遇空气变红棕色。已知用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液。各物质之间的转化关系如下图(部分反应产物已略去)。
请回答下列问题:
(1)A的化学式为 。
(2)A溶液与Na2O2反应的总化学方程式为 。
(3)E的稀溶液与F溶液反应的离子方程式为 。
(4)电解100mL盐A的溶液一段时间后,断开电路,取出电极,测得所得到的气体D在标准状况下的体积为5.6mL,则电解后溶液的pH为 。(假设溶液体积不变)
(5)若向100mL盐A的溶液中加入10g金属单质B的粉末,充分搅拌后,过滤,烘干得10.16g固体,则滤液中溶质的物质的量浓度为 。(假设溶液体积不变)
查看答案和解析>>
科目:高中化学 来源:2011-2012学年海南省琼海市高考模拟测试(一)化学试卷 题型:填空题
(10分)已知A为中学化学中的一种盐,B、C为日常生活中常见的金属。通常
条件下D为无色无味气体,无色气体G遇空气变红棕色。已知用惰性电极电解A溶液一段时间后,产物只有C、D和E的稀溶液。各物质之间的转化关系如下图(部分反应产物已略去)。

请回答下列问题:
(1)A的化学式为 。
(2)A溶液与Na2O2反应的总化学方程式为 。
(3)E的稀溶液与F溶液反应的离子方程式为 。
(4)电解100mL盐A的溶液一段时间后,断开电路,取出电极,测得所得到的气体D在标准状况下的体积为5.6mL,则电解后溶液的pH为 。(假设溶液体积不变)
(5)若向100mL盐A的溶液中加入10g金属单质B的粉末,充分搅拌后,过滤,烘干得10.16g固体,则滤液中溶质的物质的量浓度为 。(假设溶液体积不变)
查看答案和解析>>
科目:高中化学 来源:河南省模拟题 题型:推断题

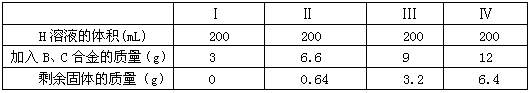
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com