
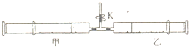
 如图所示,将甲.乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(实验均在常温常压下进行).
如图所示,将甲.乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(实验均在常温常压下进行).| 实验序号 | 甲针筒内的物质 | 乙针筒内的物质 |
| 1 | 0.3gNa2CO3粉末 | 3mL稀HCl |
| 2 | 0.3gNaHCO3粉末 | 3mL稀HCl |
| 3 | 0.8gNa2O2粉末 | 3ml H2O |


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:阅读理解

| 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
| 1 | 40mL HCl | 40mL NH3 | 产生白烟 |
| 2 | 40mL Cl2 | 10mL水 | 剩余气体为20mL |
| 3 | 30mL NO | 15mL O2 | |
| 4 | 20mL AlCl3溶液 | 10mL NaOH溶液 | 生成白色沉淀,后消失 |

查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定). 则下列说法正确的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
| 1 | 10mL FeSO4溶液 | 10mL NH3 | 生成白色沉淀,后变色 |
| 2 | 15mL H2S | 10mL SO2 | 活塞自动向内移动,析出浅黄色固体 |
| 3 | 10mL Cl2 | 40mL NH3 | |
| 4 | 25mL混合气体 | 10mL H2O(l) | 剩有无色气体,活塞自动向内移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
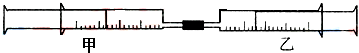
| 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
| 1 | 10mLFeSO4溶液 | 10mLNH3 | 生成白色沉淀,后变色 |
| 2 | 20mLH2S | 10mLSO2 | |
| 3 | 30mLNO2(主要) | 10mLH2O(l) | 剩有无色气体,活 塞自动向内压缩 |
| 4 | 15molCl2 | 40mLNH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com