
化学兴趣小组在家中进行化学实验,按照图一连接好线路发现灯泡不亮,按照图二连接好线路发现灯泡亮,由此得出的结论正确的是

A.NaCl是非电解质
B.NaCl溶液是电解质[来
C.NaCl固体中不存在带电离子
D.NaCl的水溶液中存在可自由移动的带电微粒
 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源:2016届四川省绵阳市高三上学期第一次诊断性测试理综化学试卷(解析版) 题型:实验题
己二酸是合成尼龙-66的主要原料之一。实验室合成己二酸的原理、有关数据及装置示意图如下:
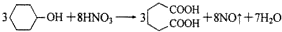
物质 | 密度(g/cm3) | 熔点 | 沸点 | 溶解性 |
环己醇 | 0.962g/cm3 | 25.9℃ | 160.8℃ | 20℃时水中溶解度为3.6g,可混溶于乙醇、苯 |
己二酸 | 1.360g/cm3 | 152℃ | 337.5℃ | 在水中的溶解度:15℃时1.44g,25℃时2.3g,易溶于乙醇、不溶于苯 |
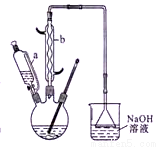
实验步骤如下:
I.在三口烧瓶中加入16 mL 50%的硝酸(密度为l.3lg/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL环己醇。
II.水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间。
Ⅲ.当环己醇全部加入后,将混合物用80℃一90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止。
Ⅳ,趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重。
请回答下列问题:
(1)本实验所用50%的硝酸物质的量浓度为__________。滴液漏斗的细支管a的作用是 。
(2)仪器b的名称为____ 使用时要从________(填“上口”或“下口”)通入冷水。
(3)NaOH溶液的作用是__________,溶液上方倒扣的漏斗作用是 。
(4)向三口烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是 。
(5)进行该实验时要控制好环己醇的滴入速率,防止反应过于剧烈,否则可能造成较严重的后果,试列举两条可能的后果: 。
(6)为了除去可能的杂质和减少产品损失,可分别用__________和____________洗涤晶体。
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三11月月考化学试卷(解析版) 题型:填空题
(一)(1)钠及其化合物是中学化学常用物质,核潜艇或宇宙飞船常用过氧化钠做供氧剂,其原理是_______________________________、_______________________________(用化学方程式表示),若上述变化过程中消耗过氧化钠的质量为 23.4g,则变化过程中转移电子数为_____________个。
23.4g,则变化过程中转移电子数为_____________个。
(2)下列关于Na2O2的叙述正确的是__________
A.Na2O2中阴、阳离子的个数比为1∶1
B.Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的质量相等
C.取a g某物质在O2中完全燃烧,将生成物与足量Na2O2固体完全反应,反应后,固体质量恰好也增加了a g,该物质可能是C6H12O6
D.Na2O2的漂白原理与SO2的漂白原理相同
E.Na2O2与水反应是水作还原剂的氧化还原反应
F.Na2O2与NaHCO3固体按物质的量之比1:1混合加热充分反应后,所得固体中Na2CO3和NaOH的物质的量之比亦为1:1
(二)切开的金属Na暴露在空气中,其变化过程如下:

(1)反应Ⅰ的反应过程与能量变化的关系如右图:

① 反应Ⅰ 是 反应(填“放热”或“吸热”),判断依据是_________________________________。
② 1 mol Na(s)全部氧化成Na2O(s)的热化学方程式是 _________________________________。
(2)白色粉末为Na2CO3。将其溶于水配制为0.1 mol/L Na2CO3溶液,下列说法正确的是 (填字母)。
Na2CO3溶液,下列说法正确的是 (填字母)。
A.升高温度,溶液的pH降低
B.c(OH-)-c (H+)=c (HCO3-)+2 c (H2CO3)
C.加入少量NaOH固体,c (CO32―)与c (Na+)均增大
D.c (Na+) > c (CO32―) > c (HCO3―) > c(OH―) > c (H+)
(3) 钠电池的研究开发在一定程度上可缓和因锂资源短缺引发的电池发展受限问题。
① 钠比锂活泼,用原子结构解释原因___________________________________。
② ZEBRA 电池是一种钠电池,总反应为NiCl2 + 2Na 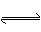 Ni + 2NaCl。其负极反应式是____________
Ni + 2NaCl。其负极反应式是____________
查看答案和解析>>
科目:高中化学 来源:2016届宁夏育才中学高三上学期第四次月考化学试卷(解析版) 题型:选择题
下列有关物质性质的应用正确的是( )
A.液氨汽化时要吸收大量的热,可用作制冷剂
B.二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸
C.生石灰能与水反应,可用来干燥氯气
D.氯化铝是一种电解质,可用于电解制铝
查看答案和解析>>
科目:高中化学 来源:2016届海南省等七校联盟高三第一次联考化学卷(解析版) 题型:填空题
I.下列分子中,立体构型是平面三角形的是_____。
A.CH4 B.NH3 C.BF3 D.SO3
II.氟及氟产品在工农业生产中应用非常广泛,回答下列问题:
(1)基态氟原子核外电子的运动状态有______种,这些电子的电子云形状有______种;氟原子的外围电子排布式为________。
(2)NaHF2(氟化氢钠)电解可制氟气,NaHF2中所含作用力的类型有____;与HF2-互为等电子体的分子有______(举一例)。
(3)C2F4分子中,碳原子的杂化轨道类型为________。
(4)三氟化硼乙醚( )的熔点为-58℃,沸点为126~129℃,它属于_____晶体。
)的熔点为-58℃,沸点为126~129℃,它属于_____晶体。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江余姚中学高一上学期期中考试化学试卷(解析版) 题型:选择题
下列叙述中,正确的是
A.次氯酸能杀死病菌,所以氯气可用于自来水的消毒
B.实验室制取氯气时,常用水来吸收多余的氯气
C.漂白粉中含有次氯酸,所以漂白粉能使染料等有机色素褪色
D.氯气不能使干燥的有色布条褪色,液氯能使干燥的有色布条褪色
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江台州中学高二上第三次统练化学试卷(解析版) 题型:选择题
分析下列反应在任何温度下均能自发进行的是
A.2N2(g)+O2(g) ═ 2N2O(g) △H=+163 kJ·mol-1
B.Ag(s)+ 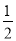 Cl2(g) ═ AgCl(s) △H= -127 kJ·mol-1
Cl2(g) ═ AgCl(s) △H= -127 kJ·mol-1
C.HgO(s) ═ Hg(l) + 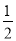 O2(g) △H=+91 kJ·mol-1
O2(g) △H=+91 kJ·mol-1
D.H2O2(l) ═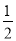 O2(g) + H2O(l) △H= -98 kJ·mol-1
O2(g) + H2O(l) △H= -98 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南常德市高二12月月考化学卷(解析版) 题型:选择题
下列说法正确的是( )
A.对于有气体参与的反应,增大压强,活化分子数增多,化学反应速率增大
B.对放热反应而言,升高温度,活化分子百分数减少,反应速率减小
C.活化分子间发生的碰撞为有效碰撞
D.使用催化剂,活化分子百分数增多,化学反应速率增大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东枣庄三中高二10月学情调查化学卷(解析版) 题型:选择题
下列叙述正确的是
A.电解饱和食盐水时,用铁作阳极,Cl- 发生氧化反应
B.铅蓄电池放电时,负极质量减轻,正极质量增加
C.马口铁(镀锡铁)镀层破损后即失去保护作用
D.钢铁发生电化学腐蚀的负极反应式:Fe-3e- == Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com