
分析 该原电池中,锌电极上电极反应式为Zn-2e-=Zn2+,铜电极上电极反应式为2H++2e-=H2↑,则电池反应式为Zn+2H+=H2↑+Zn2+,
(1)根据氢气和锌之间的关系式计算锌的质量;
(2)根据氢气和转移电子之间的关系式计算转移电子的物质的量.
解答 解:(1)设锌片的质量减少了x,
Zn+H2SO4=ZnSO4+H2↑
65g 22.4L
x 3.36L
所以 x=9.75g,
答:锌片的质量减少了9.75g;
(2)设转移电子z,则
2H++2e-=H2↑
2mol 22.4L
y 3.36L
y=$\frac{2×3.36}{22.4}$mol=0.3mol
答:通过导线的电子的物质的量是0.3mol.
点评 本题以原电池为载体考查了氧化还原反应的有关计算,侧重于学生的分析能力和计算能力的考查,注意把握原电池的工作原理,明确各物理量间的关系是解本题的关键.


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:解答题
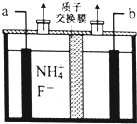 (1)某催化剂可将汽车尾气中的CO、NO转化为无毒气体.已知:
(1)某催化剂可将汽车尾气中的CO、NO转化为无毒气体.已知:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
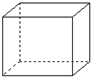 有机物的结构可用“键线式”简化表示.例如CH3-CH=CH-CH3可简写为
有机物的结构可用“键线式”简化表示.例如CH3-CH=CH-CH3可简写为  .“立方烷”是一种新合成的烃,其分子为正方体结构,其碳架结构如图:
.“立方烷”是一种新合成的烃,其分子为正方体结构,其碳架结构如图: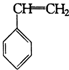 B.
B. 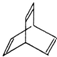 C.
C.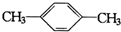 D.
D.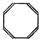
 +Br2→
+Br2→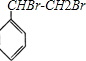 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 决定反应速率的因素只有催化剂 | |
| B. | 食物放在冰箱中会减慢食物变质的速率 | |
| C. | 锌与稀硫酸反应时,加入少量水能加快产生氢气的速率 | |
| D. | 在一定条件下2mol SO2与 1mol O2混合一定能生成2mol SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
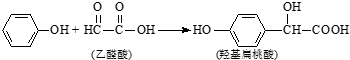
| A. | 苯酚和羟基扁桃酸互为同系物 | |
| B. | 常温下,1mol羟基扁桃酸只能与1mol Br2反应 | |
| C. | 乙醛酸的核磁共振氢谱中只有1个吸收峰 | |
| D. | 羟基扁桃酸可以发生取代、氧化、加成等反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com