
【题目】为测试一铁片中铁元素的含量,某课外活动小组提出下面方案并进行了实验。将0.200g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用![]() 的
的![]() 溶液滴定,达到终点时消耗了
溶液滴定,达到终点时消耗了![]() 溶液。
溶液。
(1)配平以下方程式并标出电子转移的方向与数目____________________。
![]()
(2)滴定到终点时的现象为____________________,铁片中铁元素的质量分数为_______________________。
(3)高锰酸钾溶液往往用硫酸酸化而不用盐酸酸化,原因是:_____________。
(4)![]() 溶液呈酸性,加硫酸后
溶液呈酸性,加硫酸后![]() 增加,请结合离子方程式并利用化学平衡移动理论解释:_____________________________。
增加,请结合离子方程式并利用化学平衡移动理论解释:_____________________________。
(5)高锰酸钾在化学品生产中,广泛用作为氧化剂。可以氧化![]() 、
、![]() 、
、![]() 、
、![]() 等多种物质,如
等多种物质,如![]() ,试推测空格上应填物质的化学式为________。
,试推测空格上应填物质的化学式为________。
(6)上述反应在恒温下进行,该过程中会明显看到先慢后快的反应,原因可能是____________________。
【答案】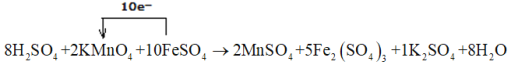 最后加入一滴高锰酸钾,出现紫红色且30s不褪色 70% 盐酸有还原性(或
最后加入一滴高锰酸钾,出现紫红色且30s不褪色 70% 盐酸有还原性(或![]() 有还原性),易被高锰酸钾氧化
有还原性),易被高锰酸钾氧化 ![]() ,加入稀硫酸,增大
,加入稀硫酸,增大![]() 浓度,平衡向左移动,抑制了
浓度,平衡向左移动,抑制了![]() 水解,所以
水解,所以![]() 增大
增大 ![]() 生成的
生成的![]() 可能有催化作用,加快了反应速度
可能有催化作用,加快了反应速度
【解析】
根据氧化还原反应中得失电子守恒配平化学方程式;根据滴定原理分析滴定终点的现象及计算物质的质量分数;根据平衡移动原理及影响速率的因素分析解答。
(1)元素的化合价变化为:Mn:+7→+2,改变数为5,Fe:+2→+3,改变数为1,根据化合价升降的总数相等可知,KMnO4与FeSO4的化学计量数比值为1:5,然后根据质量守恒配平化学方程式,配平后的化学方程式为8H2SO4+2KMnO4+10FeSO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O,电子由Fe转移到Mn: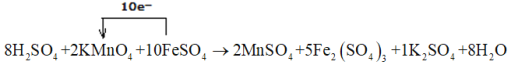 ;
;
(2)高锰酸钾滴入时被亚铁离子还原成无色,则滴定到终点时的现象为最后加入一滴高锰酸钾,出现紫红色且30s不褪色;根据方程式计算得
KMnO4~~~5FeSO4~~~5Fe
1mol 5mol
0.02mol/L×0.025L n
n(Fe)=0.02mol/L×0.025L×5=0.0025mol
则铁片中铁元素的质量分数为![]() ;
;
(3)高锰酸钾有氧化性,盐酸有还原性(或![]() 有还原性),易被高锰酸钾氧化;
有还原性),易被高锰酸钾氧化;
(4)铁离子水解:![]() ,加入稀硫酸,增大
,加入稀硫酸,增大![]() 浓度,平衡向左移动,抑制了
浓度,平衡向左移动,抑制了![]() 水解,所以
水解,所以![]() 增大;
增大;
(5)H2O2中O为-1价,被高锰酸钾氧化后生成O2,故答案为O2;
(6)因为恒温,所以影响反应速率的因素可能是催化剂,故答案为:生成的![]() 可能有催化作用,加快了反应速度。
可能有催化作用,加快了反应速度。


科目:高中化学 来源: 题型:
【题目】下列关于离子的检验说法正确的是
A.向某溶液中滴入足量盐酸,如观察到无色无味的气体产生,且能使澄清石灰水变浑浊,即证明溶液中必定有![]()
B.向某无色溶液中加入BaCl2溶液,有白色沉淀出现,再加入稀盐酸,沉淀不消失,无法证明溶液一定含有![]()
C.向某无色溶液中加入少量稀氢氧化钠溶液后,用湿润的红色石蕊试纸靠近试管口,若试纸不变蓝,则说明该溶液中无![]()
D.如透过蓝色的钴玻璃能够观察到紫色火焰,则一定有钾元素,一定不含有钠元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】共价键都有键能之说,键能是指拆开1mol共价键所需要吸收的能量。如H-H键的键能是436kJ/mol,H—Cl键的键能是431kJ/mol,Cl—Cl键的键能是247 kJ /mol,H2和Cl2反应生成1molHCl放出的热量是( )
A.431kJB.179kJC.89.5kJD.以上说法都不对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在银锌原电池中,以硫酸铜为电解质溶液,锌为_____极,电极上发生的是_____反应(“氧化”或“还原”).电极反应式为_____,锌片上观察到的现象为_____银为_____极,电极上发生的是_____反应(“氧化”或“还原”),电极反应式是_____,银片上观察到的现象是_____.
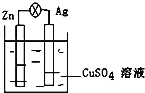
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一未知的无色溶液中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 。分别取样:①用
。分别取样:①用![]() 计测试,溶液显弱酸性;②加适量氯水和淀粉无明显现象。由此可知原溶液中
计测试,溶液显弱酸性;②加适量氯水和淀粉无明显现象。由此可知原溶液中
A.可能不含![]() B.可能含有
B.可能含有![]()
C.一定含有![]() D.一定含有3种离子
D.一定含有3种离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知以下反应中的四种物质由三种元素组成,其中a的分子立体构型为正四面体形,组成a物质的两种元素的原子序数之和小于10,组成b物质的元素为第三周期元素。下列判断正确的是
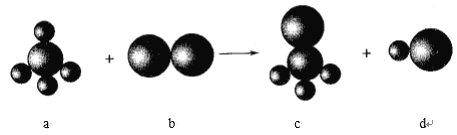
A. 四种分子中的化学键均是极性键
B. a、c分子中中心原子均采用sp3杂化
C. 四种分子中既有σ键,又有π键
D. b、d分子中共价键的键能:b>d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2016·新课标I]锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]_______________,有__________个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是______________________________。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因______________________________。
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | 49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是______________________________。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______________,微粒之间存在的作用力是_______________。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(![]() ,0,
,0,![]() );C为(
);C为(![]() ,
,![]() ,0)。则D原子的坐标参数为_______________。
,0)。则D原子的坐标参数为_______________。

②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76 pm,其密度为_____g·cm3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 饱和Na2CO3溶液与CaSO4固体反应:CO32+CaSO4![]() CaCO3+SO42
CaCO3+SO42
B. 酸化NaIO3和NaI的混合溶液:I +IO3+6H+![]() I2+3H2O
I2+3H2O
C. KClO碱性溶液与Fe(OH)3反应:3ClO+2Fe(OH)3![]() 2FeO42+3Cl+4H++H2O
2FeO42+3Cl+4H++H2O
D. 电解饱和食盐水:2Cl+2H+![]() Cl2↑+ H2↑
Cl2↑+ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠离子电池具有成本低、能量转换效率高、寿命长等优点。一种钠离子电池用碳基材料 (NamCn)作负极,利用钠离子在正负极之间嵌脱过程实现充放电,该钠离子电池的工作原理 为Na1-mCoO2+NamCn![]() NaCoO2+Cn。下列说法不正确的是
NaCoO2+Cn。下列说法不正确的是
A.放电时,Na+向正极移动
B.放电时,负极的电极反应式为NamCn—me-=mNa++Cn
C.充电时,阴极质量减小
D.充电时,阳极的电极反应式为NaCoO2-me-=Na1-mCoO2+mNa+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com