
【题目】卤族元素在自然界中都以典型的盐类存在,包括氟、氯、溴、碘和砹五种元素,位于元素周期表的第ⅦA族,其中氯、溴和碘主要来自海水.卤素元素在生产实际中承担着重要角色.请回答下列问题:
(1)将经过验纯的氢气点燃,伸入盛有氯气的集气瓶中,在集气瓶口可观察到的现象是
(2)欲检验Na2CO3、Na2SO4、NaCl的混合溶液中的Cl﹣ , 正确的操作方法是
(3)海水晒盐所获取的粗盐,经过提纯、精制之后,其水溶液进行电解,可以得到重要的化工原料.请写出该电解反应的离子方程式 . 海带中提取碘时,将海带烘干、灼烧目的是 .
(4)将0.01molCl2通入含0.03molNaBr和0.03molKI的混合液中,发生反应的离子方程式为 再将所得溶液分为两等份,其中一份蒸干、灼烧,最后得到的固体的成分一定有KCl,还有;另一份再加入少量CCl4 , 振荡,则CCl4层的颜色是 , 分离CCl4层和水层的操作名称是 , 需要使用的玻璃仪器除烧杯外,还有 .
【答案】
(1)有白雾产生
(2)取样,加过量的Ba(NO3)2溶液,过滤,取上层清液滴加AgNO3溶液,若有白色沉淀产生中,则混合溶液中含Cl﹣
(3)2Cl﹣+2H2O ![]() Cl2↑+H2↑+2OH﹣;将有机态的碘转化为无机态的碘,易于提取 、 增大固体表面积有利于溶解
Cl2↑+H2↑+2OH﹣;将有机态的碘转化为无机态的碘,易于提取 、 增大固体表面积有利于溶解
(4)Cl2+2I﹣=I2+2Cl﹣; KI、NaBr;紫红;分液;分液漏斗
【解析】解:(1)氢气在氯气燃烧产生白色雾,所以答案是:有白雾产生;(2)欲检验Na2CO3、Na2SO4、NaCl的混合溶液中的Cl﹣,首先排除碳酸根和硫酸根离子的干扰,与碳酸根与硫酸生成沉淀是钡离子,所以首先取样加过量的Ba(NO3)2溶液,然后加入可溶的硝酸银,具体操作为:取样,加过量的Ba(NO3)2溶液,过滤,取上层清液滴加AgNO3溶液,若有白色沉淀产生中,则混合溶液中含Cl﹣,
所以答案是:取样,加过量的Ba(NO3)2溶液,过滤,取上层清液滴加AgNO3溶液,若有白色沉淀产生中,则混合溶液中含Cl﹣;(3)电解食盐水生成氢氧化钠、氢气、氯气,反应的离子方程式为:2Cl﹣+2H2O ![]() Cl2↑+H2↑+2OH﹣;海带中提取碘时,将海带烘干、灼烧目的是将有机态的碘转化为无机态的碘,易于提取 增大固体表面积有利于溶解,
Cl2↑+H2↑+2OH﹣;海带中提取碘时,将海带烘干、灼烧目的是将有机态的碘转化为无机态的碘,易于提取 增大固体表面积有利于溶解,
所以答案是:2Cl﹣+2H2O ![]() Cl2↑+H2↑+2OH﹣;将有机态的碘转化为无机态的碘,易于提取;增大固体表面积有利于溶解;(4)0.01molCl2得到0.02mol的电子,所以只有碘离子参加反应,反应的离子方程式为:Cl2+2I﹣=I2+2Cl﹣;含0.03molNaBr和0.03molKI的混合液中,碘离子部分反应,所以将所得溶液分为两等份,其中一份蒸干、灼烧,最后得到的固体的成分一定有KCl,还有 KI、NaBr;另一份再加入少量CCl4,振荡,碘溶解在四氯化碳中,则CCl4层的颜色是紫红;互不相溶的液体物质的分离用分液的方法,所以分离CCl4层和水层的操作名称是分液;分液用的主要仪器为 分液漏斗,则需要使用的玻璃仪器除烧杯外,还有分液漏斗,所以答案是:Cl2+2I﹣=I2+2Cl﹣; KI、NaBr;紫红;分液;分液漏斗.
Cl2↑+H2↑+2OH﹣;将有机态的碘转化为无机态的碘,易于提取;增大固体表面积有利于溶解;(4)0.01molCl2得到0.02mol的电子,所以只有碘离子参加反应,反应的离子方程式为:Cl2+2I﹣=I2+2Cl﹣;含0.03molNaBr和0.03molKI的混合液中,碘离子部分反应,所以将所得溶液分为两等份,其中一份蒸干、灼烧,最后得到的固体的成分一定有KCl,还有 KI、NaBr;另一份再加入少量CCl4,振荡,碘溶解在四氯化碳中,则CCl4层的颜色是紫红;互不相溶的液体物质的分离用分液的方法,所以分离CCl4层和水层的操作名称是分液;分液用的主要仪器为 分液漏斗,则需要使用的玻璃仪器除烧杯外,还有分液漏斗,所以答案是:Cl2+2I﹣=I2+2Cl﹣; KI、NaBr;紫红;分液;分液漏斗.
【考点精析】利用氯气的化学性质对题目进行判断即可得到答案,需要熟知氯气的化学性质:与金属反应将金属氧化成高价态;非金属反应;与水反应;与碱反应;与还原性物质反应.


科目:高中化学 来源: 题型:
【题目】用20mL 18.4molL﹣1 浓H2SO4与金属铜共热一段时间后,冷却,过滤,除去多余的铜,将滤液加水稀释到100mL,所得溶液中SO42﹣的物质的量浓度为3.18molL﹣1 , 则此时溶液中CuSO4的物质的量浓度为( )
A.0.50 molL﹣1
B.0.75 molL﹣1
C.1.00 molL﹣1
D.3.18 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.实验室配制的亚铁盐溶液在空气中被氧化:4Fe2++O2+2H2O═4Fe3++4OH﹣
B.以金属银为阳极电解饱和硫酸铜溶液:Cu2++2H2O ![]() 2Cu+O2↑+4H+
2Cu+O2↑+4H+
C.Ca(ClO)2溶液中通入过量的SO2气体:ClO﹣+SO2+H2O═HClO+HSO3﹣
D.用酸化的高锰酸钾溶液氧化双氧水:2 MnO4﹣+6H++5H2O2═2Mn2++5O2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设C+CO22CO;△H>0,反应速率为v1;N2+3H22NH3;△H<0,反应速率为v2 , 对于上述反应,当温度升高时,v1和v2的变化情况为( )
A.同时增大
B.同时减小
C.v1增大,v2减小
D.v1减小,v2增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某有机化合物A的结构,进行如下实验:
(1)分子式的确定 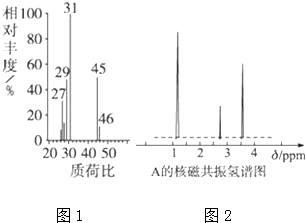
(i)将有机物A置于氧气流中充分燃烧实验测得:碳的质量分数为52.16%,氢的质量分数为13,.14%,则该物质中各元素的原子个数比是
(ii)用质谱仪测定其相对分子质量,得到如图1所示的质谱图,则该有机物A的相对分子质量为 , 分子式为
(iii)根据价键理论,预测A的可能结构并写出结构简式
(2)结构式的确定 核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目经测定,有机物A的核磁共振氢谱示意图如图2所示,则A的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于钠的化合物的说法中,正确的是( )
A.Na2CO3和NaHCO3均能与盐酸和NaOH溶液反应
B.NaHCO3固体中混有的Na2CO3可用加热的方法除去
C.Na2O2和Na2O中阴阳离子个数比均为1:2
D.分别向Na2O2和Na2O与水反应后的溶液中立即滴入酚酞溶液,现象相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若pH=2的酸溶液和pH=12的碱溶液等体积混合后溶液呈碱性,其原因可能( )
A.反应后盐水解使溶液呈碱性
B.弱酸溶液和强碱溶液反应
C.强酸溶液和弱碱溶液反应
D.一元强酸溶液和一元强碱溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列反应不能制得括号中纯净物质的是
A. 乙烯与水加成 (乙醇)
B. 等物质的量的氯气与乙烷在光照条件下反应(一氯乙烷)
C. 氯气与苯用氯化铁做催化剂反应(氯苯)
D. 乙烯与氯气加成(CH2ClCH2Cl)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《化学与生活》
(1)把新制的氢氧化铜悬浊液加入到某病人的尿液中并微热,如果观察到红色沉淀,说明尿液中可能含有的物质是
A.尿酸 B.蔗糖 C.蛋白质 D.葡萄糖
(2)垃圾处理无害化、减量化和资源化逐渐被人们认识.垃圾的分类收集是实现上述理念的重要措施.某垃圾箱上贴有如图所示的标志,向此垃圾箱中丢弃的垃圾是
A.危险垃圾 B.有害垃圾 C.可回收物 D.其他垃圾
(3)人类生命活动所需的各种营养主要来自于食物,食物的选择与身体健康关系很大.表格是某位同学的早餐食谱:
主食 | 面包 |
副食 | 酱牛肉 |
饮品 | 豆浆 |
表中主食含有的营养素主要是 (填“糖类”、“油脂”或“蛋白质”,下同);副食含有的营养素主要是 ,豆浆所属的分散系为 ( 填“溶液”“浊液”或“胶体”).考虑到营养成分的均衡搭配,你认为应该增加的配菜是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com