
欲从苯酚的乙醇溶液中分离苯酚和乙醇,有下列操作:
①过滤 ②蒸馏 ③静置分液
④加入足量的金属钠 ⑤加入足量的NaOH溶液 ⑥通入过量的二氧化碳
⑦加入足量的FeCl3 溶液 ⑧加入乙酸与浓硫酸混合液加热。
合理的实验操作步骤及顺序是( )
A. ④⑤③ B. ⑥①⑤③ C. ⑧①⑦③ D. ⑤②⑥③
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
2003年诺贝尔化学奖授予了美国科学家Peter Agre和Roderick Mackinnon以表彰他们在“水通道”和“离子通道”的研究成就。Mackinnon教授的研究内容主要是Na+、K+体积很接近,但在生物体内呈现的差别却高达1万倍,他革命性的让科学家观测Na+、K+在进入离子通道前、通道中以及穿过通道后的状态,可为病人在“离子通道”中寻找具体的病因,并研制相应药物。下列关于钠、钾的说法正确的是
A.单质钠的密度比钾的密度小 B.Na+和K+常用作氧化剂
C.钠和钾都是短周期元素 D.钠和钾的合金[ω(K)=50%~80%]在室温下呈液态
查看答案和解析>>
科目:高中化学 来源: 题型:
一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷
和氧气,其总反应为:2C2H6+702+8KOH 4K2C03+10H20,有关此电池的推断正确的
4K2C03+10H20,有关此电池的推断正确的
是( )。
A.负极反应为:14H20+702+28e- 280H-
280H-
B.放电一段时间后,负极周围pH升高
C.每消耗1 mol C2H6,则电路上转移的电子为14 mol
D.放电过程中KOH的物质的量浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
有两种有机物Q(  )与P(
)与P(  ),下列有关它们的说法中正
),下列有关它们的说法中正
确的是( )
A.二者的核磁共振氢谱中均只出现两种峰且峰面积之比为3∶1
B.二者在NaOH醇溶液中均可发生消去反应
C.一定条件下,二者在NaOH溶液中均可发生取代反应
D.Q的一氯代物只有1种、P的一溴代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.煤中含有苯和甲苯,可用分馏的方法把它们分离出来
B. C7H16的烷烃中,含有3个甲基的同分异构体有2种
C. 碳原子数小于或等于8的单烯烃中,与HBr加成产物只有一种结构,符合条件的
单烯烃有6种
D.某烃的分子式为C10H14,它不能使溴水褪色,但可使酸性KMnO4溶液褪色,且分子
结构中只有一个烷基,符合条件的烃有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.下图中A、B、C分别是三种有机物的结构模型:

请回答下列问题:
(1)A及其同系物的分子式中的碳原子数用n表示。当n=_______时,烷烃开始出
现同分异构体。B模型是有机物的________模型。
(2)结构简式为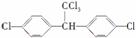 的有机物中,分子中最多有 个原子共面。
的有机物中,分子中最多有 个原子共面。
(3)等质量的A、B、C三种有机物完全燃烧生成H2O和CO2,消耗氧气的体积(相同状
况下)最大的是________(填分子式)。
Ⅱ.在有机物分子中,不同氢原子的核磁共振氢谱中给出的峰值(信号)也不同,根据
峰值(信号)可以确定有机物分子中氢原子的种类和数目。
(1)下列物质中,其核磁共振氢谱中给出的峰值(信号)只有一个的是________。
A.CH3COOH B. C(CH3)4 C.CH3COOCH3 D.CH3OH
(2)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如下图所示,则A的
结构简式为________。
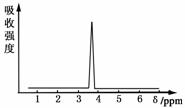
(3)用核磁共振氢谱的方法来研究C2H6O的结构,简要说明根据核磁共振氢谱的结果
来确定C2H6O分子结构的方法是_______________________ _ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
CO(g) +H2O(g)  CO2(g) +H2 (g) △H<0。
CO2(g) +H2 (g) △H<0。
(1)CO和H2O浓度变化如右图,则在该温度下,该反应的平衡常数K= 。 0~4min的平均反应速率v(CO)=_____mol·L-1·min-1。若降低温度,该反应的K值将 ,该反应的化学反应速率将 (填“增大”“减小”或“不变”)。
(2)在相同容器中发生上述反应,当温度高于850℃时, 容器内各物质的浓度变化如下表。
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
① 表中3min~4min之间反应处于______状态; c 1数值_____0.08 mol·L-1 (填大于、小于或等于)。
②反应在4min~5min间,平衡向逆方向移动,可能的原因是_________
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
(3)在相同温度下(850℃),若起始时c(CO)=1mol·L-1,c(H2O)=2mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,则此时该反应是否达到平衡状态 (填“是”与“否”),此时v(正) v(逆)(填“大于”“小于”或“等于”),你判断的依据是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在温度t ℃下,某Ba(OH)2的稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,
向该溶液中逐滴加入pH=b的盐酸,测得混合溶液的部分pH如下表所示:
| 序号 | 氢氧化钡的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
(1)依据题意判断,t ℃____25℃(填“大于”、“小于”或“等于”),该温度下水的离子积Kw=_____。
(2)b=____________,原Ba(OH)2的稀溶液的物质的量浓度为_____________。
(3)该温度下,向1L硫酸与硫酸钠的混合溶液中加入3L该Ba(OH)2的稀溶液时,沉淀正好达
最大量,从所得溶液中取出4mL并加水稀释至20mL,测得溶液的pH为7,则原硫酸与硫酸
钠混合溶液的pH为_________,以及其中Na2SO4的物质的量浓度为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com