
【题目】下列图中的实验方案,能达到实验目的的是:( )
A | B | C | D | |
实验方案 |
|
|
|
|
实验目的 | 验证FeCl3对H2O2分解反应有催化作用 | 验证单质氧化性: Cl2>Br2>I2 | 加热至混合液呈红褐色,停止加热,制备Fe(OH)3胶体 | 比较HCl、H2CO3和H2SiO3的酸性强弱 |
A. A B. B C. C D. D
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将羧酸的碱金属盐溶液用惰性电极电解可得到烃类化合物,例如:2CH3COOK+2H2O ![]() CH3CH3↑+2CO2↑+H2↑+2KOH现有下列衍变关系(A、B、C、D、E、F、G均为有机物): 回答下列问题:
CH3CH3↑+2CO2↑+H2↑+2KOH现有下列衍变关系(A、B、C、D、E、F、G均为有机物): 回答下列问题: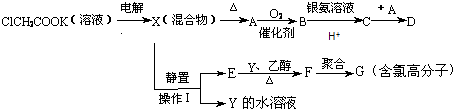
(1)电解ClCH2COOK溶液时阳极的电极反应式是(填选项).
A.2ClCH2COO﹣﹣2e﹣=ClCH2CH2Cl+2CO2↑
B.2H++2e﹣=H2↑
C.2H2O+2e﹣=2OH﹣+H2↑
D.4OH﹣﹣4e﹣=2H2O+O2↑
(2)操作Ⅰ的名称是 , G的结构简式是 .
(3)写出B与银氨溶液按物质的量1:4反应的化学方程式: .
(4)写出下列化学方程式并指出其反应类型:A→B方程式: .
E→F方程式: .
指出反应类型:A→B , E→F .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解池的叙述中不正确的是( )
A.与电源正极相连的是电解池的阴极
B.与电源负极相连的是电解池的阴极
C.在电解池的阳极发生氧化反应
D.电子从电源的负极沿导线流入电解池的阴极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法不正确的是( )
A.聚氯乙烯分子中含碳碳双键
B.以淀粉为原料可制取乙酸乙酯
C.戊烷有3种同分异构体
D.油脂的皂化反应属于水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中a、b、c表示相应仪器中加人的试剂,可用如图装置制取、净化、收集的气体是( )
编号 | 气体 | a | b | c |
|
A | NH3 | 浓氨水 | 生石灰 | 碱石灰 | |
B | CO2 | 盐酸 | 碳酸钙 | 饱和NaHCO3溶液 | |
C | NO | 稀硝酸 | 铜屑 | H2O | |
D | Cl2 | 浓盐酸 | 二氧化锰 | 饱和NaCl溶液 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,硫化铜矿的湿法冶炼已经取得很大的进展.现有一种催化氧化酸浸硫化铜矿的湿法冶炼法,其工艺流程如1图所示: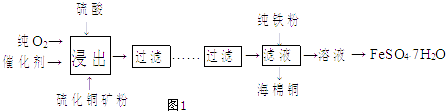
温度、固液比、反应时间、氯离子浓度都对铜的浸出率有较大的影响,下面是实验得出的这几种因素对铜的浸出率影响的变化曲线图(如图2﹣图5所示)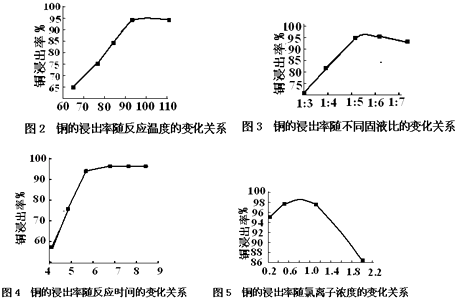
(1)根据实验以及工业生产的实际要求,从图2﹣图5中得出的最佳工艺条件为(从下表中选出序号) .
反应温度/℃ | 固液比 | c(Cl﹣)/molL﹣1 | 反应时间/h | |
A | 95 | 1:5.5 | 0.8 | 6 |
B | 100 | 1:5.5 | 0.7 | 7 |
C | 110 | 1:6 | 0.9 | 8 |
(2)上述流程从溶液中得到纯净的FeSO47H2O晶体的操作是蒸发浓缩、冷却结晶、过滤、、用乙醇淋洗、干燥.用乙醇淋洗的目的是: .
(3)副产品FeSO47H2O样品的纯度可用滴定法进行测定,实验步骤如下:步骤1:称取5.800g绿矾产品,经溶解、定容等步骤准确配制250mL溶液.
步骤2:从上述容量瓶中量取25.00mL待测溶液于锥形瓶中,
步骤3:用硫酸酸化的0.0100mol/L KMnO4溶液滴定至终点,记录消耗KMnO4溶液体积
步骤4:重复步骤2、步骤3一至两次.
①步骤1中用到的玻璃仪器有:烧杯、玻璃棒、胶头滴管和 , 步骤2量取溶液所用仪器是 .
②写出步骤3反应的离子方程式:
③数据处理:
滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
滴定前刻度/mL | 滴定后刻度/mL | ||
1 | 25.00mL | 0.02 | 40.01 |
2 | 25.00mL | 0.70 | 40.71 |
3 | 25.00mL | 0.20 | 39.20 |
计算上述样品中FeSO47H2O的质量分数为 .
④不考虑操作误差,用上述方法测定的样品中FeSO47H2O的质量分数(填偏低、偏高或无影响).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com