
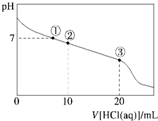
 �����£���20.00mL 0.100mol•L-1 CH3COONa��Һ����μ���0.100 0mol•L-1���ᣬ��Һ��pH��������������Ĺ�ϵ��ͼ��ʾ�������ǻӷ���������˵����ȷ�ģ�������
�����£���20.00mL 0.100mol•L-1 CH3COONa��Һ����μ���0.100 0mol•L-1���ᣬ��Һ��pH��������������Ĺ�ϵ��ͼ��ʾ�������ǻӷ���������˵����ȷ�ģ�������| A�� | �����ʾ��Һ�У�c��CH3COOH��=c��Cl-����c��OH-��=c��H+�� | |
| B�� | �����ʾ��Һ�У�c��Na+����c��Cl-����c��CH3COO-����c��CH3COOH�� | |
| C�� | �����ʾ��Һ�У�c��CH3COOH����c��Na+����c��H+����c��CH3COO-�� | |
| D�� | ���������п��ܳ��֣�c��H+��+c��Na+���Tc��CH3COOH��+c��CH3COO-�� |
���� A�������ҺpH=7�������Һ�ĵ���غ�������غ��жϣ�
B�����ʱ����Һ�д���CH3COONa��CH3COOH����Һ�����ԣ�Ӧ��c��CH3COO-����c��Cl-����
C�����ʱ��ǡ�÷�Ӧ����CH3COOH��CH3COOHΪ������ʣ�����ȫ���룬��Һ�����ԣ�
D��������Һ�е������غ��жϣ�
��� �⣺A����Һ���ڵ���غ�c��H+��+c��Na+��=c��OH-��+c��CH3COO-��+c��Cl-���������غ�c��Na+��=c��CH3COOH��+c��CH3COO-���������ҺpH=7��������ʽ�ɵ�c��CH3COOH��=c��Cl-������A��ȷ��
B�����ʱ����������10mL����Һ�д���CH3COONa��CH3COOH����Һ�����ԣ�˵��CH3COOH�������CH3COO-ˮ�⣬Ӧ��c��CH3COO-����c��Cl-������B����
C�����ʱ��ǡ�÷�Ӧ����CH3COOH��CH3COOHΪ������ʣ�����ȫ���룬��Һ�����ԣ���c��Na+����c��CH3COOH����c��H+����c��CH3COO-������C����
D����Һ�д��������غ㣺c��Na+��=c��CH3COOH��+c��CH3COO-������D����
��ѡA��
���� ���⿼������Ũ�ȴ�С�Ƚϣ���Ŀ�Ѷ��еȣ���ȷͼ����ζ�Ӧ��Һ���Ϊ���ؼ���ע�������ε�ˮ��ԭ���������غ�͵���غ�ĺ��弰Ӧ�÷���������������ѧ���ķ������������Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֻ�Тڢ� | B�� | ֻ�Т٢� | C�� | �٢ڢ� | D�� | �٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
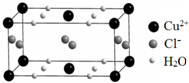 �������İ�ˮ�ӵ�����ͭ��Һ�У���Һ���ձ������ɫ�����������Ҵ�����������ɫ�ľ���[Cu��NH3��4]SO4•H2O��
�������İ�ˮ�ӵ�����ͭ��Һ�У���Һ���ձ������ɫ�����������Ҵ�����������ɫ�ľ���[Cu��NH3��4]SO4•H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢� | C�� | �ڢ� | D�� | �ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���ԭ���ڻ�ѧ��ҵ�����Ź㷺��Ӧ�ã��ֽ�ijͬѧ��Ƶ�ԭ���ͨ��
���ԭ���ڻ�ѧ��ҵ�����Ź㷺��Ӧ�ã��ֽ�ijͬѧ��Ƶ�ԭ���ͨ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������Һ��ϣ�2H++Cl-+ClO-�TCl2��+H2O | |
| B�� | ��100mL0.1mol/L FeBr2��Һ��ͨ��0.0125mol Cl2��2Fe2++4Br-+3Cl2�T2Fe3++2Br2+6Cl- | |
| C�� | �������������Һ���ն�������SO2+MnO4-+4H+�TSO42-+Mn2++2H2O | |
| D�� | ��������Һ�м������������������Һ��Al3++SO42-+Ba2++4OH-�TBaSO4��+[Al��OH��4]- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu+HNO3��ϡ����Cu��NO3��2 | |
| B�� | Cu+HNO3��Ũ����Cu��NO3��2 | |
| C�� | Cu$��_{����}^{Ũ����}$CuSO4$\stackrel{HNO_{3}}{��}$Cu��NO3��2 | |
| D�� | Cu$��_{����}^{����}$CuO$\stackrel{HNO_{3}}{��}$Cu��NO3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
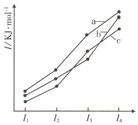
| A�� | �縺�ԣ�c��b��a | B�� | ����⻯����ȶ��ԣ�c��a��b | ||
| C�� | I5��a��c��b | D�� | ����⻯��ķе㣺a��b��c |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com