
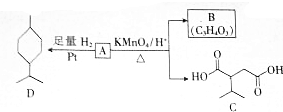
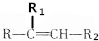 $→_{△}^{KMnO_{4}/H+}$
$→_{△}^{KMnO_{4}/H+}$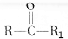 +R2COOH
+R2COOH .A与等物质的量的溴单质反应的产物有3种.
.A与等物质的量的溴单质反应的产物有3种. +H2$\stackrel{催化剂}{→}$
+H2$\stackrel{催化剂}{→}$ .
.分析 由A→D的转化加氢,有机物分子的碳链骨架没有变化,可知A分子中含有一个六元环,结合A的分子式C10H16可知还应含有两个不饱和度,再根据题中信息以及C的结构简式、B的分子式可推出A的结构简式为 ,则B的结构简式为
,则B的结构简式为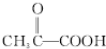 ,以此解答该题.
,以此解答该题.
解答 解:由A→D的转化加氢,有机物分子的碳链骨架没有变化,可知A分子中含有一个六元环,结合A的分子式C10H16可知还应含有两个不饱和度,再根据题中信息以及C的结构简式、B的分子式可推出A的结构简式为 ,则B的结构简式为
,则B的结构简式为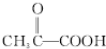 ,
,
(1)D不含苯环和碳碳双键,则不属于苯的同系物、不属于烯烃,含有环,属于环烷烃,故答案为:b;
(2)由以上分析可知A为 ,A与等物质的量的Br2进行加成反应,发生1,2-加成时得到2种,还可以发生1,4-加成,所得产物共有3种,
,A与等物质的量的Br2进行加成反应,发生1,2-加成时得到2种,还可以发生1,4-加成,所得产物共有3种,
故答案为: ;3;
;3;
(3)B的结构简式为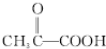 ,B的官能团名称为羰基和羧基,
,B的官能团名称为羰基和羧基,
故答案为:羰基和羧基;
(4)A的结构简式为 ,含有碳碳双键,根据D的结构简式可知,D中均为单键,所以鉴别A和D的试剂是溴水或酸性高锰酸钾溶液,
,含有碳碳双键,根据D的结构简式可知,D中均为单键,所以鉴别A和D的试剂是溴水或酸性高锰酸钾溶液,
故答案为:溴水或酸性高锰酸钾溶液;
(5)A生成D的化学方程式为 +H2$\stackrel{催化剂}{→}$
+H2$\stackrel{催化剂}{→}$ ,
,
故答案为: +H2$\stackrel{催化剂}{→}$
+H2$\stackrel{催化剂}{→}$ ;
;
(6)B的结构简式为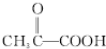 ,结合C的结构简式可知,
,结合C的结构简式可知,
a.它们都是烃的衍生物,故a正确;
b.它们都含有羧基,都能和碳酸氢钠反应,能产生二氧化碳,故b正确;
c.它们分子中氧原子数不现,所以不属于同分异构体,故c错误;
d.它们所含不同官能团,所以不属于同系物,故d错误,
故答案为:ab;
(7)根据D的结构简式可知,D的分子式为C10H20,D 的一种同分异构体,能使溴水褪色,说明有碳碳双键,且在核磁共振氢谱上有2个峰,则符合条件的结构简式为(CH3)3CCH=CHC(CH3)3,
故答案为:(CH3)3CCH=CHC(CH3)3;
点评 本题考查有机合成的分析和推断,为高频考点,侧重于学生的分析能力的考查,注意把握常见有机物的官能团的性质,注意反应条件,比较反应物和生成物的结构确定反应是解答关键,题目难度中等.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 一定条件下的可逆反应,反应物的转化率不可能达到100% | |
| B. | △H<0,△S>0的化学反应一定能自发进行 | |
| C. | 已知C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.5kJ/mol,说明碳的燃烧热为110.5kJ/mol | |
| D. | 同一反应中,△H的大小与化学反应中参加反应的物质的量无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L H2O含有分子数为NA | |
| B. | 分子总数为NA的N2、CO混合气体体积约为22.4 L,质量为28 g | |
| C. | 常温常压下,1.6 g CH4含原子数为0.5NA | |
| D. | 4 g金属钙变成钙离子时失去的电子数目为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
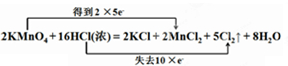 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②③⑤ | C. | ②④⑤ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 温度/℃ | 400 | 500 | 600 |
| SO2转化率/% | 99.2 | 93.5 | 73.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(s)+O2(g)═CO(g);△H=-393.5 kJ/mol | |
| B. | 2H2(g)+O2(g)═2H2O(g);△H=+571.6 kJ/mol | |
| C. | CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H=-890.3 kJ/mol | |
| D. | $\frac{1}{2}$C6H12O6(s)+3O2(g)═3CO2 (g)+3H2O(l);△H=-1400 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用已知浓度NaOH溶液滴定未知浓度盐酸,滴定终点时,俯视刻度线,则测得盐酸浓度偏小 | |
| B. | 用新制氢氧化铜悬浊液可以鉴别乙酸、葡萄糖和淀粉三种溶液 | |
| C. | 通常采用产生气泡的快慢,来比较不同条件下Na2S2O3溶液与稀硫酸的反应速率 | |
| D. | 受强酸或强碱腐蚀致伤时,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗,并视情况作进一步处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠溶液与盐酸反应:Na2CO3+2H+═2Na++H2O+CO2↑ | |
| B. | 氧化铜与硫酸溶液反应:Cu2++2H+═Cu2++H2O | |
| C. | 锌与稀硫酸反应:Zn+2H+═Zn2++H2↑ | |
| D. | 硫酸铜溶液中放入铁片:3Cu2++2Fe═2Fe3++3Cu |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com