
����Ŀ��һ���¶��£���10 mL 0.40 mol��L��1 H2O2��Һ�м�������FeCl3��Һ����ͬʱ�̲������O2�����(������Ϊ��״��)���±���ʾ��
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
������ʾ����Ӧ���������У��� 2Fe3+��H2O2 == 2Fe2+��O2����2H+���� H2O2��2Fe2+��2H+ == 2H2O��2Fe3+����Ӧ�����������仯����ͼ��ʾ������˵���������
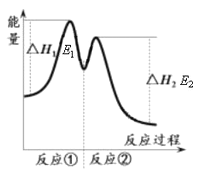
A. Fe3+�������������������ķֽ�����
B. ��Ӧ�������ȷ�Ӧ����Ӧ���Ƿ��ȷ�Ӧ
C. ��Ӧ2H2O2(aq) == 2H2O(l)��O2(g)����H��E1��E2��0
D. 0��6 min��ƽ����Ӧ���ʣ�v(H2O2)��3.33��10��2 mol��L��1��min��1
���𰸡�C
�������������ܷ�Ӧ![]() ,Fe3+�Ǵ����������������������ķֽ���������A��ȷ����Ӧ����������������ڷ�Ӧ������������ȷ�Ӧ����Ӧ�������������С�ڷ�Ӧ��������Ƿ��ȷ�Ӧ����B��ȷ���ʱ�=�����������������Ӧ�������������Ӧ2H2O2(aq) == 2H2O(l)��O2(g)����H
,Fe3+�Ǵ����������������������ķֽ���������A��ȷ����Ӧ����������������ڷ�Ӧ������������ȷ�Ӧ����Ӧ�������������С�ڷ�Ӧ��������Ƿ��ȷ�Ӧ����B��ȷ���ʱ�=�����������������Ӧ�������������Ӧ2H2O2(aq) == 2H2O(l)��O2(g)����H![]() E1��E2����C������0��6 min�������������ʵ�����0.001mol������H2O2�����ʵ�����
E1��E2����C������0��6 min�������������ʵ�����0.001mol������H2O2�����ʵ�����![]() 0.002mol������v(H2O2)��3.33��10��2 mol��L��1��min��1����D��ȷ��
0.002mol������v(H2O2)��3.33��10��2 mol��L��1��min��1����D��ȷ��


 ���㼤�������100�ִ��Ծ�ϵ�д�
���㼤�������100�ִ��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ϊ98%��Ũ���ᣨ��=l.84g��cm-3������240mLl.84mol��L-1ϡ���ᣬ���в�����ȷ���� ( )
A. ������ˮ����ע��ʢ��һ����Ũ������ձ��У������Ͻ�������ȴ
B. ����Ķ���������100mL��Ͳ��250mL����ƿ��������ƽ
C. ��������ƿ�м�������ˮ�������õ�Ũ����ע������ƿ����ˮ����
D. ��ȡŨ��������Ϊ25.0mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��ȷ����
A. ����������������Һ��Ӧ��H++ OH��= H2O
B. ϡH2SO4�����۷�Ӧ��2Fe+6H+=2Fe3++ 3H2��
C. ����ͨ��ˮ�У�Cl2��H2O![]() 2H+��Cl����ClO��
2H+��Cl����ClO��
D. AlCl3��Һ�м��������İ�ˮ��Al3++ 3NH3��H2O = Al(OH)3��+3NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ�����ڱ���һ���֣��������е���ĸ�ֱ����һ�ֻ�ѧԪ�أ��Իش��������⣺ 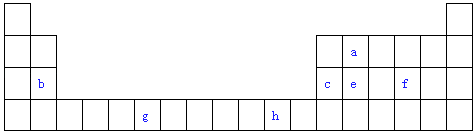
��1��д��Ԫ��g�Ļ�̬ԭ�ӵ����Ų�ʽ ��
��2��f�ڿ�����ȼ�ղ���ķ��ӹ���Ϊ �� ����ԭ�ӵ��ӻ���ʽΪ �� �÷�������ѡ����ԡ������Ǽ��ԡ������ӣ�
��3����aԭ�Ӹ�eԭ����1��1������϶��γɵľ��壬�����뾧��e��ͬ����������۵���ߵ������ѧʽ�����Դӽṹ�Ƕȼ��Խ��� ��
��4��c���ʾ�����ԭ�ӵĶѻ���ʽ��ͼ����ʾ���侧��������ͼ����ʾ��ԭ��֮���λ�ù�ϵ��ƽ��ͼ��ͼ����ʾ�� 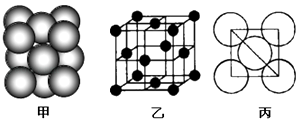
����֪c��ԭ�Ӱ뾶Ϊd���ף�NA��������٤��������c�����ԭ������ΪM����ش�
�پ�����cԭ�ӵ���λ��Ϊ �� ��ʾԭ�ӿռ�ռ���ʵĴ���ʽΪ ��
�ڸþ�����ܶ�Ϊg/cm3���ú��й���ĸ�Ĵ���ʽ��ʾ����b��h�У���c���ʾ�����ԭ�ӵĶѻ���ʽ��ͬ��������Ԫ�ط��ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ŀ�ĵ�������һ�����ʶԲ������п�ʴ���Ƴɵģ����������ǣ�������
A.����
B.�ռ�
C.����
D.�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ijһԪ�ȴ�������A����ʽΪC6H11Cl�����Է�����ͼ��ʾ��ת���� 
�ṹ��������A������ֻ����һ������A�ĺ˴Ź�������������壬�����֮��Ϊ1��1��2��3��4��Aת��ΪBʱ���ɵ��л���ֻ������һ�֣���ش��������⣺
��1��д����Ӧ���ͣ�C��E �� E��G ��
��2��д���ṹ��ʽ��F �� E ��
��3��д����Ӧ����ʽ��A��B �� C��D ��
��4������ʽ��E��ͬ����������5��̼ԭ�ӵĶ�Ԫ�����ͬ���칹�����֣������������칹����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ͻ�8.3g����300mL2mol/L����ʱ���ڱ�״���²�������5.6L������Ӧ�����Һ�м��������ռ���Һ����ֽ��������ɳ������������Ϊ
A. 9g B. 16.8g C. 18.5g D. 22.5g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������ܴﵽʵ��Ŀ�ĵ���
ѡ�� | ʵ����� | ʵ��Ŀ�� |
A | ��ʢ��2mL0.1mo/LAgNO3��Һ���Թ��еμ�һ����0.1mo/LNaCl��Һ���������еμ�һ����0.1mol/LKI��Һ | ֤����ͬ�¶��µ��ܶȻ�����Ksp(AgCl)>Ksp(AgI) |
B | ȡ��֧�Թܣ��ֱ����4mL0.01mol/LKMnO4������Һ��Ȼ����һ֧�Թ��м���0.1mol/LH2C2O4Һ2mL������һ֧�Թ��м���0.1mol/L H2C2O4Һ4mL����¼��ɫʱ�� | ֤������Ũ��Խ��Ӧ����Խ�� |
C | ��ʢ��1mLŨ������Թ��м���5mL0.01mol/LK2Cr2O7��Һ | ֤�������������Ũ�ȣ�ʹƽ��Cr2O72-(��ɫ)+H2O |
D | �����BaCO3������NaOH��Һ��������֪Ũ�ȵ�����(�÷�̪��ָʾ��) | �ζ����е�NaOH���� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ͼ1��ʾ���ף�P4���ķ��ӽṹ��ͼ2��ʾ���������ף�P4O6���ķ��ӽṹ��ͼ3��ʾ���������ף�P4O10���ķ��ӽṹ������˵������ȷ���ǣ� �� 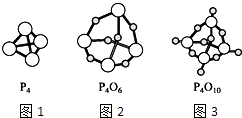
A.P4O6�е���ԭ�Ӳ���sp2��ʽ�ӻ�
B.���������ס��������������������ƶ���ʾ���ӵ�ʵ�����
C.P4��P4O6��P4O10������ͬһPԭ����������ѧ��֮��ļнǶ���60��
D.P4O6������4��Pԭ�ӹ����������壬6��Oԭ�ӹ�����������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com