
 ;
;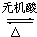 CH3COOH+(CH3)2CHOH.
CH3COOH+(CH3)2CHOH. 分析 有机物分子中N(H)=$\frac{102×9.8%}{1}$=10,故N(O)=$\frac{10}{5}$=2,N(C)=$\frac{102-10-16×2}{12}$=5,故该有机物的分子式为C5H10O2,一定条件下,A与一定氢气反应生成B,A含有不饱和键,B分子的结构可视为一个碳原子上连接两个甲基和另外两个结构相同的基团,则B为 ,故A为
,故A为 .
.
解答 解:(1)有机物分子中N(H)=$\frac{102×9.8%}{1}$=10,故N(O)=$\frac{10}{5}$=2,N(C)=$\frac{102-10-16×2}{12}$=5,故该有机物的分子式为C5H10O2,
故答案为:C5H10O2;
(2)①一定条件下,A与一定氢气反应生成B,B分子的结构可视为一个碳原子上连接两个甲基和另外两个结构相同的基团,则B为 ,则A为
,则A为 ,
,
故答案为: ;
;
②A中含有-CHO,能发生还原反应,含有-OH,能发生取代、酯化反应,由于相邻C原子上没有H原子,则不能发生消去反应,故答案为:b.
(3)A( )还有另一类酯类同分异构体,该异构体在酸性条件下水解,生成两种相对分子质量相同的化合物,则为乙酸与丙醇,其中一种的分子中有2个甲基,则为2-丙醇,A的同分异构体为CH3COOCH(CH3)2,此反应的化学方程式是:CH3COOCH(CH3)2+H2O
)还有另一类酯类同分异构体,该异构体在酸性条件下水解,生成两种相对分子质量相同的化合物,则为乙酸与丙醇,其中一种的分子中有2个甲基,则为2-丙醇,A的同分异构体为CH3COOCH(CH3)2,此反应的化学方程式是:CH3COOCH(CH3)2+H2O 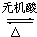 CH3COOH+(CH3)2CHOH,
CH3COOH+(CH3)2CHOH,
故答案为:CH3COOCH(CH3)2+H2O 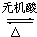 CH3COOH+(CH3)2CHOH.
CH3COOH+(CH3)2CHOH.
点评 本题考查有机物的推断、有机物官能团的结构和性质、限制条件同分异构体书写等,熟练掌握官能团的性质与转化,是对有机化学基础的综合考查,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 溴水,浓H2SO4 | B. | 酸性KMnO4溶液,浓H2SO4 | ||
| C. | 澄清石灰水,浓H2SO4 | D. | 浓H2SO4,溴水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应①为取代反应,有机产物与水混合浮在上层 | |
| B. | 反应③为取代反应,有机产物是一种烃 | |
| C. | 反应②为氧化反应,反应现象是火焰明亮并带有浓烟 | |
| D. | 反应④中1 mol苯最多与3 mol H2发生加成反应,是因为苯分子含有三个碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯与环丁烷互为同系物 | |
| B. | 碳氢化合物中的化学键都是极性键 | |
| C. | 乙醇与金属钠反应时,乙醇分子中的C-H键断裂 | |
| D. | 苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
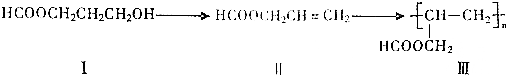
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀pH | 1.9 | 7.0 | 3.4 |
| 完全沉淀pH | 3.2 | 9.0 | 4.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com