
【题目】假设图中原电池产生的电压、电流强度均能满足电解、电镀要求,即为理想化。①~⑧为各装置中的电极编号。当K闭合后,下列说法正确的有( )

①D装置中纯Cu电极反应为:Cu2++2e-=Cu
②整个电路中电子的流动方向为:③→②;①→⑧;⑦→⑥;⑤→④;
③C装置原理上是一个电镀池(Ag表面镀Cu),期中Cu作阴极,Ag作阳极
④A装置中C电极反应为:O2+4e-+2H2O=4OH-
A. ③④ B. ①② C. ②③④ D. ①②④
科目:高中化学 来源: 题型:
【题目】碳酸二甲酯(CH3O)2CO]是一种具有发展前景的“绿色”化工产品,电化学合成碳酸二甲酯的工作原理如图所示(加入两极的物质均是常温常压下的物质)。下列说法正确的是

A. H+由石墨2极通过质子交换膜向石墨l极移动
B. 石墨l极发生的电极反应为:2CH3OH+CO-e-=== (CH3O)2CO+H+
C. 石墨2极与直流电源正极相连
D. 电解一段时间后,阴极和阳极消耗的气体的物质的量之比为l∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可从铅蓄电池中回收铅,实现铅的再生。在工艺中得到含Na2PbCl4的电解液,电解Na2PbCl4溶液后生成Pb,如图所示。下列说法不正确的是

A. 阳极区会有气泡冒出,产生O2
B. 一段时间后,阳极附近pH明显增大
C. 阴极的电极反应方程式为PbCl42+ 2e ![]() Pb + 4Cl-
Pb + 4Cl-
D. Na2PbCl4浓度下降后可在阴极区加入PbO,实现电解液的继续使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组探究过量甲醛与新制氢氧化铜的反应,探究过程如下:
(一)提出猜想
(1)甲同学通过查阅资料,提出猜想1和猜想2。
猜想1:HCHO + Cu(OH)2![]() Cu + CO↑+ 2H2O
Cu + CO↑+ 2H2O
猜想2:HCHO + 4Cu(OH)2 + 2NaOH![]() 2Cu2O + Na2CO3 + 6H2O
2Cu2O + Na2CO3 + 6H2O
猜想1和猜想2均体现了甲醛的________性。
(2)乙同学类比乙醛与新制氢氧化铜的反应,提出猜想3。
用化学方程式表示猜想3:________。
(二)进行实验,收集证据
已知:可用银氨溶液检测CO,反应为CO + 2Ag(NH3)2OH ![]() 2Ag↓+ (NH4)2CO3 + 2NH3。实验在如下装置中进行。反应结束后,A中生成紫红色固体沉淀物,C中银氨溶液无明显变化,气囊略鼓起。
2Ag↓+ (NH4)2CO3 + 2NH3。实验在如下装置中进行。反应结束后,A中生成紫红色固体沉淀物,C中银氨溶液无明显变化,气囊略鼓起。
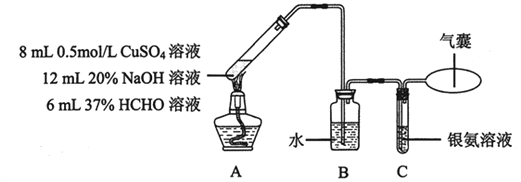
(3)配制银氨溶液所需的试剂是________。
(4)装置B中水的作用是________。
(5)甲同学取A中反应后溶液加入到足量稀盐酸中,无明显现象。乙同学另取该溶液加入到BaCl2溶液中,产生大量白色沉淀。
实验方案明显不合理的是________(填“甲”或“乙”),理由是________。
(6)已知Cu2O![]() Cu + CuSO4。
Cu + CuSO4。
丙同学通过实验证明生成的紫红色固体沉淀物是Cu,其实验方案为________。
(三)得出结论
(7)写出过量甲醛与新制氢氧化铜可能发生反应的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于 ,下列结论正确的是( )
,下列结论正确的是( )
A. 该有机物分子式为C13H16 B. 该有机物属于苯的同系物
C. 该有机物分子至少有4个碳原子共直线 D. 该有机物分子最多有13个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇分子中不同的化学键如图,关于乙醇在各种反应中断裂键的说法不正确的是( )

A. 乙醇和钠反应,键①断裂
B. 在Ag催化下和O2反应,键①③断裂
C. 乙醇和浓H2SO4共热140℃时,键①或键②断裂;在170℃时,键②⑤断裂
D. 乙醇完全燃烧时断裂键①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分弱酸的电离平衡常数如表所示:
弱酸 | HCOOH | HCN | H2CO3 |
电离平衡常数(25℃) | K=1.77×10-4 | K=6.2×10-10 | K1=4.4×10-7 K2=4.7×10-11 |
下列选项错误的是( )
A. 2CN-+H2O+CO2===2HCN+CO![]()
B. 2HCOOH+CO![]() ===2HCOO-+H2O+CO2↑
===2HCOO-+H2O+CO2↑
C. 中和等体积,等pH的HCOOH和HCN消耗NaOH的量前者小于后者
D. 等体积等浓度的HCOONa和NaCN溶液中所含离子总数前者大于后者
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下2 mL 1 mol·L-1 NaHCO3溶液,pH约为8,向其中滴加几滴饱和CaCl2溶液,有白色沉淀和无色气体生成。下列说法中,不正确的是
A. NaHCO3溶液中,HCO3-水解程度大于其电离程度
B. NaHCO3溶液中,c(Na+) > c(HCO3-) > c(OH-) > c(H+)
C. 最终所得的混合溶液中,c(Na+) + c(H+) = c(HCO3-) + 2c(CO32-)+ c(OH-)
D. 滴加饱和CaCl2溶液促进了HCO3-的电离
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com