
【题目】乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如图所示:
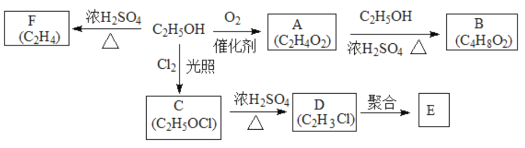
(1)A的结构简式为______。
(2)由A生成B的化学方程式为______。
(3)由乙醇生成C的反应类型为______。
(4)D中官能团名称是氯原子和______。
(5)由F生成乙醇的化学方程式为______。
(6)E的结构简式为_____。
【答案】CH3COOH CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O 取代反应 碳碳双键 CH2=CH2+H2O
CH3COOCH2CH3+H2O 取代反应 碳碳双键 CH2=CH2+H2O![]() CH3CH2OH
CH3CH2OH 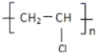
【解析】
乙醇在浓硫酸作用下加热发生消去反应生成乙烯,F是乙烯;乙醇能被氧化为乙酸,A是乙酸;乙酸、乙醇在浓硫酸催化作用下生成乙酸乙酯,B是乙酸乙酯;乙醇分子中的1个H原子被取代生成C;C在浓硫酸的作用下发生消去反应得D为CH2=CHCl,D发生加聚反应得E为 ,据此分析解答。
,据此分析解答。
(1)根据上述分析可知,A为乙酸,其结构简式为:CH3COOH;
(2)A→B为乙酸和乙醇发生酯化反应生成乙酸乙酯,反应的化学方程式为CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(3)乙醇与C的分子式比较可知,乙醇分子中的1个H原子被取代,所以反应类型为取代反应;
(4)D的结构简式为CH2=CHCl,其中官能团的名称为氯原子和碳碳双键;
(5)乙烯与水发生加成反应生成乙醇,反应的化学方程式为CH2=CH2+H2O![]() CH3CH2OH;
CH3CH2OH;
(6)D发生加聚反应得到E,E的结构简式为 。
。


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:
【题目】常见气体在标准状况下的密度为1.25 g·L-1。
(1)该气体的相对分子质量为________。
(2)若该气体的分子式为A2型,其名称为________;
若该气体的分子式为AB型,其名称为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应4 NH3(g)+5O2(g)![]() 4NO(g)+6 H2O(g),下列叙述正确的是
4NO(g)+6 H2O(g),下列叙述正确的是
A.NH3和H2O化学反应速率关系是2v正(NH3)= 3v正(H2O)
B.达到化学平衡时,4v正(O2)= 5v逆(NO )
C.达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大
D.若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、R为原子序数依次增大的短周期元素。25℃时,其最高价氧化物的水化物溶液(浓度均为0.001mol·L-1)的pH和原子半径的关系如图所示。下列说法中正确的是( )
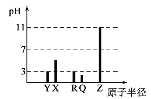
A.Y和Z的简单离子半径:Y<Z
B.R、Q的气态氢化物的稳定性:R>Q
C.R的最高价氧化物对应水化物的化学式为HRO3
D.上述五种元素中有两种元素是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:CH2=CHCH3(g)+Cl2(g)![]() CH2=CHCH2Cl(g)+HCl(g)。在一定压强下,按ω=
CH2=CHCH2Cl(g)+HCl(g)。在一定压强下,按ω=![]() 向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(
向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(![]() )与温度(T)、ω的关系,图乙表示反应的平衡常数K与温度T的关系。则下列说法正确的是( )
)与温度(T)、ω的关系,图乙表示反应的平衡常数K与温度T的关系。则下列说法正确的是( )

A.图甲中ω1>1
B.图乙中,线A表示正反应的平衡常数
C.在恒容容器中进行,压强不变时反应达到平衡状态
D.当温度为T1、ω=2时,Cl2的转化率约为33.3%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有机物结构的叙述中不正确的是
A.乙烯、溴苯分子中的所有原子均共平面
B.在有机物分子中,含有的氢原子个数一定是偶数
C.![]() 属于同种物质,说明苯分子中6个碳原子之间的键是完全一样的
属于同种物质,说明苯分子中6个碳原子之间的键是完全一样的
D.CH2Cl2只有一种结构说明甲烷分子是正四面体结构,而不是平面正方形结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大。其中X与Y可形成一种淡黄色物质P,常温下将0.05 mol P溶于水,配成1 L溶液,其中![]() ;Z为金属元素,且Z可在W的一种氧化物中燃烧,生成一种白色的物质和一种黑色的物质。下列说法错误的是()
;Z为金属元素,且Z可在W的一种氧化物中燃烧,生成一种白色的物质和一种黑色的物质。下列说法错误的是()
A. 氢化物的沸点:W<X
B. 简单离子半径:X>Y>Z
C. 化合物P中既含有离子键又含有共价键
D. W、X、Y三种元素形成的物质的水溶液显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)制取CoC2O4·2H2O工艺流程如下
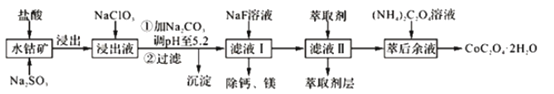
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(1)CoC2O4·2H2O中C的化合价是____________________________。
(2)写出浸出过程中Na2SO3与Co2O3发生反应的离子方程式:______________。
(3)浸出液中加入NaClO3的目的是____________________________。
(4)加Na2CO3能使浸出液中某些金属离子转化成氢氧化物沉淀,沉淀除Al(OH)3外,还有的成分是______________(填化学式),试用离子方程式和必要的文字简述其原理:____________________________。
(5)萃取剂对金属离子的萃取率与pH的关系如图,萃取剂的作用是______________;其使用的适宜pH范围是______________。
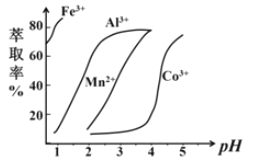
A. 2.02.5
B. 3.03.5
C. 4.04.5
(6)滤液I“除钙、镁”是将其转化为MgF2、CaF2沉淀。己知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量 NaF后,所得滤液 c(Mg2+)/c(Ca2+) =______________。
(7)用m1kg水钴矿(含Co2O360%)制备CoC2O4·2H2O,最终得到产品m2kg,产率(实际产量/理论产量×100%)为____________________________。(已知:M(Co2O3)=166, M(CoC2O4·2H2O)=183,仅需列出数字计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年为“国际化学元素周期表年”。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法不正确的是( )
![]()
A.原子半径:W<X
B.X的最高价氧化物的水化物是强碱
C.Y单质可用做半导体材料
D.气态氢化物热稳定性:Z<W
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com