
【题目】毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl22H2O的流程如图: 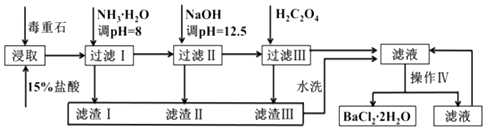
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀的pH | 11.9 | 9.1 | 1.9 |
完全沉淀的pH | 13.9 | 11.1 | 3.2 |
已知:Ksp(BaC2O4)=1.6×10﹣7 , Ksp(CaC2O4)=2.3×10﹣9
(1)实验室用37%的盐酸配制1mol/L盐酸,下列仪器中,不需要使用的是
a.容量瓶 b.量筒 c.烧杯 d.滴定管
为了加快毒重石的酸浸速率,可以采取的措施有(至少两条).
(2)加入氨水调节溶液pH=8的目的是 . 滤渣Ⅱ中含(填化学式).加入H2C2O4时应避免过量,原因是 .
(3)操作Ⅳ的步骤是:、过滤.
(4)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行.
已知:2CrO42﹣+2H+=Cr2O72﹣+H2O;Ba2++CrO42﹣=BaCrO4↓
步骤Ⅰ:移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b molL﹣1盐酸标准液滴定至终点,测得滴加盐酸体积为V0mL.
步骤Ⅱ:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b molL﹣1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL.通过计算,氯化钡溶液浓度为molL﹣1(用含字母的式子表示).
【答案】
(1)d;研磨成粉、加热、搅拌等
(2)使Fe3+形成Fe(OH)3沉淀而除去;Mg(OH)2、Ca(OH)2;H2C2O4过量会导致形成BaC2O4沉淀,产品产量减少
(3)蒸发浓缩、冷却结晶
(4)![]()
【解析】解:(1)实验室用37%的盐酸配置15%的盐酸,需量取浓盐酸的体积和水的体积,所以要用量筒,且需使用烧杯作为容器稀释,玻璃棒搅拌,不用的是滴定管,故选d,为了加快毒重石的酸浸速率,可以研磨成粉、加热、搅拌等,增大反应速率,所以答案是:d;研磨成粉、加热、搅拌等;(2)根据流程图和表中数据可知:Fe3+完全沉淀时的pH为3.2,加入氨水,调pH为8,Fe3++3NH3H2O=Fe(OH)3↓+3NH4+ , Fe3+完全沉淀,滤渣1为Fe(OH)3 , 加入氢氧化钠调节PH=12.5,Ca2+完全沉淀时的pH为13.9,Mg2+完全沉淀时的pH为11.1,Mg2+完全沉淀,Ca2+部分沉淀,滤渣Ⅱ中含Mg(OH)2、Ca(OH)2 , 溶液中主要含Ca2+、Ba2+ , Ksp(BaC2O4)=1.6×10﹣7 , Ksp(CaC2O4)=2.3×10﹣9 , 易形成CaC2O4沉淀,加入H2C2O4时应避免过量,防止CaC2O4沉淀完全后,过量的H2C2O4会导致生成BaC2O4沉淀,产品的产量减少,
所以答案是:使Fe3+形成Fe(OH)3沉淀而除去;Mg(OH)2、Ca(OH)2;H2C2O4过量会导致形成BaC2O4沉淀,产品产量减少;(3)操作Ⅳ是从氯化钡溶液中获得氯化钡晶体,可以通过蒸发浓缩、冷却结晶、过滤得到,
所以答案是:蒸发浓缩、冷却结晶;(4)步骤Ⅱ:待Ba2+完全沉淀后,再加入酸碱指示剂,用b molL﹣1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL,则发生2CrO42﹣+2H+═Cr2O72﹣+H20 的盐酸的物质的量为:V1×10﹣3×bmol,步骤Ⅰ:用b molL﹣1盐酸标准液滴定至终点,测得滴加盐酸体积为V0mL,加入的总盐酸的物质的量:V0×10﹣3×bmol,Ba2++CrO42﹣═BaCrO4↓,与Ba2+反应的CrO42﹣的物质的量为V0×10﹣3×bmol﹣V1×10﹣3×bmol=(V0﹣V1)b×10﹣3mol,步骤Ⅱ:移取y mLBaCl2溶液于锥形瓶中,所以BaCl2溶液的浓度为: ![]() mol/L=
mol/L= ![]() mol/L,若步骤Ⅱ中滴加盐酸时有少量待测液溅出,V1减小,则Ba2+浓度测量值将偏大,
mol/L,若步骤Ⅱ中滴加盐酸时有少量待测液溅出,V1减小,则Ba2+浓度测量值将偏大,
所以答案是: ![]() .
.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】制备二氧化硫并研究其性质,如图所示. 
(1)A中铜与浓硫酸反应的化学方程式是 .
(2)B、C中的实验现象分别是、 .
(3)浸氢氧化钠溶液的棉花团的作用是 , 反应的离子方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过量的下列溶液与水杨酸( ![]() )反应能得到化学式为C7H5O3Na的是( )
)反应能得到化学式为C7H5O3Na的是( )
A.NaHCO3溶液
B.Na2CO3溶液
C.NaOH溶液
D.NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.4g NaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1molL﹣1稀盐酸.下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是( )
A.
B.
C.
D.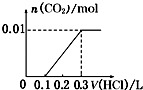
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将汽车尾气中含有的CO利用不仅能有效利用资源,还能防治空气污染.工业上常用CO与H2在由Al、Zn、Cu等元素形成的催化剂作用下合成甲醇.
(1)图1是某同学画出CO分子中氧原子的核外电子排布图, 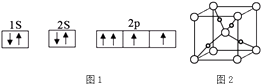
请判断该排布图(填“正确”或“错误”),理由是(若判断正确,该空不用回答).
(2)写出两种与CO互为等电子体的离子 .
(3)向CuSO4溶液中加入足量氨水可得到深蓝色[Cu(NH3)4]SO4溶液,[Cu(NH3)4]SO4中 所含配位键是通过配体分子的给出孤电子对,接受电子对形成,SO42﹣的空间构型是 , 该物质中N、O、S三种元素的第一电离能大小顺序为>>(填元素符号).
(4)甲醇与乙烷的相对分子质量相近,故二者分子间的作用力(范德华力)相近,但是二者沸点的差距却很大,造成该差异的原因是;在甲醇分子中碳原子轨道的杂化类型为 .
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图2所示:
①在该晶胞中,Cu+的配位数是 ,
②若该晶胞的边长为a pm,则Cu2O的密度为gcm﹣3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于维生素的下列说法正确的是( )
A.维生素是生物生长发育和新陈代谢所必需的物质
B.维生素容易在体内积存,主要积存在肝脏
C.维生素容易被人体吸收,多余的随尿排出体外,不易在体内积存,所以容易缺乏
D.维生素都是强还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是动植物生长不可缺少的元素,含氮化合物也是重要的化工原料.自然界中存在如下氮的循环过程,工业上也可通过一系列的化学反应模拟该过程,实现氮的转化.
(1)请写出过程①中雷电固氮的化学反应方程式 .
(2)过程③中NH3在土壤中会被微生物转化成HNO2 , 过程④中HNO2会被微生物继续转化为HNO3 , 试写出过程③的化学方程式 .
(3)工业上利用氢气与空气中分离出的氮气合成氨气,模拟实现过程②,写出工业合成氨反应的方程式 .
(4)工业上利用氨气制备硝酸.同学甲欲探究硝酸能否与H后金属发生反应,做了如下实验:向盛有稀硝酸的试管中加入Cu片,请你写出相关的实验现象 , 该实验的结论是 .
(5)实验室中用NaNO2与氯化铵共热制取N2 , 该反应体现了NaNO2的性,亚硝酸钠暴露于空气中会生成 , 体现了NaNO2的性. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素性质呈现周期性变化的根本原因是( )
A. 核外电子排布呈周期性变化B. 元素的相对原子质量逐渐增大
C. 核电荷数逐渐增大D. 元素化合价呈周期性变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com