
白云石的主要成分为CaCO3、MgCO3,还含有少量Fe、Si的化合物,实验室以白云石为原料制Mg(OH)2及CaCO3。步骤如下:

实验过程中需要的数据见下表:
|
|
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
Fe3+ |
1.9 |
3.2 |
|
Fe2+ |
7.0 |
9.0 |
|
Mg2+ |
9.5 |
11.0 |
请回答下列问题:
(1)过滤中所需的玻璃仪器是 。溶液A中含有Ca2+,Mg2+,Fe2+,Fe3+,则试剂①可选择
(填字母)
A.KMnO4 B.Cl2 C.H2O2
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是 ,然后通入CO2。通入CO2气体时请把右边的装置图补充完整(不允许更换溶液,导气管以下连接的仪器自选)。
(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为 。

(4)若将制取的Mg(OH)2:加入到某聚乙烯树脂中,树脂可燃性大大降低,Mg(OH)起阻燃作用的主要原因是 。
(12分)(1)玻璃棒、烧杯、漏斗(2分);BC(2分)
(2)NH3(1分);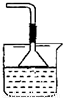 (2分,使用干燥管也得分)
(2分,使用干燥管也得分)
(3) Ksp[Fe(OH)3]<Ksp[Fe(OH)2]<Ksp[Mg(OH)2](2分)
(4)Mg(OH)2受热分解时吸收大量的热,使环境温度下降;同时生成耐高温、稳定性好的MgO覆盖在可燃物表面,阻燃效果更佳。(2分,答出其中一个方面即可)
【解析】
试题分析:根据流程可知,白云石加盐酸反应后的溶液中主要为氯化钙、氯化镁、氯化亚铁、氯化铁,加试剂①将亚铁离子氧化为铁离子,再加氧化镁除去铁离子,溶液C中主要含Ca2+、Mg2+,加CaO促进镁离子水解从而除去镁离子。
(1)过滤操作中的主要仪器是铁架台(带铁圈)、烧杯、玻璃棒、漏斗,因此主要的玻璃仪器是烧杯、玻璃棒、漏斗。由于选择氧化剂时不能引入新的杂质,高锰酸钾的还原产物是Mn2+,属于杂质,因此不能选择高锰酸钾溶液,所以试剂①为氯气或双氧水,即答案选B或C。
(2)CO2溶于水,溶液显酸性,不能和氯化钙反应生成白色沉淀。所以要制备碳酸钙沉淀,应该首先通入氨气,然后再通入CO2。由于氨水溶液显碱性,所以通入二氧化碳时应注意防止倒吸,因此正确的装置图可以为 。
。
(3)由表格中的数据可知,沉淀的pH越小,则溶度积越小。所以Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序Ksp[Fe(OH)3]<Ksp[Fe(OH)2]<Ksp[Mg(OH)2]。
(4)Mg(OH)2起阻燃作用的主要原因是Mg(OH)2受热分解时吸收大量的热,使环境温度下降;同时生成耐高温、稳定性好的MgO覆盖在可燃物表面,阻燃效果更佳。故答案为:Mg(OH)2受热分解时吸收大量的热,使环境温度下降;同时生成耐高温、稳定性好的MgO覆盖在可燃物表面,阻燃效果更佳.
考点:考查过滤操作、氧化剂的选择;碳酸钙制备、防倒吸装置的选择;溶度积常数的判断以及氢氧化镁的性质与用途等


 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:

| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |



查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |

查看答案和解析>>
科目:高中化学 来源: 题型:
白云石的主要成分为CaCO3·MgCO3,还含有少量Fe、Si的化合物。实验室以白云石为原料制备Mg(OH)2及CaCO3。步骤如下:

实验过程中需要的数据见下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
请回答下列问题:
(1)溶液A中含有Ca2+、Mg2+、Fe2+、Fe3+,则试剂①可选择_________(填字母,下同);试剂②可选择_________;试剂③可选择_________。
(A)KMnO4(B)Cl2(C)MgO(D)CaO
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是_______,然后通入CO2。通入CO2气体应选择的最佳装置为_______(填字母)。

(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为________________________________。
(4)将制取的Mg(OH)2煅烧得到MgO,然后在还原炉(真空)中,1200℃条件下,用硅铁(铁不参与反应)还原生成镁蒸气。在还原过程中反应温度对生成金属镁的影响如下图:

煅烧Mg(OH)2所需要的仪器除三角架、酒精灯外,还必须选择___________。MgO与硅铁发生的反应达到平衡后,平衡常数表达式为_______________________。由图可知,还原反应的△H ____0(填“>”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
白云石的主要成分为CaCO3·MgCO3,还含有少量Fe、Si的化合物。实验室以白云石为原料制备Mg(OH)2及CaCO3。步骤如下:

实验过程中需要的数据见下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
请回答下列问题:
(1)溶液A中含有Ca2+、Mg2+、Fe2+、Fe3+,则试剂①可选择_________(填字母,下同);试剂②可选择_________;试剂③可选择_________。
(A)KMnO4(B)Cl2(C)MgO(D)CaO
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是_______,然后通入CO2。通入CO2气体应选择的最佳装置为_______(填字母)。

(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为________________________________。
(4)将制取的Mg(OH)2煅烧得到MgO,然后在还原炉(真空)中,1200℃条件下,用硅铁(铁不参与反应)还原生成镁蒸气。在还原过程中反应温度对生成金属镁的影响如下图:

煅烧Mg(OH)2所需要的仪器除三角架、酒精灯外,还必须选择___________。MgO与硅铁发生的反应达到平衡后,平衡常数表达式为_______________________。由图可知,还原反应的△H ____0(填“>”或“<”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com