
【题目】过度肥胖者的脂肪组织中,占细胞质量50%以上的物质是( )
A. 蛋白质 B. 脂肪 C. 糖类 D. 水
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A.图I表示常温下盐酸滴加到0.1mol/L某强碱溶液得到的滴定曲线
B.图II表示一定条件下进行的反应2SO2+O2![]() 2SO3各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积
2SO3各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积
C.图III表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20mlBa(OH)2溶液时铝离子恰好沉淀完全
D.图IV表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中充入等物质的量的气体A和B,一定温度下发生如下反应:A(g)+xB(g) ![]() 2C(g)。达到平衡后,只改变反应的一个条件,测得容器中物质的浓度,反应速率随时间的变化关系如图所示。下列说法中正确的是
2C(g)。达到平衡后,只改变反应的一个条件,测得容器中物质的浓度,反应速率随时间的变化关系如图所示。下列说法中正确的是

A.8min时表示正反应速率等于逆反应速率
B.前20minA的反应速率为0.05mol/(L·min)
C.反应方程式中的x=1,30min时表示增大压强
D.40min时改变的条件是升高温度,且正反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:2Al(s)+O2(g)=Al2O3(s) △H=-1644.3kJ·mol-1
2Fe(s)+O2(g)=Fe2O3(s) △H=-815.88kJ·mol-1
写出铝粉与氧化铁粉末发生铝热反应的热化学方程式 。
(2)高铁酸钾(K2FeO4)在水中的反应为4FeO42-+10H2O![]() 4Fe(OH)3+8OH-+3O2。图1是25℃时K2FeO4在不同pH溶液中浓度的变化情况,图2是K2FeO4在不同温度时溶液浓度的变化情况。
4Fe(OH)3+8OH-+3O2。图1是25℃时K2FeO4在不同pH溶液中浓度的变化情况,图2是K2FeO4在不同温度时溶液浓度的变化情况。

①pH=4.74时,反应从开始到800min时平均反应速率v(OH-)= 。
②图1在800min后,三种溶液中的c(FeO42-)均不再改变。随着pH的变大,此反应的平衡常数K (填“变大”、“变小”或“不变”)。
③图2在240min后,四种溶液中FeO42-的浓度不再变化,下列说法正确的是
a.上述反应的△H>0 b.升高温度,该反应pH减小
c.温度越高,反应速率越慢 d.加入盐酸,FeO42-的浓度减小
④FeO42-在水溶液中的存在形态如图3所示。下列说法正确的是

A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=10的这种溶液中加硫酸至pH=2,HFeO4-的分布分数逐渐变大
C.向pH=6的这种溶液中加KOH溶液,发生反应的离子方程式为:HFeO4-+OH-=FeO42-+H2O
⑤高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂。
已知:4FeO42-+10H2O=4Fe(OH)3+8OH-+3O2,K2FeO4在处理水的过程中所起的作用是 。
(3)常温常压下,饱和氯水中氯气总浓度约为0.09mol/L,且存在可逆反应:Cl2 + H2O ![]() HCl + HClO,实验测得约有三分之一的氯气与水发生了反应。反应Cl2+H2O
HCl + HClO,实验测得约有三分之一的氯气与水发生了反应。反应Cl2+H2O![]() HCl+HClO的平衡常数为 。
HCl+HClO的平衡常数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明缺硒可导致克山病。克山病是一种地方性心肌病,急重症病人可发生猝死。营养学和流行病学界专家认为,成人每天硒的摄取量约在40~100 μg就可满足人体需要。根据资料,下列解释不正确的是( )
A. 硒是人体必需的化学元素
B. 硒在人体生长发育过程中的作用不可替代
C. 硒的作用重大,只要有了硒,人体就能正常生长发育
D. 硒是人体必需的微量元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.根据结构对有机物进行分类,有助于对其性质的掌握。
A. B.
B. C.
C.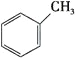
上述有机物属于芳香烃的是____________ (填字母),它与苯的关系是____________,
写出苯与溴发生反应的化学方程式___________________,
Ⅱ.下列几组物质中,互为同位素的有____________,
互为同素异形体的有___________,
互为同系物的有____________,
互为同分异构体的有____________,
属于同种物质的有____________。
①O2和O3 ②35Cl和37Cl
③![]() 和
和![]()
④ 和
和
⑤CH3(CH2)2CH3和(CH3)2CHCH3
⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素在生物体内虽然含量很少,却是维持正常生命活动不可缺少的。该观点可以通过下面哪一实例得到证明?( )
A. 缺Mg时叶片变黄 B. 油菜缺少B时只开花不结果
C. 动物血液钙盐含量太低会抽搐 D. 缺P会影响ATP的吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。已知A的气态氢化物能与其最高价氧化物的水化物反应,B原子最外层电子数是电子层数的3倍,C+和D3+离子的电子层结构相同,B与E属于同一主族。
请回答下列问题:
(1)E在元素周期表中的位置是_______________。
(2)上述元素形成的简单离子中,半径最小的是____________________(填离子符号)。
(3)由上述元素中的一种或几种组成的物质甲可以发生如下反应:

①若乙具有漂白性,则乙的电子式为__________。
②若丙的水溶液是强碱性溶液,则甲为___________或__________(填化学式)。
③若乙为二元弱酸,丙既能溶于强酸、又能溶于强碱,则乙的名称为_________;用电离方程式表示丙既能溶于强酸、又能溶于强碱的原因______________________________。
④乙遇空气变为红棕色,有同学认为“浓硫酸可以干燥气体甲”,为验证其观点是否正确。用如下装置进行实验时,分液漏斗中应加入_________(填试剂名称)。实验过程中,浓硫酸中未发现有气体逸出,且溶液变为红棕色,由此得出的结论是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组欲鉴定某硫酸钠样品中是否含有亚硫酸钠,设计方案如下:取少量固体配成溶液,往溶液中滴加少量酸性KMnO4溶液,观察溶液是否褪色。

如果溶液紫色褪去,说明该样品中含有亚硫酸钠。
(1)用离子方程式表示该反应原理: 。
(2)图I表示100mL量筒中液面的位置,A与B,B与C刻度间相差10mL,如果刻度A为30,量筒中液体的体积是____________mL。图II表示25mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填字母)________________。
A.等于amL B.等于(25-a)mL C.大于amL D.大于(25-a)mL
(3)该小组同学欲测定样品中亚硫酸钠的含量,操作步骤如下:
a.称取mg样品,用蒸馏水溶解并置于锥形瓶中
b.将V1mL C1mol/L的酸性KMnO4溶液(过量)倒入锥形瓶中振荡
c.用C2mol/L草酸钠(Na2C2O4)溶液滴定过量的KMnO4,至滴定终点时用去Na2C2O4溶液V2mL
①KMnO4溶液应装在_________式滴定管中,达到滴定终点时溶液颜色的变化 。
②样品中Na2SO3的物质的量为 mol。(用含C1 、V1 、C2、 V2的代数式表示)。
(4)下列操作会导致测得的Na2SO3的物质的量偏高的是 (填字母,双选)。
A.未用Na2C2O4标准液润洗滴定管
B.滴定前仰视盛有Na2C2O4溶液的滴定管,滴定后俯视
C.滴定前滴定管尖嘴处有气泡,滴定后消失
D.滴定时摇动锥形瓶,瓶中的液滴溅出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com