
 CO2(g)+H2(g),得到如下二组数据:
CO2(g)+H2(g),得到如下二组数据:| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
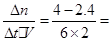 0.13mol/(L·min)
0.13mol/(L·min)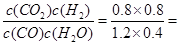 1.3(650℃)
1.3(650℃)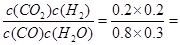 0.17(900℃)
0.17(900℃)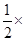 (①-②+4×③)可知:
(①-②+4×③)可知:

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源:不详 题型:单选题

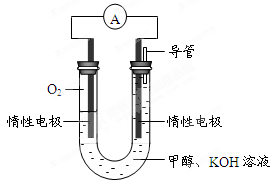
A.钢铁的腐蚀过程绝大多数都是电化学腐蚀 | B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | C.电解CuCl2饱和溶液,生成金属铜和氯气 | D.电解MgCl2饱和溶液,可制得金属镁 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.16g | B.32g | C.19.2g | D.12.8g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在潮湿的酸性土壤中 | B.在潮湿不透气的中性土壤中 |
| C.在干燥致密不透气的土壤中 | D.在潮湿透气的盐碱地中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 nLiF+nC。则下列说法不正确的是
nLiF+nC。则下列说法不正确的是 nLi+
nLi+ nC+nLiF
nC+nLiF查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
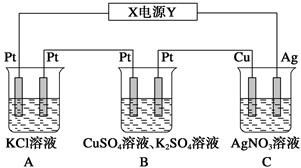
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
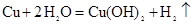 发生的是
发生的是| A.铜片作负极,碳棒作正极,氯化钠作电解质溶液 |
| B.铜锌合金在潮湿空气中发生电化学腐蚀 |
| C.用铜片作阴、阳电极,电解硫酸铜溶液 |
| D.用铜片作阴、阳电极,电解硫酸钠溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.红色铁锈的主要成分是Fe(OH)3 |
| B.钢材在空气中的反应只有氧化反应、还原反应及化合反应 |
| C.钢材在空气中的腐蚀主要为电化学腐蚀,其负极的反应为:Fe-3e-=Fe3+ |
| D.空气中阳光、雨水、湿度对钢材的腐蚀有较大影响 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com