
| A.红色铁锈的主要成分是Fe(OH)3 |
| B.钢材在空气中的反应只有氧化反应、还原反应及化合反应 |
| C.钢材在空气中的腐蚀主要为电化学腐蚀,其负极的反应为:Fe-3e-=Fe3+ |
| D.空气中阳光、雨水、湿度对钢材的腐蚀有较大影响 |
科目:高中化学 来源:不详 题型:填空题
 CO2(g)+H2(g),得到如下二组数据:
CO2(g)+H2(g),得到如下二组数据:| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.粗铜精炼时,把粗铜接在电源的负极 |
| B.充电时,把铅蓄电池的负极接在外电源的正极 |
| C.镀锡铁破损后铁更易被腐蚀 |
D.碱性氢氧燃料电池工作时,负极反应为: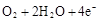 = =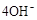 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
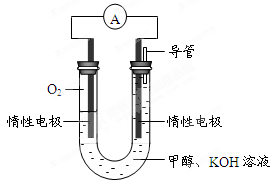
 水的产物),试用有关的电极反应式,离子方程式和化学方程式表示Fe(OH)3的生成:
水的产物),试用有关的电极反应式,离子方程式和化学方程式表示Fe(OH)3的生成: ;
;查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原电池的负极反应为:Fe-3e-→ Fe3+ |
B.发生吸氧腐蚀的总反应为:Fe +2H+ Fe2+ + H2↑ Fe2+ + H2↑ |
| C.钢铁设备上连接铜块可以防止腐蚀 |
| D.在南方沿海地区,钢铁更容易被腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

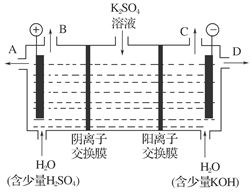
 收集到气体0.168 L(标况),若电解过程中无其他副反应发生,经测定电解后A中溶液体积恰为1000mL,求A溶液的pH。
收集到气体0.168 L(标况),若电解过程中无其他副反应发生,经测定电解后A中溶液体积恰为1000mL,求A溶液的pH。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2H+ +2e- = H2↑ | B.Fe - 2e- = Fe2+ | C.2H2O + O2 + 4e- = 4OH- | D.Fe-3 e- = Fe3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com