
| A. | 纯碱和烧碱都属于碱 | B. | 干冰和氨都属于弱电解质 | ||
| C. | 沼气和乙醇都属于可再生能源 | D. | 铝和铜在工业上都常用电解法冶炼 |
分析 A.水溶液中电离出的氢氧根离子全部是氢氧根离子的化合物为碱,纯碱是碳酸钠的俗称;
B.水溶液中部分电离的电解质为弱电解质,干冰和氨在水溶液和熔融态时均不能导电;
C.天然气、煤、石油属于化石燃料,用完之后不能再产生,属于不可再生能源.用完之后能够再产生的物质,属于可再生能源;
D.工业上常用电解法冶炼金属铝,用热还原法冶炼金属铜;
解答 解:A、纯碱是碳酸钠的俗称,属于盐类,烧碱是氢氧化钠的俗称,属于碱,故A错误;
B、干冰和氨在水溶液和熔融态时均不能导电,本身不能电离出离子属于非电解质,故B错误;
C、沼气的主要成分是天然气,属于可再生能源,乙醇属于可再生能源,故C正确;
D、工业上常用置换法来冶炼金属铜、电解氧化铝来冶炼金属铝,故D错误.
故选C.
点评 本题考查物质的分类及金属的冶炼,物质的俗称一定要熟记,根据物质的组成来确定物质所属的类别,注意常见概念的掌握,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ①③④⑤ | C. | ④⑤ | D. | ①④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
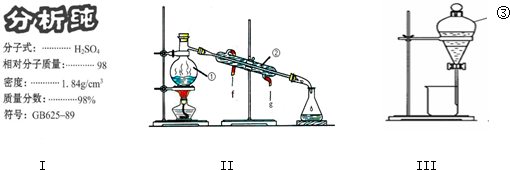
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+、Al3+、SCN-、Cl- | B. | Fe3+、Na+、S2-、Cl- | ||
| C. | K+、H+、Cl-、AlO2- | D. | Na+、Ca2+、HCO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
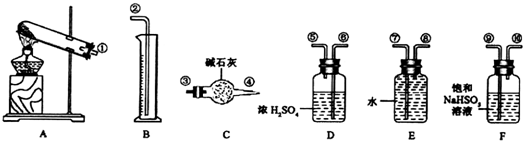
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
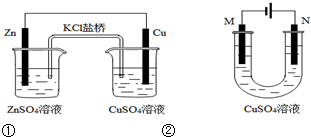
| A. | 装置①中盐桥内的K+移向CuSO4溶液 | |
| B. | 装置①将电能转变为化学能 | |
| C. | 若装置②用于铁棒镀铜,则N极为铁棒 | |
| D. | 若装置②用于电解精炼铜,则N极为粗铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应开始时的速率:甲=乙 | |
| B. | 反应所需时间:甲<乙 | |
| C. | 反应开始时,酸的物质的量浓度:乙<甲 | |
| D. | 反应结完后溶液的pH值:甲<乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | B. | NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$N2O↑+2H2O | ||
| C. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O | D. | 4HNO3═4NO2↑+O2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ② | C. | ③ | D. | ④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com