
(6分)已知2X2(g)+Y2(g) 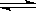 2Z(g) ΔH=-akJ·mol-1(a>0),在一个容积固定的容器中加入2mol X2和1mol Y2在500℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
2Z(g) ΔH=-akJ·mol-1(a>0),在一个容积固定的容器中加入2mol X2和1mol Y2在500℃时充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
⑴此反应平衡常数表达式为____________ _;若将温度降低到300℃,则反应平衡常数将_____(填增大、减少或不变)。
⑵若原来容器中只加入2mol Z,500℃充分反应达平衡后,吸收热量c kJ,则Z浓度_______Wmol·L—1(填“>”、“<”或“=”),a、b、c之间满足关系______ _____(用代数式表示)。
⑶能说明反应已达平衡状态的是___________________。
| A.浓度c(Z)=2c(Y2) | B.容器内压强保持不变 |
| C.v逆(X2)=2v正(Y2) | D.容器内的密度保持不变 |
(12分,每空2分).⑴ K=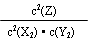 ;增大 ⑵=;a =" b" + c ⑶BC (4)变大
;增大 ⑵=;a =" b" + c ⑶BC (4)变大
解析试题分析:(1)化学常数是在一定条件下的可逆反应中,当可逆反应反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据反应的方程式可知,该反应的平衡常数的表达式K=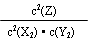 。正反应是放热反应,所以降低温度平衡向正反应方向移动,平衡常数增大。
。正反应是放热反应,所以降低温度平衡向正反应方向移动,平衡常数增大。
(2)2mol Z就相当于是2mol X2和1mol Y2,所以在温度和容器容积不变的情况下,两次平衡是等效的,因此Z的浓度仍然是Wmol·L—1。两次热效应的绝对值之和等于该反应的反应热,因此a=b+c。
(3)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。平衡时浓度不再发生变化,但各物质的浓度之间不一定相等或满足某种关系,A不正确;反应前后体积减小,所以压强也是减小,因此压强不再变化时,可以说明达到平衡状态,B正确;C中反应速率的方向相反,且满足速率之比是相应的化学计量数之比,正确;密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,D不正确,所以答案选BC。
(4)由于反应是体积减小的,因此压强也是减小的。所以如果保持恒压,则有利于平衡向正反应方向移动,反应物的转化率将增大。
考点:考查平衡常数、平衡状态以及等效平衡的判断、外界条件对平衡状态的影响等
点评:所谓等效平衡是指外界条件相同时,同一可逆反应只要起始浓度相当,无论经过何种途径,都可以达到相同的平衡状态。等效平衡的判断及处理一般步骤是:进行等效转化——边倒法,即按照反应方程式的计量数之比转化到同一边的量,与题干所给起始投料情况比较。等效平衡一般有三种类型:I类:恒温恒容下对于反应前后气体体积发生变化的反应来说(即△n≠0的体系):等效转化后,对应各物质起始投料的物质的量与原平衡起始态相同。II类:恒温恒容下对于反应前后气体体积没有变化的反应来说(即△n=0的体系):等效转化后,只要反应物(或生成物)的物质的量的比例与原平衡起始态相同,两平衡等效。III类:恒温恒压下对于气体体系等效转化后,要反应物(或生成物)的物质的量的比例与原平衡起始态相同,两平衡等效。解答该类型试题的关键是分清类别,用相应的方法求解即可。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| c2(Z) |
| c2(X)?c(Y) |
| c2(Z) |
| c2(X)?c(Y) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 相关信息 |
| X | X的一种核素质量数为14,中子数为7 |
| Y | Y的过氧化物是一种淡黄色固体,可用作供氧剂 |
| Z | Z的基态原子M层电子数比L层少2个 |
| W | W的基态原子的价电子排布式为3d104sl |
查看答案和解析>>
科目:高中化学 来源: 题型:
(16分)已知X、Y、Z、T四种元素中,只有T不是短周期元素,与它们有关部分信息如下表:
(1)Y元素位于周期表的第 周期 族;写出T基态原子电子排布式: 。
(2)X元素单质分子中含有![]() 键的键数之比为 ,其化学性质 (填“活泼”或“稳定”):
键的键数之比为 ,其化学性质 (填“活泼”或“稳定”):
(3)对Z元素的单质或化合物描述一定正确的是 。
a.单质不溶于任何溶剂 b.其最高价氧化物的水化物为弱酸
c.其最高价氧化物常温下为气态d.气态氢化物不稳定
(4)上述四种元素中,其最高价氧化物的水化物呈两性的物质是 (填化学式),试用电离方程式表示其两性的原因 。
(5)已知:①4XH3(g)+5O2(g)=4XO(g)+6H2O(g) △H=-905kJ/mol
②4XH3(g)+3O2(g)=2X2(g)+6H2O(g) △H=-1268kJ/mol
写出X2与O2反应生成XO的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2012届安徽省马鞍山市高三第一次教学质量检测理科综合试卷化学部分(解析版) 题型:填空题
(16分)已知X、Y、Z、T四种元素中,只有T不是短周期元素,与它们有关部分信息如下表:
(1)Y元素位于周期表的第 周期 族;写出T基态原子电子排布式: 。
(2)X元素单质分子中含有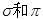 键的键数之比为 ,其化学性质 (填“活泼”或“稳定”):
键的键数之比为 ,其化学性质 (填“活泼”或“稳定”):
(3)对Z元素的单质或化合物描述一定正确的是 。
a.单质不溶于任何溶剂 b.其最高价氧化物的水化物为弱酸
c.其最高价氧化物常温下为气态d.气态氢化物不稳定
(4)上述四种元素中,其最高价氧化物的水化物呈两性的物质是 (填化学式),试用电离方程式表示其两性的原因 。
(5)已知:①4XH3(g)+5O2(g)=4XO(g)+6H2O(g) △H=-905kJ/mol
②4XH3(g)+3O2(g)=2X2(g)+6H2O(g) △H=-1268kJ/mol
写出X2与O2反应生成XO的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年安徽省马鞍山市高三第一次教学质量检测理科综合试卷化学部分(解析版) 题型:填空题
(16分)已知X、Y、Z、T四种元素中,只有T不是短周期元素,与它们有关部分信息如下表:

(1)Y元素位于周期表的第 周期 族;写出T基态原子电子排布式: 。
(2)X元素单质分子中含有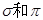 键的键数之比为 ,其化学性质
(填“活泼”或“稳定”):
键的键数之比为 ,其化学性质
(填“活泼”或“稳定”):
(3)对Z元素的单质或化合物描述一定正确的是 。
a.单质不溶于任何溶剂 b.其最高价氧化物的水化物为弱酸
c.其最高价氧化物常温下为气态d.气态氢化物不稳定
(4)上述四种元素中,其最高价氧化物的水化物呈两性的物质是 (填化学式),试用电离方程式表示其两性的原因 。
(5)已知:①4XH3(g)+5O2(g)=4XO(g)+6H2O(g) △H=-905kJ/mol
②4XH3(g)+3O2(g)=2X2(g)+6H2O(g) △H=-1268kJ/mol
写出X2与O2反应生成XO的热化学方程式 。[来源:Zxxk.Com]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com